Циклический путь АМФ и система вторичных посредников в клеточной сигнализации
Циклический путь усиления и его усилительный каскад играют ключевую роль в передаче сигнала внутри клетки. В циклическом пути АМФ (цАМФ) (рис. 5.6) активация рецептора при связывании первого посредника (например, гормона адреналина) позволяет рецептору активировать связанный с ним G-белок, известный как Gs (индекс «s» означает стимулирующий). Данная активация заставляет Gs стимулировать свой эффекторный белок — фермент плазматической мембраны аденилатциклазу (также называемую аденилатциклазой). Активированная аденилатциклаза, каталитический центр которой расположен на цитозольной поверхности плазматической мембраны, превращает цитозольный АТФ в циклический 3',5'-аденозинмонофосфат (цАМФ) (рис. 5.7). Затем циклический АМФ действует как второй мессенджер, распространяясь по всей клетке и запуская последовательность событий, приводящих к конечной реакции клетки на первый посредник.
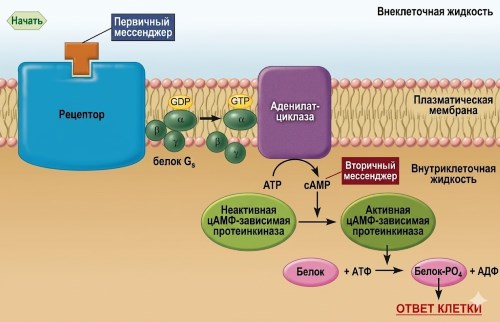
Рисунок 5.6. Система вторичного обмена циклическими АМФ. На рисунке не показан другой регуляторный белок Gi, с которым определенные рецепторы могут взаимодействовать, вызывая ингибирование аденилатциклазы.
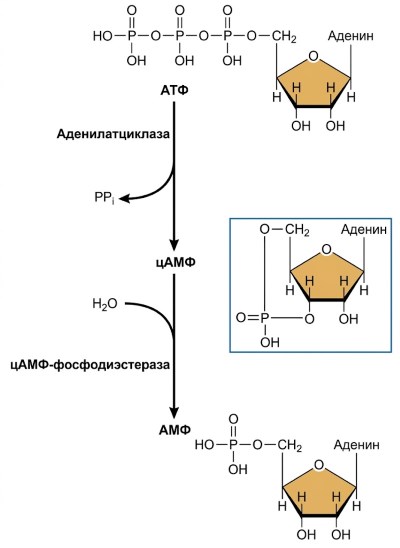
Рисунок 5.7. Образование и распад цАМФ. АТФ преобразуется в цАМФ под действием фермента плазматической мембраны аденилатциклазы. цАМФ инактивируется цитозольным ферментом фосфодиэстеразой цАМФ, которая превращает цАМФ в нециклизованную форму АМФ.
Действие цАМФ в конечном счете прекращается при его расщеплении до АМФ — реакции, катализируемой ферментом фосфодиэстеразой цАМФ (см. рис. 5.7). Данный фермент также находится под физиологическим контролем, поэтому клеточную концентрацию цАМФ можно изменять либо за счет скорости его синтеза под действием мессенджера, либо за счет скорости распада под действием фосфодиэстеразы. Кофеин и теофиллин (активные компоненты кофе и чая) являются широко используемыми стимуляторами, которые частично подавляют активность фосфодиэстеразы цАМФ, тем самым продлевая действие цАМФ в клетках. Во многих клетках, например в кардиомиоцитах, повышенная концентрация цАМФ вызывает усиление функций (увеличение частоты сердечных сокращений).
Что именно делает цАМФ внутри клетки? Он связывается с ферментом, известным как цАМФ-зависимая протеинкиназа (или протеинкиназа А), и активирует его (см. рис. 5.6). Следует напомнить, что протеинкиназы фосфорилируют другие белки — часто ферменты — путем переноса на них фосфатной группы. Изменения активности белков, фосфорилируемых цАМФ-зависимой протеинкиназой, обусловливают реакцию клетки (секрецию, сокращение и т.д.). Каждая из различных протеинкиназ, участвующих в многочисленных путях передачи сигнала, имеет свои собственные специфические субстраты.
По сути, активация аденилатциклазы белком Gs инициирует «каскад усиления», который последовательно превращает белки из неактивных форм в активные. Рисунок 5.8 иллюстрирует преимущества такого каскада. Находясь в активном состоянии, одна молекула фермента может превращать в продукт не одну, а множество молекул субстрата — например, 100. Следовательно, одна активная молекула аденилатциклазы способна катализировать образование 100 молекул цАМФ (и, соответственно, 100 активированных молекул цАМФ-зависимой протеинкиназы А). На каждом из двух последующих этапов активации фермента происходит еще одно 100-кратное усиление, так что одна молекула первого посредника может привести к образованию 1 миллиона молекул продукта. Это помогает объяснить, как гормоны и другие посредники эффективны при крайне низких внеклеточных концентрациях. Например, одна молекула адреналина способна заставить печень вырабатывать и высвобождать 10⁸ молекул глюкозы.
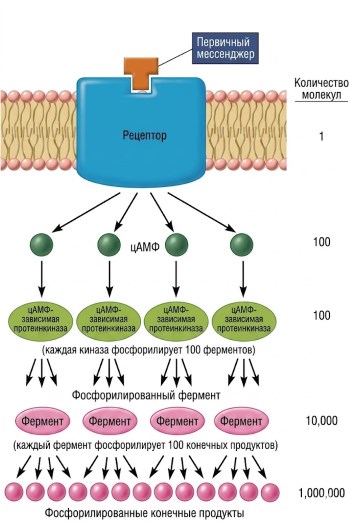
Рисунок 5.8. Пример усиления сигнала. В данном примере одна молекула первого мессенджера приводит к образованию 1 миллиона конечных продуктов. Другие пути передачи второго мессенджера имеют сходные процессы усиления. Этапы между активацией рецептора и генерацией цАМФ опущены для простоты.
Кроме того, активированная цАМФ-зависимая протеинкиназа может проникать в ядро клетки, где фосфорилирует белок, который затем связывается со специфическими регуляторными участками определенных генов (считается, что такие гены реагируют на цАМФ). Следовательно, действие цАМФ может быть быстрым и не зависеть от изменений в активности генов (например, при выработке адреналина и глюкозы) либо более медленным и зависеть от образования новых генных продуктов. Как активация одной молекулой цАМФ (цАМФ-зависимой протеинкиназы) может быть общей для столь разнообразных биохимических последовательностей и клеточных реакций? Ответ заключается в том, что цАМФ-зависимая протеинкиназа способна фосфорилировать большое количество различных белков (рис. 5.9), оказывая множественное действие в пределах одной клетки и различное — в разных клетках.
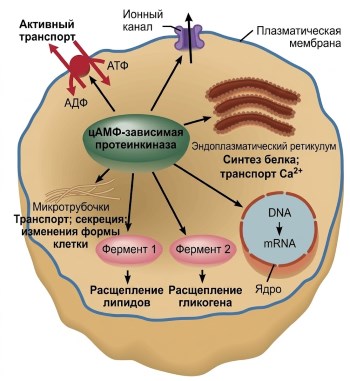
Рисунок 5.9. Разнообразие клеточных реакций, индуцируемых цАМФ, обусловлено главным образом тем, что активированная цАМФ-зависимая протеинкиназа может фосфорилировать множество различных белков, активируя или ингибируя их. На рисунке показана протеинкиназа, фосфорилирующая семь различных белков: белок микротрубочек, АТФазу, ионный канал, белок эндоплазматического ретикулума, белок, участвующий в стимуляции транскрипции гена в мРНК, и два фермента.
Например, адреналин через цАМФ-путь воздействует на жировые клетки, стимулируя расщепление триглицеридов — процесс, опосредованный особым фосфорилированным ферментом, который преимущественно экспрессируется в адипоцитах. В печени адреналин через цАМФ стимулирует как гликогенолиз, так и глюконеогенез — процессы, опосредуемые фосфорилированными ферментами, отличными от тех, которые экспрессируются в жировых клетках. В то время как фосфорилирование, опосредованное цАМФ-зависимой протеинкиназой, активирует одни ферменты, оно ингибирует другие. Например, фермент, катализирующий скорость-лимитирующую стадию синтеза гликогена, подавляется фосфорилированием, что объясняет, как адреналин ингибирует синтез гликогена, одновременно стимулируя его распад.
До сих пор не упоминалось, что рецепторы некоторых первых мессенджеров при активации ингибируют аденилатциклазу, что приводит к уменьшению выработки цАМФ. Это происходит потому, что данные рецепторы связаны с другим G-белком — Gi (индекс «i» обозначает ингибирующий). Активация Gi вызывает ингибирование аденилатциклазы, снижая концентрацию цАМФ в клетках и, таким образом, уменьшая фосфорилирование ключевых белков. Многие клетки экспрессируют как стимулирующие (Gs), так и ингибирующие (Gi) G-белки в своих мембранах, что обеспечивает жесткую регуляцию внутриклеточной концентрации цАМФ. Эта общая черта подчеркивает принцип, согласно которому большинство физиологических функций контролируются множеством регуляторных систем, часто работающих в противоположных направлениях, что позволяет точно настраивать клеточные реакции. Наконец, как показано на рисунке 5.9, цАМФ-зависимая протеинкиназа может фосфорилировать определенные ионные каналы плазматической мембраны, заставляя их открываться или закрываться. Это непрямое управление ионными каналами с помощью G-белка использует путь вторичной передачи, отличный от прямого воздействия G-белка на ионный канал. В таблице 5.2 приведены три способа, с помощью которых активация рецептора приводит к открытию или закрытию ионных каналов, вызывая изменения мембранного потенциала.

Фосфолипаза С, диацилглицерин и инозитолтрисфосфатный путь. В этой системе G-белок, называемый Gq, активируется рецептором, связанным с первым мессенджером. Активированный Gq затем активирует эффекторный фермент плазматической мембраны — фосфолипазу С. Данный фермент катализирует расщепление фосфолипида плазматической мембраны, известного как фосфатидилинозитолбисфосфат (PIP₂), на диацилглицерин (DAG) и инозитолтрисфосфат (IP₃) (рис. 5.10). И DAG, и IP₃ затем функционируют как вторые мессенджеры, но совершенно по-разному.
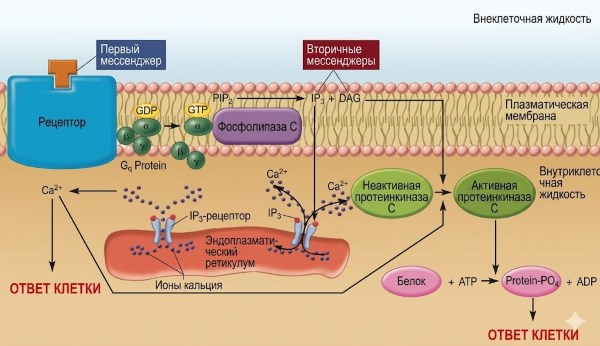
Рисунок 5.10. Механизм, с помощью которого активированный рецептор стимулирует ферментативно опосредованное расщепление PIP₂ с образованием IP₃ и DAG. Затем IP₃ связывается с рецептором на эндоплазматическом ретикулуме. Этот рецептор представляет собой управляемый лигандом ионный канал, который, будучи открытым, обеспечивает высвобождение Ca²⁺ из эндоплазматического ретикулума в цитозоль. Вместе с DAG Ca²⁺ активирует протеинкиназу С.
DAG активирует представителей семейства родственных протеинкиназ, известных под общим названием протеинкиназа С, которая, подобно цАМФ-зависимой протеинкиназе, затем фосфорилирует большое число других белков, приводя к ответной реакции клетки. IP₃, напротив, не выполняет функцию вторичного мессенджера путем прямой активации протеинкиназы. Вместо этого цитозольный IP₃ связывается с рецепторами, расположенными в эндоплазматическом ретикулуме; данные рецепторы представляют собой управляемые лигандом Ca²⁺-каналы, которые открываются при связывании с IP₃. Поскольку концентрация Ca²⁺ в эндоплазматическом ретикулуме намного выше, чем в цитозоле, Ca²⁺ диффундирует из этой органеллы в цитозоль, значительно увеличивая цитозольную концентрацию Ca²⁺. Эта повышенная концентрация Ca²⁺ затем продолжает последовательность событий, приводящих к реакции клетки на первый сигнал. Примечательно, что одним из действий Ca²⁺ является активация некоторых форм протеинкиназы С (отсюда название «С» — кальций).
Ион кальция в качестве вторичного посредника. Ион кальция (Ca²⁺) выполняет функцию вторичного посредника в большом разнообразии клеточных реакций как на химические, так и на электрические раздражители. Физиология Ca²⁺ как вторичного посредника требует анализа двух общих вопросов: (1) как стимулы приводят к увеличению цитозольной концентрации Ca²⁺? (2) как повышенная концентрация Ca²⁺ вызывает реакцию клеток? С помощью активных транспортных систем в плазматической мембране и мембранах определенных клеточных органелл концентрация Ca²⁺ в цитозоле поддерживается на чрезвычайно низком уровне. Следовательно, всегда существует большой электрохимический градиент, благоприятствующий диффузии Ca²⁺ в цитозоль по Ca²⁺-каналам, расположенным как в плазматической мембране, так и в эндоплазматическом ретикулуме. Стимул может изменить это устойчивое состояние, воздействуя на системы активного транспорта и/или ионные каналы, что приводит к изменению концентрации Ca²⁺ в цитозоле. Наиболее распространенные способы, с помощью которых активация рецепторов увеличивает Ca²⁺ в цитозоле, приведены в верхней части таблицы 5.3.

Теперь обратимся к тому, как повышенная концентрация Ca²⁺ в цитозоле вызывает клеточные реакции (см. нижнюю часть таблицы 5.3). Общим знаменателем действия Ca²⁺ является его способность связываться с различными цитозольными белками, изменяя их конформацию и тем самым активируя их функцию. Одним из наиболее важных таких белков, присутствующих во всех клетках, является кальмодулин (рис. 5.11). При связывании с Ca²⁺ кальмодулин изменяет форму, позволяя Ca²⁺-кальмодулину активировать или ингибировать большое разнообразие ферментов и других белков, многие из которых являются протеинкиназами. Активация или ингибирование этих кальмодулин-зависимых протеинкиназ приводит посредством фосфорилирования к активации или ингибированию белков, участвующих в конечных реакциях клетки на первый мессенджер. Однако кальмодулин — не единственный внутриклеточный белок, на который влияет связывание Ca²⁺. Например, в мышцах определенных типов Ca²⁺ связывается с белком тропонином и инициирует сокращение. Для справки в таблице 5.4 приведены данные о производстве и функциях основных вторичных посредников, описанных в этой главе.
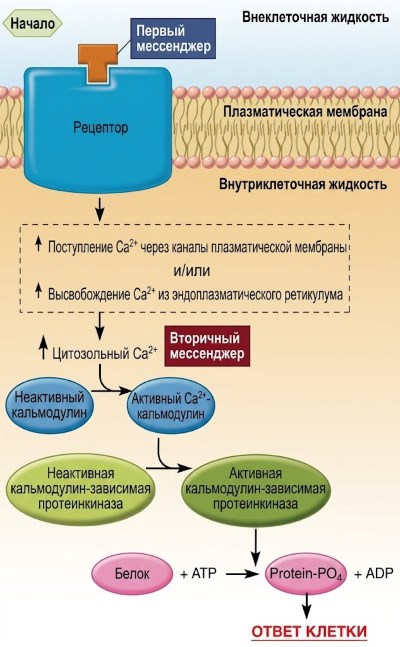
Рисунок 5.11. Ca²⁺, кальмодулин и кальмодулинзависимая протеинкиназная система. Существует множество кальмодулинзависимых протеинкиназ. В таблице 5.3 приведены механизмы повышения цитозольной концентрации Ca²⁺.

Другие переносчики: эйкозаноиды. В нескольких местах данного текста упоминаются переносчики, которые не так легко классифицировать, как описанные выше. Среди них — эйкозаноиды. Эйкозаноиды представляют собой семейство молекул, получаемых из полиненасыщенной жирной кислоты арахидоновой кислоты, которая присутствует в фосфолипидах плазматической мембраны. К эйкозаноидам относятся циклические эндопероксиды, простагландины, тромбоксаны и лейкотриены (рис. 5.12). Они вырабатываются во многих типах клеток в ответ на различные внеклеточные сигналы, включая факторы роста, молекулы иммунной защиты и даже другие эйкозаноиды. Таким образом, эйкозаноиды могут действовать как внеклеточные, так и внутриклеточные мессенджеры в зависимости от типа клеток.
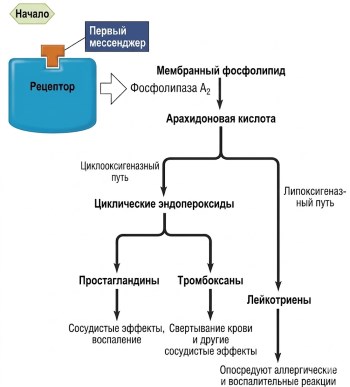
Рисунок 5.12. Пути синтеза эйкозаноидов и некоторые из их основных функций. Фосфолипаза А₂ — это фермент, участвующий в образовании всех эйкозаноидов; это место, где действуют раздражители. Противовоспалительные стероиды ингибируют фосфолипазу А₂. Действие циклооксигеназы ингибируется аспирином и другими нестероидными противовоспалительными препаратами (НПВП). Существуют также препараты, которые ингибируют фермент липоксигеназу, блокируя образование лейкотриенов. Эти препараты могут быть полезны в борьбе с астмой, при которой избыток лейкотриенов связан с аллергическими и воспалительными компонентами заболевания.
Синтез эйкозаноидов начинается, когда соответствующий стимул (гормон, нейромедиатор, паракринное вещество, лекарственное средство или токсический агент) связывает свой рецептор и активирует фосфолипазу А₂ — фермент, локализованный на плазматической мембране стимулируемой клетки. Как показано на рисунке 5.12, этот фермент отщепляет арахидоновую кислоту от мембранных фосфолипидов. Затем арахидоновая кислота может метаболизироваться двумя путями: один инициируется ферментом циклооксигеназой (ЦОГ), что приводит к образованию циклических эндопероксидов, простагландинов и тромбоксанов; другой инициируется ферментом липоксигеназой, приводя к образованию лейкотриенов. В обоих путях синтез специфических эйкозаноидов опосредован ферментами, поэтому ферменты эйкозаноидного пути, экспрессирующиеся в конкретной клетке, определяют, какие эйкозаноиды синтезирует клетка.
Каждое крупное подразделение эйкозаноидов содержит более одного представителя. На основе структурных различий молекулы внутри каждого подразделения обозначаются буквой — например, PGA и PGE для простагландинов типов A и E, — которые затем могут быть разделены на дополнительные группы (например, PGE₂). После синтеза эйкозаноиды могут в некоторых случаях действовать как внутриклеточные посредники, но чаще всего они высвобождаются немедленно и действуют локально. По этой причине эйкозаноиды обычно подразделяют на паракринные и аутокринные вещества. После того как они подействуют, они быстро метаболизируются местными ферментами до неактивных форм. Эйкозаноиды оказывают широкий спектр эффектов, особенно на кровеносные сосуды и при воспалении, многие из которых будут описаны в следующих главах.
Некоторые лекарственные препараты влияют на эйкозаноидный обмен и являются одними из наиболее широко используемых во всем мире. Например, аспирин ингибирует циклооксигеназу и, следовательно, блокирует синтез эндопероксидов, простагландинов и тромбоксанов. Аспирин и другие препараты, блокирующие циклооксигеназу, в совокупности называются нестероидными противовоспалительными средствами (НПВП). Их основное применение — уменьшение боли, лихорадки и воспаления. Термин «нестероидные» отличает их от синтетических глюкокортикоидов (аналогов стероидных гормонов, вырабатываемых надпочечниками), используемых в больших дозах в качестве противовоспалительных препаратов; эти стероиды ингибируют фосфолипазу А₂ и, следовательно, блокируют выработку всех эйкозаноидов.
Прекращение активности в путях передачи сигнала. После запуска пути передачи сигнала в конечном итоге отключаются, чтобы предотвратить хроническую чрезмерную стимуляцию клетки, которая может быть вредной. Ключевым событием обычно является прекращение активации рецептора. Реакция на сигналы — это преходящие явления, которые сохраняются лишь короткое время и исчезают, когда рецептор больше не связан с первым сигналом. Основным способом прекращения активации рецептора является снижение концентрации молекул первого мессенджера в области рецептора, что происходит по мере того, как ферменты метаболизируют первый мессенджер, когда первый мессенджер поглощается соседними клетками или когда он просто рассеивается.
Кроме того, рецепторы могут быть инактивированы по крайней мере тремя другими способами: (1) рецептор подвергается химическому изменению (обычно путем фосфорилирования), что может снизить его сродство к первому связующему веществу, вызывая высвобождение связующего вещества; (2) фосфорилирование рецептора может предотвратить дальнейшее связывание G-белка с рецептором; (3) рецепторы плазматической мембраны могут быть удалены, когда комбинация первого мессенджера и рецептора попадает в клетку путем эндоцитоза. Данные процессы контролируются физиологически. Например, во многих случаях ингибирующее фосфорилирование рецептора опосредуется протеинкиназой, которая первоначально активировалась в ответ на первый мессенджер, образуя отрицательную обратную связь.
На этом мы завершаем описание основных принципов работы путей передачи сигнала. Важно понимать, что эти пути не существуют изолированно, а могут быть активны одновременно в одной клетке, подвергаясь сложным взаимодействиям. Это возможно потому, что один первый посредник может вызвать изменения более чем в одном пути, и, что немаловажно, множество различных первых посредников могут одновременно влиять на клетку. Более того, на одном или нескольких уровнях между различными путями передачи сигнала могут возникать значительные «перекрестные помехи». Например, активные молекулы, генерируемые в пути цАМФ, могут изменять активность рецепторов и сигнальных молекул, генерируемых другими путями.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 125;











