Принцип жестких и мягких кислот и оснований (принцип ЖМКО)
Принцип, разработанный Пирсоном, по сути является обоснованием кислотно-основного взаимодействия на основе учета химического состава и электронного строения вещества, а также сравнительной устойчивости образуемых ими комплексов кислота-основание:
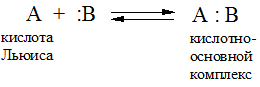
Данный принцип постулирует, что «жесткие» кислоты предпочтительно реагируют с «жесткими» основаниями, а «мягкие» кислоты – с «мягкими» основаниями.
«Жесткие» кислоты – это акцепторы, характеризующиеся низкой поляризуемостью, высокой электроотрицательностью и низкой энергией свободных граничных орбиталей; трудно восстанавливаются (H+; Li+; Na+; K+; RCO+; CO2)
«Жесткие» основания – это доноры, характеризующиеся низкой поляризуемостью, высокой электроотрицательностью и низкой энергией занятых граничных орбиталей; трудно окисляются (H2O; OH- ; F- ; R-OH; RO- ; R-O-R; R-NH2; RCOO- )
«Мягкие» кислоты – акцепторы с высокой поляризуемостью, низкой электроотрицательностью, легко восстанавливаются, а их свободные граничные орбитали характеризуются высокой энергией (CH3Hg + ; Cu+; Ag+; R+ ; RO+ ; RHal)
«Мягкие» основания– доноры с высокой поляризуемостью, низкой электроотрицательностью и легко окисляются, а их занятые граничные орбитали имеют высокую энергию ( H– ; I–; CN–; CO; R2S; R–; C2H4; C6H6)
С учетом такого подхода к понятиям кислота и основание, можно, например, прогнозировать возможное смещение равновесия реакции между метанолом и иодоводородом в газовой фазе:

Метанол и метилйодид следует рассматривать как продукты взаимодействия мягкой кислоты - +CH3 с основаниями: в одном случае жестким – OH¯; во втором мягким – I¯. Тогда согласно принципу взаимодействия «мягкий – мягкий» и «жесткий – жесткий» равновесие будет сдвинуто вправо:

Дата добавления: 2020-10-01; просмотров: 660;











