На основе природы реагирующих частиц
Радикальные (гомолитические) реакции. Подобные реакции протекают с участием радикалов –частиц, характеризующихся наличием неспаренного электрона.Если молекулу атакует радикал, то происходит гомолитический разрыв ковалентной связи в молекуле с образованием новых радикалов. Исходный же радикал взаимодействует с одной из образовавшихся частиц:
В общем виде:
Например:
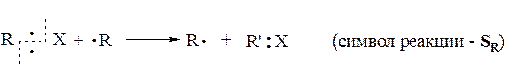
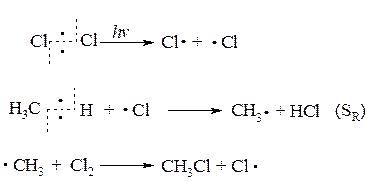
Электрофильные реакции.Данный тип реакций протекает с участием электрофильных реагентов, которые атакуют положение с повышенной электронной плотностью в субстрате. Если молекула атакуется электрофильной частицей, то происходит гетеролитическое расщепление связи в субстрате, и замещаемая частица (атом или группа атомов) уходит в виде положительного иона.
В общем виде:
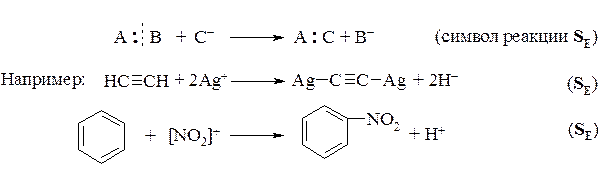
Нуклеофильные реакции.В этих процессах участвуют нуклеофильные реагенты, которые атакуют положение с пониженной электронной плотностью в субстрате. Здесь также происходит гетеролитический разрыв связи, но замещаемая частица отщепляется в виде аниона.
В общем виде:
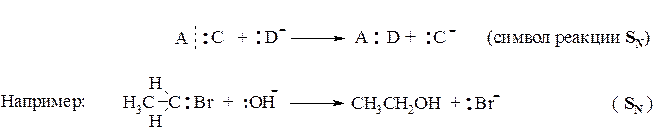
Электрофильные и нуклеофильные реакции объединяют как гетеролитические реакции.
В органических реакциях атом углерода способен образовывать ионы, заряд которых зависит от того, у какой из частиц остается электронная пара при разрыве связи:
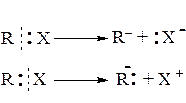
При потере атомом углерода электрона образуется положительно заряженная частица – карбкатион.
Если при разрыве связи общая электронная пара остается у атома углерода, то образующаяся частица приобретает отрицательный заряд и называется карбанионом.
 Метильный радикал– •CH3 образуется при гомолитическом (симметричном) разрыве связи C-H в метане. Атом углерода здесь находится в состоянии sp2 – гибридизации, поэтому геометрия – тригональная. Неспаренный электрон расположен на «чистой» негибридизованной р-орбитали:
Метильный радикал– •CH3 образуется при гомолитическом (симметричном) разрыве связи C-H в метане. Атом углерода здесь находится в состоянии sp2 – гибридизации, поэтому геометрия – тригональная. Неспаренный электрон расположен на «чистой» негибридизованной р-орбитали:
 Карбкатион – положительно заряженный органический ион, заряд которого локализован преимущественно на атоме углерода, находящегося в состоянии sp2 – гибридизации. Такой атом имеет три связи и вакантную р-орбиталь. Катион CH3+, например, характеризуется плоской тригональной геометрией:
Карбкатион – положительно заряженный органический ион, заряд которого локализован преимущественно на атоме углерода, находящегося в состоянии sp2 – гибридизации. Такой атом имеет три связи и вакантную р-орбиталь. Катион CH3+, например, характеризуется плоской тригональной геометрией:

 Ион карбония – карбкатион, положительный заряд которого делокализован между несколькими фрагментами, окружающими карбкатионный центр.
Ион карбония – карбкатион, положительный заряд которого делокализован между несколькими фрагментами, окружающими карбкатионный центр.
Карбанионы – органические анионы, характеризующиеся четным числом электронов и преимущественной локализацией отрицательного заряда на атоме углерода. Теоретические расчеты указывают на пирамидальную геометрию карбанионного углеродного атома в метильном анионе. Если между карбанионным центром и связанным с ним заместителем имеет место сопряжение, то характерна плоская (тригональная) геометрия.
Дата добавления: 2020-10-01; просмотров: 595;











