Мономолекулярные реакции, в которые могут вступить радикалы
1. Напишите все мономолекулярные реакции, в которые могут вступить радикалы:
а)
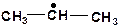
| б)
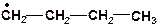
|
в)
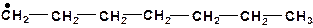
|
2. Напишите все возможные реакции замещения атома водорода с углеводородами. Какая из этих реакций пойдет наиболее легко? Наиболее трудно?
а)
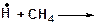
| в)
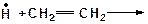
|
б)
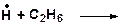
| г)
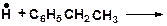
|
3. Напишите возможные реакции замещения и укажите наиболее вероятную из них:
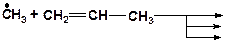
4. Напишите возможные реакции замещения и укажите наименее вероятную из них:
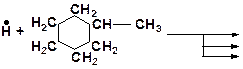
5. Напишите возможные реакции замещения и укажите наиболее вероятную из них:
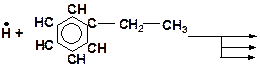
6. Напишите возможные реакции замещения и укажите наиболее вероятную из них:
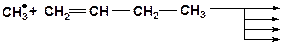
7. Напишите возможные реакции замещения и укажите наиболее вероятную из них:
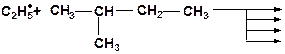
8. Напишите возможные реакции замещения и расположите в порядке возрастания трудности их осуществления:
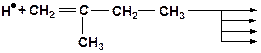
9. Напишите возможные варианты распада радикала. Какое направление распада наиболее вероятно?
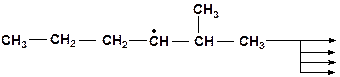
10. Напищите возможные варианты распада радикала. Какое направление распада наиболее вероятно?
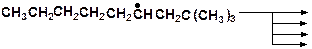
11. Какие радикалы могут образовываться при взаимодействии. Укажите возможные направления распада образующихся радикалов.
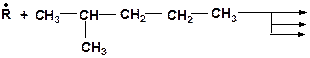
12. Какие радикалы могут образоваться при взаимодействии:
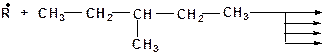
13. Какие радикалы могут образовываться при взаимодействии:
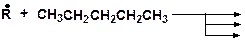
14. Напишите возможные реакции в системе:
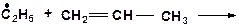
15. Напишите моно- и бимолекулярные реакции, которые могут протекать в системах:
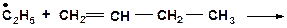
|
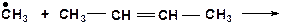
|
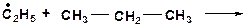
|
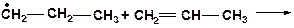
|
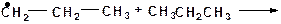
|
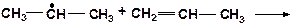
|
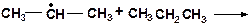
|
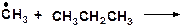
|
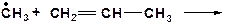
|
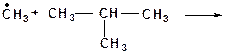
|
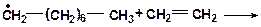
|
6.3 Карбоний ионный механизм термокаталитических
процессов переработки нефтяного сырья
Химизм превращения углеводородов в процессе каталитического крекинга углеводородов и основные реакции процесса каталитического крекинга подробно рассмотрены в разделе 3.1.4.
Основные стадии цепного карбкатионного механизма каталитического крекинга и реакции, в которые вступают карбкатионы, приведены в разделе 3.1.5.
Химические превращения углеводородов крекируемого сырья, протекающие по карбкатионному механизму на поверхности цеолитсодержащего катализатора, могут быть представлены в следующей последовательности [2]:
1. Первичные мономолекулярные реакции крекинга и деалкилирования (распад по С–С-связи) высокомолекулярных соединений исходного сырья с образованием низкомолекулярных углеводородов:
- крекинг парафинов с образованием низкомолекулярного парафина и олефина;
- крекинг олефинов с образованием низкомолекулярных олефинов;
- деалкилирование алкилароматических углеводородов;
- крекинг нафтенов с образованием олефинов.
2. Вторичные бимолекулярные реакции углеводородов на поверхности цеолита с участием карбоний ионов, образующихся присоединением протона к олефину (инициирование цепи). Стабильность карбкатионов возрастает в ряду:
СН3+ < С2Н5+ < С+перв. < С+втор. < С+трет.
Третичный карбкатион является самым стабильным, этим объясняется высокий выход изопарафиновых углеводородов, особенно изобутана.
Наиболее характерные реакции карбониевых ионов (развитие цепи): распад С–С-связи, перенос гидрид-иона (Н-перенос), изомеризация, циклизация, дециклизация, деалкилирование, алкилирование, полимеризация, поликонденсация и др.
Обрыв цепи превращений карбониевых ионов происходит возвратом протона к поверхности катализатора или отнятием электрона от центров Льюиса.
Распад С–С-связи карбкатиона – наиболее важная целевая реакция, приводящая к образованию низкомолекулярных топливных фракций и С3-С4 углеводородовв газах каталитического крекинга.
Правила распада С–С-связи карбкатиона:
- легче разрывается С–С-связь, находящаяся в b-положении по отношению к атому углерода, несущему заряд (правило
b-распада); - образующиеся олефины содержат двойную связь у первого углеродного атома;
- наиболее вероятен b-распад карбкатиона с образованием олефина с меньшей длиной цепи. Продукт первичного b-распада – карбоний-ион RCH2+ – может снова крекироваться до образования более стабильных карбкатионов или углеводородов (после отдачи протона или присоединения электрона);
- более выгодным для алкилароматических или алкилнафтеновых углеводородов является отрыв всей алкильной группы;
- поскольку образование СН3+ и С2Н5+ требует высоких энергетических затрат, цепной распад карбкатионов прерывается до образования карбониевых ионов с числом углеродных атомов 3-5.
Перенос гидрид-иона (Н-перенос) протекает следующим образом:
R¢H + +R² ® +R¢ + R²H
Лучшими гидрид-донорами являются нафтены, полициклические нафтены или нафтено-ароматические углеводороды, изоалканы и олефины. Энергетически более выгоден отрыв гидрид-иона от третичного, затем вторичного и менее выгоден от первичного углеродного атома. Нафтеновые, алкилароматические и изопарафиновые углеводороды часто содержат третичные атомы углерода и поэтому интенсивно участвуют в реакциях Н-переноса. Акцепторами гидрид-ионов являются наименее стабильные карбоний ионы или углеводороды, содержащие несколько p-связей (диолефины). Именно Н-перенос обусловливает повышенные выход топливных фракций и химическую стабильность бензинов каталитического крекинга.
По Н-переносу осуществляются следующие реакции каталитического крекинга:
олефин + нафтен ® парафин + арен;
олефин + парафин ® парафин + олефин;
олефин + олефин ® арен + парафин;
олефин + олефин ® арен + водород;
арен + арен ® кокс + парафин + водород.
Изомеризация карбониевых ионов является также важной целевой реакцией. Изомеризация протекает быстрее чем крекинг, часто предшествует b-распаду. Сочетание реакций изомеризации и b-распада обусловливает повышенное содержание в продуктах каталитического крекинга углеводородов изостроения. Изомеризация карбониевых ионов может происходить либо путем передачи протона (гидридный сдвиг) или метильной группы (скелетная изомеризация) вдоль углеводородной цепи.
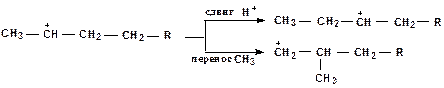
Реакции циклизации и дециклизации с участием карбоний ионов протекают через мультиплетную хемосорбцию:
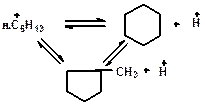
или через диеновый синтез:
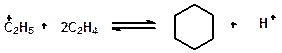
Циклопентаны в условиях каталитического крекинга более устойчивы, чем циклогексаны. Циклогексаны подвергаются дегидрированию в арены посредством Н-переноса. При наличии длинных боковых цепей в циклоалкановом карбониевом ионе возможны изомеризация боковой цепи и деалкилирование. Бициклические циклоалкановые карбониевые ионы ароматизируются в большей степени, чем моноциклические.
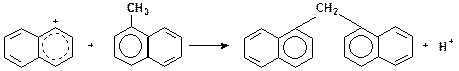
Реакции конденсации ароматических углеводородов, дающие соединения с более высокой молекулярной массой, вплоть до кокса, характерны для каталитического крекинга. Ареновый карбкатион вступает в последовательные реакции присоединения (конденсации) к ароматическим углеводородам и Н-переноса. Процесс конденсации вследствие высокой стабильности полициклического аренового карбоний иона продолжается до обрыва цепи:
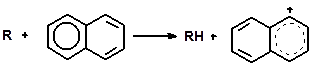
14. Напишите реакции деалкилирования и разложите их в порядке возрастания трудности их осуществления:
а)
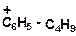
|
б)
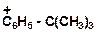
|
в)
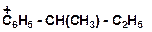
|
г)
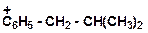
|
15. Напишите механизм реакции перераспределения метильных групп:
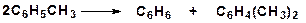
16. Напишите механизм распада дифенилэтана:
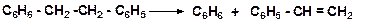
Дата добавления: 2020-08-31; просмотров: 1311;











