Порядок выполнения работы
Для проведения работы необходимы:
Ø установка для измерения поверхностного натяжения;
Ø бюретки;
Ø конические колбы емкостью 50 мл;
Ø воронки и фильтровальная бумага;
Ø 0,2 М растворы пропилового, бутилового и пентилового спиртов.
Готовят 5 водных растворов пропилового, бутилового и пентилового спиртов разбавлением исходных растворов водой в соответствии с данными:
| Объем исходного раствора спирта, мл | 25,000 | 19,000 | 12,500 | 6,300 | 3,200 |
| Объем добавляемой воды, мл | 0,000 | 6,000 | 12,500 | 18,700 | 21,800 |
| Концентрация раствора с, моль/л | 0,200 | 0,150 | 0,100 | 0,050 | 0,025 |
С помощью установки, указанной преподавателем, определяют поверхностное натяжение приготовленных растворов (методику измерений см. в работах 5 и 6 по физической химии). Измерение поверхностного натяжения следует проводить быстро, так как может происходить испарение спирта с поверхности раздела фаз.
По полученным данным для каждого спирта строят изотермы поверхностного натяжения и по ним находят поверхностную активность 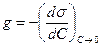 , а также значения ds/dc в нескольких точках изотерм. По уравнению (3.8) вычисляют значения Г и строят изотермы адсорбции Г = f(c). Данные расчета g, ds/dc и Г для исследуемых спиртов записывают в таблицу (см. табл. 3. 2).
, а также значения ds/dc в нескольких точках изотерм. По уравнению (3.8) вычисляют значения Г и строят изотермы адсорбции Г = f(c). Данные расчета g, ds/dc и Г для исследуемых спиртов записывают в таблицу (см. табл. 3. 2).
Таблица 3. 2 – Экспериментальные и расчетные данные по адсорбции алифатических спиртов
| Концентрация раствора спирта, моль/л | Наибольшее давление пузырька DР или сила отрыва кольца F | Поверхностное натяжение sж–г, Дж/м2 | 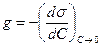
| 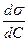
| Г, моль/м2 |
Затем рассчитывают соотношение поверхностных активностей для соседних гомологов:
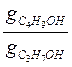 и
и 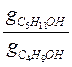
По изотермам Г = f(c) определяют значения Гмакс. и, приняв, что для ПАВ Гмакс » А¥, по уравнениям (3.23) и (3.24) рассчитывают s0 и d.
Полученные значения сравнивают с табличными и делают вывод об ориентации молекул ПАВ в насыщенном адсорбционном слое.
Работа 20 «Определение удельной поверхности адсорбентов методом газовой хроматографии»
Цель работы: определение удельной поверхности адсорбента по удерживаемому объему; определение удельной поверхности адсорбента методом тепловой десорбции (БЭТ).
Краткая теория.Газовая хроматография используется для решения таких физико-химических задач, как определение коэффициентов распределения и активности, термодинамических функций распределения и адсорбции. Этот метод применяется также для определения удельной поверхности адсорбентов, катализаторов, наполнителей.
Наибольшее распространение для оценки Sуд получили следующие хроматографические методы:
Ø метод, основанный на установлении изотермы адсорбции по параметрам хроматографического пика;
Ø фронтальный метод, по которому величина адсорбции рассчитывается по площади, заключенной между концентрационными фронтами адсорбата и несорбирующегося газа;
Ø метод тепловой десорбции, в котором количество сорбирующегося вещества находится по количеству адсорбата, поступившему при нагревании из адсорбента в поток газа-носителя.
На рисунке 3.2 приведена принципиальная схема газового хроматографа.
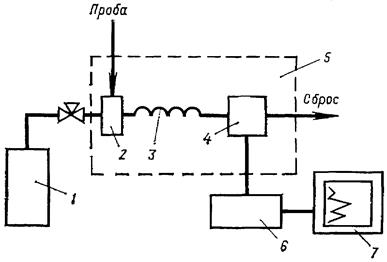
рисунок 3.2 – Блок-схема газового хроматографа:
1 – баллон с газом-носителем; 2 – дозатор-испаритель; 3 – хроматографическая колонка; 4 – детектор; 5 – термостат; 6 – электронный усилитель; 7 – самопишущий потенциометр.
Газ-носитель из баллона 1 под давлением поступает в дозатор 2 (дозатор-испаритель служит для ввода пробы в поток газа-носителя) и последовательно проходит хроматографическую колонку 3 и детектор 4. Сигнал детектора усиливается (блок 6) и подается на потенциометр 7. Для испарения жидкой или, что реже, твердой пробы, в дозаторе поддерживается необходимая температура.
Хроматографическая колонка представляет собой металлическую или стеклянную трубку, заполненную насадкой (адсорбентом). Детектор предназначен для определения содержания компонентов в потоке газа-носителя. Работа детекторов основана на измерении одного из физических параметров компонента (теплопроводность, потенциал ионизации, плотность и др.).
Из детектора через усилитель сигнал поступает в самопишущий потенциометр, который выписывает хроматограмму – графическое изображение зависимости выходного сигнала детектора от времени или объема газа-носителя (рисунок 3.3).
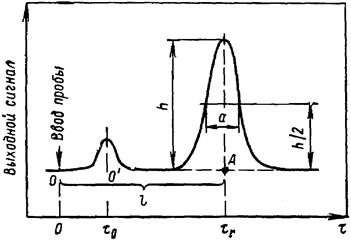
рисунок 3.3 – Хроматограмма и ее основные параметры.
На хроматограмме точка О соответствует моменту ввода пробы в колонку. Вещество, не адсорбируемое в колонке, выходит через время t0 (на хроматограмме – точка О¢). Время удерживания такого компонента называется «мертвым» временем удерживания. Оно пропорционально свободному объему хроматографической колонки v0 и обратно пропорционально объемной скорости газа-носителя U:
t0 = v0 / U (3.25)
Время, прошедшее от момента ввода пробы до появления максимума пика, называется временем удерживания компонента tr. При постоянной скорости движения диаграммной ленты самописца время удерживания удобно выражать расстоянием l, пройденным пером самописца от точки О до А. Объем газа-носителя, прошедшего через хроматографическую колонку за время tr, называется удерживаемым объемом Vr. Поскольку удерживаемый объем зависит не только от природы адсорбента и адсорбата, но и от свободного объема колонки, то вводят понятие приведенного удерживаемого объема V'r:
V'r = Vr – V0 = U(tr – t0) (3.26)
Скорость газа-носителя обычно экспериментально определяют при комнатной температуре и атмосферном давлении, поэтому в приведенный объем вводят поправку, учитывающую условия работы хроматографической колонки. Рассчитанный таким образом удерживаемый объем называется исправленным удерживаемым объемом Vu:
Vu = j . V'r (3.27)
где j – поправочный коэффициент, учитывающий сжимаемость газа и отличие условий хроматографирования от условий внешней среды.
Величину, полученную как отношение Vu к массе адсорбента m, находящегося в хроматографической колонке, называют удельным удерживаемым объемом:
Vm = Vu/m (3.28)
В практической работе используется еще ряд характеристик, таких, как относительный удерживаемый объем, коэффициенты разделения и селективности, и т. д.
Для количественной обработки хроматограмм можно использовать либо высоту пика, пропорциональную концентрации вещества, либо площадь пика, пропорциональную абсолютному содержанию компонента в газовой смеси. Чаще определяют площадь пиков, используя один из следующих методов: планиметрию, вырезание и взвешивание пиков, расчет площади как произведение основания пика а на половину высоты – или же с помощью электронных, аналоговых или механических интеграторов. Количество анализируемых компонентов по площади пиков можно определить, пользуясь калибровочной кривой (метод абсолютной калибровки), или при помощи вводимого стандарта (метод внутренней нормализации).
Наиболее простым из хроматографических методов определения удельной поверхности является метод, основанный на измерении удерживаемых объемов. Для двух образцов 1 и 2 адсорбента одной и той же природы, но с различной удельной поверхностью можно записать:
Vm1 = ВSуд 1. exp (Q/RT) (3.29)
Vm2 = ВSуд 2. exp (Q/RT) (3.30)
где Vm1 и Vm2 – удельные удерживаемые объемы, рассчитанные по уравнению (3.28);
В – постоянная при данной температуре, зависящая от изменения энтропии адсорбата при адсорбции;
Sуд 1 и Sуд 2 – удельная поверхность адсорбентов;
Q – теплота адсорбции.
Если удерживаемые объемы измерять при одной температуре, то
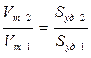 или
или 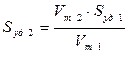 (3.31)
(3.31)
Из уравнения (11.31) следует, что, вычислив Vm1 и Vm2 по уравнениям (3.26) и (3.28) для двух образцов адсорбента и зная удельную поверхность одного из них Sуд1, можно рассчитать удельную поверхность второго сорбента.
Рассмотренный сравнительный метод применим для адсорбентов одной природы и требует знания удельной поверхности для одного из образцов. Этих недостатков лишен метод тепловой десорбции. Согласно этому методу по изменению состава газового потока (гелий с добавкой азота), проходящего через хроматографическую колонку с исследуемым адсорбентом, определяют количество азота, адсорбированного из газовой смеси при охлаждении адсорбента жидким азотом и десорбированного с него при последующем нагревании его до комнатной температуры. Изменяя концентрацию азота в газовой смеси, можно установить количество адсорбированного газа при различных концентрациях азота в исходной газовой смеси и, следовательно, построить изотерму адсорбции и вычислить по ней, используя линейную форму уравнения БЭТ, предельную емкость монослоя и соответствующую ей удельную поверхность адсорбента.
Дата добавления: 2020-07-18; просмотров: 787;











