ЭДС окислительно-восстановительных реакций
Энергия Гиббса и ЭДС реакции связаны уравнением:
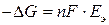 , где
, где
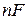 – количество электричества, прошедшее через элемент;
– количество электричества, прошедшее через элемент;
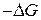 – уменьшение свойств энергии Гиббса;
– уменьшение свойств энергии Гиббса;
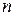 – количество электронов перемещающихся от восстановителя к окислителю;
– количество электронов перемещающихся от восстановителя к окислителю;
 – постоянная Фарадея;
– постоянная Фарадея;
Знак «–» перед 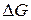 свидетельствует о возможности протекания реакции.
свидетельствует о возможности протекания реакции.
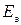 – ЭДС.
– ЭДС.
Зная окислительно-восстановительные потенциалы, можем определить ЭДС:
 .
.
Окислительно-восстановительная реакция возможна, когда электродвижущая сила реакции является положительной величиной: в этом случае изменение свободной энергии 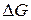 сохраняет отрицательный знак, т. е. общий запас энергии в системе уменьшается. Чем меньше окислительно-восстановительный потенциал пары, тем больше восстановительная способность вещества или иона (восстановителя). Чем больше окислительно-восстановительный потенциал, тем больше окислительная способность вещества или иона (окислителя) в данной паре.
сохраняет отрицательный знак, т. е. общий запас энергии в системе уменьшается. Чем меньше окислительно-восстановительный потенциал пары, тем больше восстановительная способность вещества или иона (восстановителя). Чем больше окислительно-восстановительный потенциал, тем больше окислительная способность вещества или иона (окислителя) в данной паре.
Окислительно-восстановительные реакции идут в сторону образования более слабых окислителей и восстановителей.
Из всех возможных при данных условиях окислительно-восстановительных реакций в первую очередь протекает та, которая имеет наибольшую разность окислительно-восстановительных потенциалов.
Кинетика электродных процессов. Равновесные потенциалы могут быть определены в условиях отсутствия в цепи тока. При прохождении электрического тока потенциалы электродов изменяются.
Изменение потенциала электрода при прохождении электрического тока, называется поляризацией:
 , где
, где
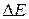 – поляризация;
– поляризация; 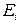 – потенциал электрода при прохождении электрического тока;
– потенциал электрода при прохождении электрического тока; 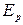 – равновесный потенциал.
– равновесный потенциал.
Поляризация может наблюдаться как на катоде, так и на аноде, поэтому различают катодную и анодную поляризации 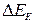 и
и 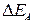 .
.
Изменение потенциала при прохождении тока также называется перенапряжением.
Поляризация электрода в отрицательную сторону связана с протеканием процесса восстановления (катодная поляризация), а в положительную сторону – с протеканием процесса окисления (анодная).
Для электролиза аналогично: при прохождении электрического тока изменяются потенциалы электродов электролизера, то есть возникает электродная поляризация. Вследствие катодной поляризации потенциал катода становится более отрицательным, а из-за анодной поляризации потенциал анода становится более положительным. Поэтому разность потенциалов при прохождении электрического тока  при электролизе больше, чем разность равновесных потенциалов электродов
при электролизе больше, чем разность равновесных потенциалов электродов
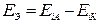 .
.
Поляризация электрода – необходимое условие протекания электродного процесса. Чем сильнее поляризован электрод, тем больше скорость соответствующей полуреакции.
Если речь идет о катодном выделении водорода, то поляризацию называют перенапряжением водорода. Перенапряжение выделения водорода на различных металлах различно.
Дата добавления: 2020-03-21; просмотров: 592;











