ТЕПЛОЁМКОСТЬ. УРАВНЕНИЕ КИРХГОФА.
Теплоёмкость– то количество теплоты, которое необходимо сообщить или отнять телу или системе, чтобы их температура изменилась на 1 градус. Теплоёмкость — величина экстенсивная, так как зависит от размера системы. Теплоёмкость,рассчитанная на 1 моль вещества, называется мольной, а на единицу массы – удельной.
Различают:
— истинную теплоёмкость: 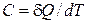 [
[ 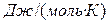 ]. (1.25)
]. (1.25)
— среднюю теплоёмкость: 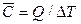 . (1.26)
. (1.26)
Наиболее часто используются следующие теплоемкости:
1. Изохорная теплоемкость. При нагреве или охлаждении вещества при постоянном объеме справедливо:
. 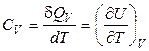 . (1.27)
. (1.27)
2. Изобарная теплоемкость. При нагреве или охлаждении вещества при постоянном давлении справедливо:
. 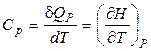 . (1.28)
. (1.28)
Следует знать, что теплоёмкость при постоянном давлении Ср больше, чем теплоёмкость при постоянном объёме СV, так как нагревание вещества при постоянном давлении сопровождается работой расширения, т.е.
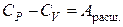 . (1.29)
. (1.29)
Для идеальных газов справедливо уравнение Майера:
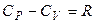 . (1.30)
. (1.30)
Величина R (универсальная газовая постоянная) равна работе расширения 1 моля идеального газа (при р = const) при увеличении его температуры на 1 градус.
Отношение 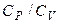 обозначается символом
обозначается символом 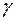 (адиабатический коэффициент), который всегда больше нуля (
(адиабатический коэффициент), который всегда больше нуля ( 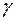 > 0).
> 0).
Зависимость теплоёмкости веществ в области не очень низких температур (Т ≥ 298 К) обычно выражается в виде следующих полиномов:
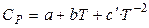 . (1.31)
. (1.31)
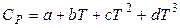 . (1.32)
. (1.32)
Значения a, b, c, c´, d приведены в справочниках физико-химических и термодинамических величин.
Рассмотрим уравнение Кирхгоффа, описывающее зависимость энтальпии реакции от температуры:
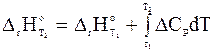 , (1.33)
, (1.33)
где
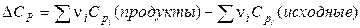 ,
,
т. е. разность между суммой теплоёмкостей продуктов реакции и исходных веществ с учётом стехиометрических коэффициентов.
Для вычисления интеграла необходимо знать зависимость теплоёмкости от температуры для всех веществ, что не всегда возможно. Поэтому уравнение Кирхгоффа применяют в трёх приближениях.
1. При наиболее грубом приближении полагают, что DСp = 0, т.е. считают равными суммарные теплоёмкости продуктов и исходных веществ. Тогда 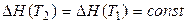 ,
,
т.е. тепловой эффект считается не зависящим от температуры. Этим приближением пользуются, если теплоемкости некоторых участников реакции неизвестны.
2. Во втором приближении считают разность теплоёмкостей постоянной величиной DСР = const. Тогда
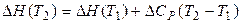 . (1.34)
. (1.34)
Это уравнение применяют только для небольшого интервала температур Т2 – Т1, в котором известны величины теплоёмкостей.
3. В наиболее точном приближении используют зависимость всех СРi от температуры. Если теплоемкости веществ даны в виде полиномов, например (1.34), то уравнение Кирхгоффа можно проинтегрировать, после чего оно будет иметь следующий вид:
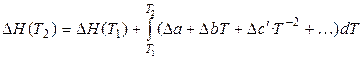 . (1.35)
. (1.35)
Последнее уравнение можно использовать только в том интервале температур Т2 – Т1, для которого определены коэффициенты ai, bi, ci температурной зависимости теплоёмкостей веществ.
ЛЕКЦИЯ 2
Второй закон термодинамики. Энтропия. Вычисление изменения энтропии для различных процессов. Постулат Планка. Энергия Гиббса и энергия Гельмгольца. Уравнение Гиббса-Гельмгольца. Самопроизвольное протекание химических реакций. Расчет изменения энергии Гиббса в химических реакциях. Химический потенциал. Активность и летучесть.
Дата добавления: 2016-06-18; просмотров: 3611;











