Розчинення газів у металі та шлаці
Кисень у металі найчастіше розчиняється внаслідок дисоціації оксидів заліза шлаку за реакцією:
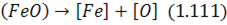
яка завжди відбувається в сталеплавильних процесах завдяки їх окислювальному характеру.
Складнішим є питання розчинення в металі азоту і водню.
У разі безпосереднього контакту газової фази з металом реакція їх розчинення в металевій ванні подається у вигляді рівнянь:
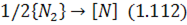
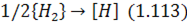
або в загальному вигляді:
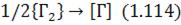
Із виразу для константи рівноваги реакції (1.114) урівноважений з газовою фазою вміст газу в металі:
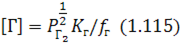
тобто пропорційний до парціального тиску газу в газовій фазі в степені 1/2. Цю залежність називають законом Сівертса.
Температура процесу неістотно впливає на константу рівноваги і розчинюваність газу в рідкому металі. Певною мірою на неї впливає коефіцієнт активності газу, особливо за наявності в металі підвищеного вмісту вуглецю, як це відбувається на початку плавки.
У той же час значне зменшення розчинності газів у металі відбувається під час переходу з рідкого стану в твердий.
Реакції (1.112 і 1.11З) відбуваються за етапами дисоціації та адсорбції на поверхні металу:
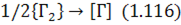
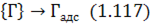
та переходу адсорбованих атомів газу до розчину:
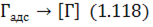
Найповільнішим із зазначених є етап (1.116), а етап (1.117) відповідає каталітичному впливу поверхні металу на дисоціацію молекул газів.
Поверхнево-активні кисень, сірка і вуглець, розчинені в металі, перешкоджають як переходу газів до металу, так і їх відокремленню з металу.
Газова фаза, що містить азот і водень, може контактувати зі шлаком, який знаходиться на поверхні металу. У цьому разі водень переходить до шлаку за реакцією:
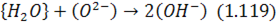
якщо шлак основний, або:
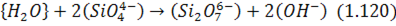
якщо кислий, створюючи аніон гідроксильної групи. Унаслідок цього вміст останньої в шлаці підвищується, шо порушує рівновагу перерозподілу водню між шлаком і металом реакції:
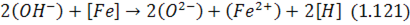
З аналізу рівнянь (1.119 – 1.121) випливає, що підвищення основності шлаку і збільшення вмісту аніонів кисню 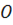 , в ньому сприяють зростанню розчинення водню в шлаці, що відповідно спричинює перехід водню до металу. Навпаки, підвищення окислюваності шлаку запобігає розчиненню водню в металі, хоча оксиди заліза, дисоціюючи в шлаці, підвищують вміст аніонів кисню.
, в ньому сприяють зростанню розчинення водню в шлаці, що відповідно спричинює перехід водню до металу. Навпаки, підвищення окислюваності шлаку запобігає розчиненню водню в металі, хоча оксиди заліза, дисоціюючи в шлаці, підвищують вміст аніонів кисню.
У практиці сталеплавильного виробництва кислі шлаки перешкоджають переходу газів з атмосфери агрегату до металу через шар. шлаку більшою мірою, а основні – меншою. Це є однією з небагатьох переваг кислих сталеплавильних процесів на відміну від основних.
Для шлаків будь-якого складу згідно з реакціями (1.119 і 1.120) вміст водню в шлаці і відповідно в металі пропорційний до парціального тиску водню в газовій атмосфері сталеплавильного агрегату в степені 1/2, тобто характер залежності такий самий, як і в разі безпосереднього контакту металу з газовою фазою.
Щодо переходу до шлаку азоту газової фази існують різні думки. Деякі дослідники вважають, що в основних шлаках може розчинятися до 0,002-0,008% азоту, а в кислих – 0,002-0,005%. Інші взагалі заперечують можливість розчинення азоту в окислювальних шлаках. Перші вважають, що азот розчиняється у вигляді аніонів 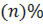 але реакції розчинення не наводять.
але реакції розчинення не наводять.
Із практики сталеплавильного виробництва відомо, що шлак надійно захищав метал від розчинення азоту на відміну від водню.
Газ із металу виділяється в зворотному напрямі, якщо парціальний тиск газу в газовій фазі зменшується порівняно з попереднім. Під час виплавки сталі це звичайно відбувається завдяки окисленню з металу вуглецю, оскільки газоподібні продукти реакції, що у вигляді бульбашок барботують через метал, мають при утворенні нульовий парціальний тиск азоту і водню, тобто не містять їх. Тому при спливанні бульбашок азот і водень з металу надходять до бульбашок, їх тиск поступово зростає, що зменшує швидкість надходження. У результаті з підвищенням швидкості окислення вуглецю прискорюється відокремлення з металу азоту і водню. Водночас якщо в газовій фазі агрегату містяться азот і водень з парціальним тиском, що перевищує рівновагу реакцій (1.112; 1.11З) або (1.119, 1.120), ці гази надходитимуть до металу так само, як наведено раніше.
Отже, одночасно відбуваються процеси надходження і відокремлення азоту і водню з металу, а їх вміст у металі залежить від співвідношення швидкостей цих процесів. Звичайно на початку плавки внаслідок розвинення і поступового зростання окислення вуглецю відокремлення азоту і водню з металу переважає, а вміст газів у металі зменшується. Такий стан триває майже 1/2-2/3 протягом усього процесу плавки. Після того як вміст вуглецю в металі набагато зменшується, настає момент, коли починає переважати процес надходження газів до металу. Чим довше триватиме такий стан, тим більше азоту і водню лишатиметься в металі після завершення процесу плавки.
У цих процесах особливе місце посідають технології, що передбачають вдування в метал окислювальних газів,і насамперед технічно чистого кисню. При виробництві кисню з повітря вміст залишків азоту повітря залежить від технології виробництва і становить 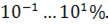 Оскільки при взаємодії кисню з металом у первинній реакційній зоні на поверхні контакту кисню з металом розвиваються температури приблизно 2500°C, процеси дисоціації азоту за реакцією (1.116) прискорюються, що сприяє збільшенню швидкості його розчинення в металі. Чим вищий вміст азоту в кисні, тим більша концентрація азоту в металі протягом усього процесу плавки і наприкінці їх.
Оскільки при взаємодії кисню з металом у первинній реакційній зоні на поверхні контакту кисню з металом розвиваються температури приблизно 2500°C, процеси дисоціації азоту за реакцією (1.116) прискорюються, що сприяє збільшенню швидкості його розчинення в металі. Чим вищий вміст азоту в кисні, тим більша концентрація азоту в металі протягом усього процесу плавки і наприкінці їх.
При вдуванні повітря концентрація азоту в метал підвищується завдяки його значному вмісту в повітрі.
Кожний газоподібний окислювач має певну вологість, що залежить від технології виробництва та його температури. Пари води є джерелом надходження водню до металу під час вдування окислювачів, що відбувається на поверхні контакту газу з металом. Тому перед використанням окислювальних газів їх осушують.
Гази з металів виділяють шляхом позапічної обробки сталі вакуумуванням. При цьому зменшується тиск азоту і водню, що призводить до порушення рівноваги реакцій (1.112, 1.11З) або (1.119, 1.120) та забезпечує виділення газів із сталі. Якщо при цьому до сталі вводяться нейтральні гази, які майже не містять азоту і водню, або відбувається окислення вуглецю з утворенням бульбашок газових продуктів, реакції окислення, виділення азоту і водню прискорюється як унаслідок розвинення поверхні виділення, так і внаслідок перемішування ванни, що прискорює масоперенос азоту і водню, розчинних у металі, до поверхні виділення.
Випарювання
Речовина переходить у паровий стан на поверхні розділу речовини з газовою фазою.
Якщо речовина знаходиться в твердому або рідинному розчині, то її випарювання визначається вмістом речовини в розчині.
Наприклад, марганець, розчинений у залізі сталеплавильної ванни, може випарюватись у газову фазу, що утворюється в самій ванні внаслідок окислення вуглецю при вдуванні у ванну окислювачів. У цьому разі реакцію випарювання можна записати у вигляді:
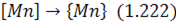
Згідно з виразом для константи рівноваги процесу парціальний тиск марганцю в газовій фазі визначається за виразом:
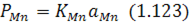
Оскільки константа рівноваги залежить від температури, 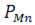 визначається температурою на поверхні, де відбувається випарювання марганцю. Випарювання супроводжується витратами теплоти, тому з підвищенням температури
визначається температурою на поверхні, де відбувається випарювання марганцю. Випарювання супроводжується витратами теплоти, тому з підвищенням температури 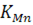 збільшуватиметься, що збільшить також парціальний тиск пари марганцю. Останній також визначається вмістом марганцю в металі через
збільшуватиметься, що збільшить також парціальний тиск пари марганцю. Останній також визначається вмістом марганцю в металі через 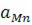 у рівнянні (1.123). Нарешті, взаємодія марганцю з іншими елементами, які входять у розчин заліза, що визначає коефіцієнт активності марганцю в залізі, також впливатиме на випарювання марганцю.
у рівнянні (1.123). Нарешті, взаємодія марганцю з іншими елементами, які входять у розчин заліза, що визначає коефіцієнт активності марганцю в залізі, також впливатиме на випарювання марганцю.
При відомому значенні 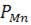 можна визначити концентрацію марганцю в газовій фазі як добуток парціального тиску марганцю на густину газової фази. Звичайно в розрахунках забрудненості газової фази пилом випарюваної речовини користуються її концентрацією (визначається в грамах або кілограмах на метр кубічний залежно від величини концентрації).
можна визначити концентрацію марганцю в газовій фазі як добуток парціального тиску марганцю на густину газової фази. Звичайно в розрахунках забрудненості газової фази пилом випарюваної речовини користуються її концентрацією (визначається в грамах або кілограмах на метр кубічний залежно від величини концентрації).
Процес випарювання відбувається поетапно: масоперенос марганцю в розчині заліза, тобто в металі, з об’єму останнього до поверхні випарювання; власне випарювання як перехід зі стану конденсованої речовини /рідини/ до газоподібного, що відбувається на поверхні розподілу; нарешті, переносу пари марганцю від поверхні розподілу до об’єму газової фази.
Швидкість масопереносу в металі та газовій фазі залежить від типу переносу. Якщо об’єму відповідної фази наближається до нуля, коли гравітаційного перемішування майже не відбувається, масоперенос визначається молекулярною дифузією. Якщо набуло розвитку гравітаційне перемішування в металі або в газовій фазі внаслідок різної густини в окремих місцях відповідної фази, швидкість масопереносу визначається природною конвекцією. Нарешті, при штучному вимушеному перемішуванні металу та газової фази швидкість масопереносу визначається штучною, вимушеною, конвекцією.
В усіх розглянутих випадках в окремих фазах визначаються коефіцієнти масопереносу марганцю в металі та пари марганцю в газовій фазі, які разом з константою швидкості власне переходу з конденсованого стану речовини до стану пари дають змогу розрахувати загальний, або сумарний, коефіцієнт масопереносу процесу в цілому 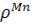 . За допомогою останнього визначається питома інтенсивність переносу за однією з фаз, найчастіше за металом:
. За допомогою останнього визначається питома інтенсивність переносу за однією з фаз, найчастіше за металом:
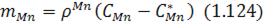
де: 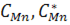 – концентрація марганцю відповідно в об’єму металу та на його поверхні.
– концентрація марганцю відповідно в об’єму металу та на його поверхні.
Концентрація марганцю на поверхні металу розраховується за його вмістом на поверхні 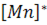 , що згідно з виразом для константи рівноваги реакції (1.122)визначається за рівнянням:
, що згідно з виразом для константи рівноваги реакції (1.122)визначається за рівнянням:
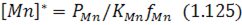
Пара речовини, у даному разі марганцю, у газовій фазі може опинитися в умовах, що відрізняються від умов, при яких відбувалося випарювання, тобто на поверхні розподілу металу і газової фази. У більшості випадків температура газової фази поступово знижується. Наприклад, у мартенівській печі або в конвертері газова фаза спочатку має високу температуру, але, рухаючись по тракту відводу газів, поступово втрачає теплоту, що знижує їх температуру аж до атмосферної під час викиду газів в атмосферу. Зниження температури супроводжується зменшенням парціального тиску пари марганцю, а різниця між первинною концентрацією, що створилася під час випарювання марганцю, й існуючою концентрацією згідно з тиском у даний момент часу, призводить до створення - конденсованого стану марганцю – його пилу.
Процес конденсації відбувається шляхом зародження об’єму нової фази – марганцю в конденсованому вигляді, його пилу з подальшим збільшенням розмірів зародків нової фази. Звичайно під час конденсації, що відбувається відповідно протягом процесу зниження температури, часточки пилу встигають збільшитися до субмікронного розміру. За цією ознакою пил, що утворився внаслідок випарювання, відрізняється від пилу, що з"явився в результаті механічного виносу малих часточок твердих або рідинних матеріалів і фаз, що набагато грубіші. Розмір більшої кількості часточок пилу випарювання становить близько 0,10 мкм.
Коли відбувається випарювання з багатокомпонентного розчину, яким є метал, то випарюються всі компоненти одночасно за своїми властивостями в рідкому стані. Тому пил від конденсації пари цих елементів, у тому числі заліза, є сумішшю цих речовин.
Концентрація пилу в газовій фазі залежить від наведених раніше чинників, але найсильніше від температури. У сталеплавильному виробництві найповніше вивчено випарювання металу, яке відбувається або при температурі ванни, або при температурі, що створюється внаслідок відповідних процесів.
Під час вдування окислюваних газів, насамперед кисню, до металу на поверхні розподілу розвиваються температури, які перевищують температуру ванни. Це відбувається в первинній зоні взаємодії, звідки гази, що утворюються, виходять насичені парою елементів, розчинних у залізі, і заліза. При цьому на випарювання істотно впливає окислення вуглецю на поверхні контакту металу з окислювачем у первинній реакційній зоні, оскільки внаслідок повного окислення металу створюється газова фаза, яка крім інших газів містить переважно 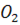 і також може насичуватись парою випарюваних елементів. Унаслідок кількість пилу, що створюється в первинній реакційній зоні при вдуванні окислювального газу у ванну, майже пропорційна до вмісту вуглецю в металі. Випарюються не лише метал, а й оксиди, що утворюються внаслідок окислення металу.
і також може насичуватись парою випарюваних елементів. Унаслідок кількість пилу, що створюється в первинній реакційній зоні при вдуванні окислювального газу у ванну, майже пропорційна до вмісту вуглецю в металі. Випарюються не лише метал, а й оксиди, що утворюються внаслідок окислення металу.
Оскільки найбільшою концентрація вуглецю в металі є звичайно на початку плавки, а протягом цього процесу зменшується, то кількість пилу, що утворюється, у цілому знижується протягом сталеплавильного процесу.
Вміст кисню при окислювальному дутті підвищується, а інших домішок зменшується при підвищенні температури в зоні взаємодії і збільшення кількості пилу, що утворюється. Тому застосування технічно чистого кисню в сталеплавильному виробництві, конвертерному та мартенівському процесах, поряд з підвищенням продуктивності процесів та інших техніко-економічних показників, істотно утруднюється через потребу очищення газів, що утворюються, від пилу. Іноді витрати на очищення газів від пилу становлять майже половину капітальних витрат при спорудженні цехів. Але незважаючи на це гази, що викидаються в атмосферу, забруднюють навколишнє середовище.
Зменшити випарювання можна шляхом зменшення температури в зоні взаємодії завдяки розведенню дуття за киснем, уведенню в дуття відновлювачів або матеріалів, що братимуть на своє нагрівання частину теплоти, яка виділяється при взаємодії, наприклад порошкове вапно. Ці заходи істотно впливають на технологію процесу, що треба враховувати при їх застосуванні. Сьогодні жодний із розглянутих заходів не застосовується для зменшення пилоутворення.
Разом із випарюванням запилення газової фази, одо виходить зі сталеплавильного агрегату, відбувається за рахунок механічного виносу пилоподібних шихтових матеріалів (вапно, вапняк, плавиковий шпат,- боксит, залізна руда тощо) унаслідок значної швидкості газів у сталеплавильних агрегатах, що досягає десятків метрів за секунду.
Запобігти цьому можна лише шляхом усунення малих часточок (пилоподібної фракції) шихтових матеріалів, розсіваючи їх перед використанням.
Нарешті, малі часточки (краплі) рідинних фаз плавки, металу і шлаку утворюються внаслідок виділення зі сталеплавильної ванни газів, що виникають переважно при окисленні вуглецю. Цічасточки, з одного боку, вилітають на велику висоту внаслідок значної первинної кінетичної енергії, яку вони отримують під час утворення, а з іншого – завдяки тому, що гази, які виділяються з ванни, підхоплюють їх і виносяться разом із ними зі сталеплавильного агрегату.
В окремих випадках пара речовин і пил, що утворюється, мають велику токсичність. Це стосується також звичайних елементів, насамперед марганцю і хрому. Свинець, що майже не розчиняється в залізі, використовують при виробництві окремих марок сталі шляхом змішування з нею під час розливки. Оскільки температура кипіння свинцю нижча за температуру сталі, парціальний тиск пари свинцю дорівнює атмосферному тиску, тобто є максимально можливим. Пара і пил свинцю мають велику токсичність, що потребує відповідних газоочисних пристроїв у зоні введення свинцю в сталь.
Деякі шихтові матеріали, наприклад плавиковий шпат, який застосовують для плавки, або сода, яку використовують під час позапічної обробки чавуну, сублімують і випарюються при температурах сталеплавильних процесів, а їх пара і пил токсичні. Як і в інших випадках, треба або вжити захисних заходів, або відмовитися від їх використання. Наприклад, свого часу великого поширення набуло використання плавикового шпату та інших флюоридів для виготовлення твердих сумішей, які застосовують при розливці сталі у виливниці* Оскільки при цьому запобігти шкідливим викидам у навколишнє середовище неможливо, довелося відмовитися від їх використання.
Дата добавления: 2020-02-05; просмотров: 774;











