Химические свойства алканов
Для алканов характерны реакции замещения атома водорода, разрыва углеродной цепи. Алканы содержат одни только ковалентные, неполярные, прочные σс-с- и σс-н-связи. Реакции алканов протекают только в жестких условиях и начинаются с гомолитического разрыва связей и образованием промежуточных частиц – углеводородных радикалов, (см. раздел 3.1.4).
Пример постадийных превращений алканов и промежуточных частиц - радикалов в процессе крекинга, (см. раздел 3.1.4). Ниже представлен механизм реакции замещения водорода на галоген, (SR), [8, c.75]:
I стадия – инициирование цепи. Начинается с гомолитического разрыва Cl – Cl связи в молекуле галогена, атаки образующегося хлорид – радикала, отыва атома водорода и образования метильного радикала:
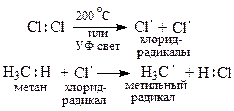
II стадия – рост цепи:
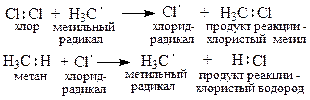
По аналогичной схеме реакция продолжается. Она включает в себя около 1000 подобных стадий. Затем цепь обрывается.
III стадия – обрыв цепи в результате рекомбинации:
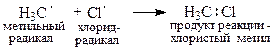
Направление реакции определяется свойствами промежуточных частиц – углеводородных радикалов. Радикальные реакции в органической химии протекают через образование преимущественно наиболее устойчивых радикалов. В алканах они протекают по атому углерода с наибольшим числом заместителей. Исключение – реакции с участием хлора.
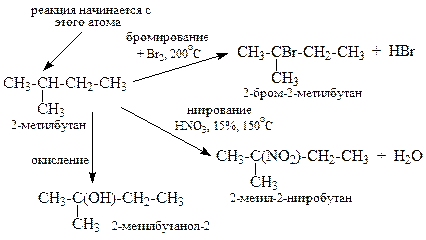
Хлорид-радикал – высокоактивен. Реакции с его участием начинаются по атому углерода с наибольшим числом водородов, поскольку вероятность столкновения в этом случае выше:
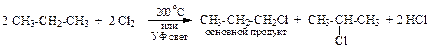
Мольное соотношение количеств веществ продуктов реакции 1-хлорпропан : 2-хлорпропан равняется 6 : 2, что соответствует соотношению количеств атомов водорода у первичных и вторичного углеродных атомов.
ТЕМА 4
Дата добавления: 2016-06-15; просмотров: 2553;











