Номенклатура ароматических соединений ряда бензола и изомерия в бензольном кольце.
Ароматические соединения.
Ароматичность.
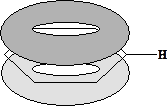 Эффект дополнительного перекрывания π-орбиталей (эффект сопряжения), наблюдаемый в диенах, возможен и в циклических молекулах. Более того, при чередовании простых и двойных связей в цикле, в некоторых случаях возможно полное обобществление π-электронов с образованием единой для всех р-электронов тороидальной молекулярной π-орбитали (на схеме указан только один атом водорода). При этом наблюдается значительный выигрыш в энергии. Соединения, обладающие такими свойствами, называются ароматическими, а тип сопряжения – ароматическим.
Эффект дополнительного перекрывания π-орбиталей (эффект сопряжения), наблюдаемый в диенах, возможен и в циклических молекулах. Более того, при чередовании простых и двойных связей в цикле, в некоторых случаях возможно полное обобществление π-электронов с образованием единой для всех р-электронов тороидальной молекулярной π-орбитали (на схеме указан только один атом водорода). При этом наблюдается значительный выигрыш в энергии. Соединения, обладающие такими свойствами, называются ароматическими, а тип сопряжения – ароматическим.
Критерии ароматичности:
1. Расположение участвующих во взаимодействии атомов в одной плоскости.
2. Наличие негибридизованной орбитали у всех участвующих в сопряжении атомов (не обязательно атомов углерода).
3. Структура должна удовлетворять правилу Хюккеля: количество π-электронов, участвующих в кольцевом сопряжении удовлетворяет формуле 4n+2 где n=0,1,2,3,....
Когда количество π-электронов равно 4n наблюдается «антиароматичность» - проигрыш в энергии при попытке сопряжения. Антиароматические соединения как правило не плоские и проявляют свойства обычных полиолефинов. В качестве примера можно привести циклооктатетраен-1,3,5,7, упоминавшийся ранее в качестве продукта тетрамеризации ацетилена.
4. Возникновение кольцевого молекулярного тока в переменном магнитном поле. Данный эффект наблюдается в спектрах ядерного магнитного резонанса на ядрах 1Н (ЯМР 1Н) в виде изменения резонансной частоты ядер водорода связанных с ароматическим кольцом по сравнению с неароматическими соединениями содержащими кратную связь.
Примеры моно и бициклических ароматических соединений:
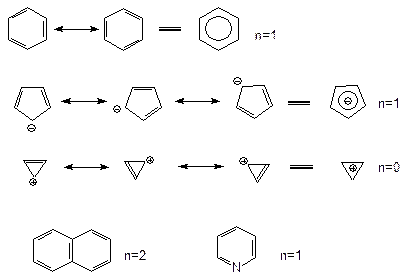 В циклопентадиенильном анионе (структура 2) на одной из участвующих в сопряжении р-орбиталей находится пара электронов, и суммарное количество π-электронов – 6, так что правило Хюккеля выполняется. В циклопропенильном катионе (структура 3), наоборот, одна из р-орбиталей вакантная (катионный центр) и поэтому в сопряжении участвуют только два электрона на трех орбиталях, что тоже соответствует правилу Хюккеля.
В циклопентадиенильном анионе (структура 2) на одной из участвующих в сопряжении р-орбиталей находится пара электронов, и суммарное количество π-электронов – 6, так что правило Хюккеля выполняется. В циклопропенильном катионе (структура 3), наоборот, одна из р-орбиталей вакантная (катионный центр) и поэтому в сопряжении участвуют только два электрона на трех орбиталях, что тоже соответствует правилу Хюккеля.
За счет делокализации электронов наблюдается значительный выигрыш в энергии (~80 ккал/моль).
Формы, изображенные на схемах с кратными связями, называются граничными (или резонансными)
Номенклатура ароматических соединений ряда бензола и изомерия в бензольном кольце.
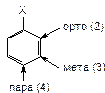
| Отсчет начинается от наиболее старшего заместителя в кольце (см. таблицу 1). Нумерация идет таким образом, чтобы сумма цифр была наименишей. Если с бензольным кольцом связана длинная углеводородная цепь, содержащая заместители, то, обычно, считают бензольное кольцо относительно этой цепи заместителем (фенил). |
Для дизамещенных производных бензола часто используют альтернативную номенклатуру. Рассматривают положение младшего заместителя относительно старшего (Х). Если но расположен рядом – используют приставку орто- (о-), если через один – мета- (м-), если напротив – пара- (п-).
В ряду ароматических соединений часто используются тривиальные названия соответствующих ядер и их замещенных. В этом случае нумерация в цикле осуществляется от того заместителя, который входит в тривиальное название (ему присваивается № 1). Также поступают в случае использования приставок орто-, мета- и пара-.

Дата добавления: 2016-06-15; просмотров: 4220;











