Силикаты определяют в виде кремниевой кислоты
SiO32–+2HOH ↔ H2SiO3↓+2OH–. Для усиления гидролиза добавляют кислоту и NH4Cl и нагревают.
3. Регулирование кислотности и щелочности р-ров. (Для увеличения pH добавляют CH3COONa, для уменьшения – NH4Cl).
Теории кислот и оснований
Классическое понятие кислот и оснований было введено Аррениусом. Кислоты – вещества, при диссоциации (ионизации) молекул которых в воде образуются катионы водорода Н+ (H2SO4). Основания – вещества, при диссоциации молекул которых в воде образуются гидроксил анионы ОН–(NaOH). Реакция нейтрализации сводится к образованию молекул (растворителя) воды.
С накоплением экспериментального материала было установлено, что некоторые вещества, например, соли проявляют кислотные или основные свойства, а в реакции нейтрализации не образуются молекулы растворителя. Наиболее ярко это проявляется в неводных растворителях. Например, NH4Cl в жидком аммиаке ведет себя как кислота; мочевина в жидком аммиаке – кислота, а в безводной уксусной кислоте – основание; HNO3 в жидком HF и безводной H2SO4 – основание.
В связи с этим Brönsted и Lowry предложили (1923) протолитическую теорию (теорию переноса протона) кислот и оснований: кислоты – вещества (или ионы), способные отдавать протоны (доноры протонов); основания – вещества (или ионы), способные принимать, получать протоны (акцепторы протонов). Кислоты делят на нейтральные, катионные и анионные. Каждая кислота имеет сопряженное основание и наоборот. Пару кислота-основание называют сопряженной парой.
А(кислота) ↔ Н+ + В(основание).
Реакция нейтрализации сводится к образованию новых кислот и основания.
А1 + В2 ↔ В1 + А2
Вещества, способные как отдавать, так и принимать протоны называются амфипротонные, например, Н2О, NH3. Они одновременно являются и кислотами, и основаниями.
Электронная теория кислот и оснований предложена Lewis. Кислоты – вещества (или ионы) способные принимать свободную пару электронов. Например, у атома алюминия в возбужденном состоянии электронная конфигурация:
13Al[Ne] 3s13p2 ↑↑↑ _ .
3s 3p
Три гибридные sp2 орбитали могут участвовать в образовании ковалентных связей, например, с атомами хлора, как в AlCl3. Свободная 3p орбиталь может быть использована для образования ковалентной связи по донорно-акцепторному механизму.
Основание ‑ вещества (или ионы), способные отдавать свободную пару электронов (NH3).
Примеры кислот и оснований по различным теориям приведены в табл.5.
Таблица 5
| Автор | Кислота | Основание | |||||||
| Arrhenius | H2SO4↔H+ + HSO4– | NaOH ↔OH– + Na+ | |||||||
| Brönsted, Lowry |  HCl
Нейтральные CH3COOH
кислоты H2O HCl
Нейтральные CH3COOH
кислоты H2O
H3O+ Катионные NH4+ кислоты [Al(H2O)6]3+
Анионные HCO3− кислоты H2PO4− | ↔ H+ + ↔ H+ + ↔ H+ + ↔ H+ + ↔ H+ + ↔ H+ + ↔ H+ + ↔ H+ + | Cl− CH3COO– OH– H2O NH3 [Al(H2O)5OH]2+ CO32− HPO42− | ||||||
| Lewis |  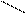  F F
 F B
F
Cl F B
F
Cl
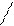 
  Al
Cl Cl Al
Cl Cl
| 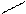 H H
   H N :
H H N :
H
| |||||||
Буферные системы
Buffer в буквальном переводе означает нечто, что уменьшает воздействие на систему внешней силы. В отношении растворов − это системы, способные сохранять, примерно, постоянную концентрацию ионов H+ при добавлении небольших количеств кислоты или щелочи, а также при разбавлении.
Такими буферирующими свойствами обладают смеси:
1. Cлабая кислота + ee соль сильного основания, например,
СН3СООН + СН3СООNa − ацетатный буфер (рН ~ 5);
2. Слабое основание + его соль сильной кислоты, например,
NH3 . H2O + NH4Cl − аммиачный буфер (рН ~ 9);
3. Смесь двух кислых разнозамещенных солей многоосновной кислоты, например, Na2HPO4 + KH2PO4 − фосфатный буфер (рН ~ 7);
4. Индивидуальная соль, например,
Na2B4O7 . 10H2O, рН~9;
5. Концентрированные растворы сильных кислот и щелочей.
Рассмотрим более подробно ацетатный буфер: уксусная кислота – слабый электпролит, ацетат натрия (соль) – сильный электролит.
СН3СООН ↔ СН3СОО− + Н+,
СН3СООNa → СН3СОО− + Na+.
Напишем выражение для константы ионизации слабой кислоты Kia и учтем, что в смеси концентрация ацетат аниона практически равна концентрации соли сs, а концентрация непроионизировавших молекул – концентрации кислоты ca
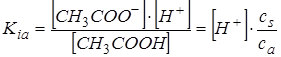 .
.
Выразим [H+] и pH:
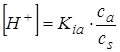 ,
, 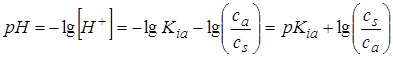 .
.
Из полученного уравнения Henderson-Hasselbalch следует, что pH такой буферной смеси определяется значением pKia и соотношением концентраций соли и кислоты. Если cs=ca, то pH = pKia и для ацетатного буфера pH = 4,76.
Рассуждая аналогично, получим для аммиачного буфера:
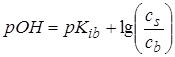 ,
, 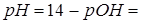
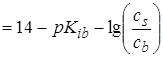 ,
,
где Kib и cb – константа ионизации и концентрация слабого основания смеси соответственно. Если cs=cb, то pH=14−pKib и для аммиачного буфера pH=14−4,75=9,25.
Дата добавления: 2022-02-05; просмотров: 589;