Электрохимическая коррозия
Электрохимическая коррозия – разрушение металлов в среде электролита.
Детали многих металлических конструкций работают в среде электролита: опоры мостов, водный транспорт, паровые котлы, химическая аппаратура, водопроводные трубы, кузова автомобилей. В сырую погоду, при суточных колебаниях темпертур на поверхности металлов конденсируется пленка воды, в которой растворяются газы из загрязненной атмосферы (СO2, SO2, NO2, H2S, и др.) и образуется электролит.
Поверхность металлов неоднородна. На поверхности металла имеются дефекты кристаллической решетки, примеси других металлов, включения соединений с неметаллами и интерметаллические соединения, продукты взаимодействия с окружающей средой (оксиды, гидроксиды, соли, грязь), неровности поверхности. Эти участки поверхности металла в растворе электролита будут иметь другой, отличный от основного металла потенциал. Таким образом, на поверхности металлов создается система локальных, короткозамкнутых через металл гальванических элементов. Работа этих микроскопических элементов сопровождается коррозионным разрушением металла.
В качестве примера рассмотрим модель гальвано-пары железо-медь в кислой и нейтральной средах. В гальванопаре Fe/Cu более активным является железо, стандартный потенциал которого –0,44 В, а у меди +0,34 В. В кислой среде на аноде будет проходить реакция окисления железа:
Fe0 –2ē → Fe2+.
Ионы железа – Fe2+ – будут переходить в раствор, электроны – на медь, заряжая ее отрицательно. На поверхности меди ионы Н+ из раствора восстанавливаются (водородная деполяризация):
2H+ +2ē → H2.
Суммарная окислительно-восстановительная реакция коррозии железа:
Fe0 + 2H+ → Fe2+ + H2.
В нейтральных и щелочных растворах на катодных участках поверхности металла происходит процесс восстановления растворенного в воде кислорода (кислородная деполяризация):
O2 + 2H2O +4ē → 4OH–.
Суммарная реакция коррозионного процесса:
2Fe0 + O2 + 2H2O → 2Fe2+ + 4OH–,
Fe2+ + 2OH– → Fe(OH)2.
В результате коррозии образуется Fe(OH)2, который дальше окисляется атмосферным кислородом воздуха до Fe(OH)3, окончательный продукт окисления – гидратированный оксид железа (III) (ржавчина):
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3 → 4FeOOH + 4H2O.
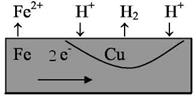
Рис. 9.4. Схема коррозии в кислой среде при контакте с менее активным металлом.
Гальванические пары возникают также при контакте металла с его химическими соединениями. Например, при коррозии стали анодом является зерна железа, катодом – карбид железа Fe3C (рис. 9.5).
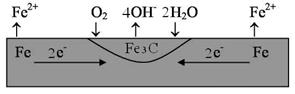
Рис. 9.5. Схема образования коррозионных гальванических микроэлементов в углеродистой стали, находящейся во влажном воздухе
Разность потенциалов может возникнуть вследствие различной концентрации растворенного кислорода. Раствор на поверхности металла и на участках, куда затруднен доступ кислорода, вследствие конструкционных особенностей деталей, содержит разное количество растворенного кислорода, что ведет к возникновению разности потенциалов на этих участках деталей.
В промышленных центрах атмосфера содержит загрязняющие газы: SO2, NO2, CO2, H2S и др., которые растворяясь в воде, дают кислоты, агрессивные по отношению к металлам. В кислой среде на железе будет протекать процесс коррзии с водородной деполяризацией. О влиянии состава атмосферного воздуха на скорость коррозии можно судить по следующим данным: в сельской местности скорость коррозии стали составляет 100-250, в промышленных городах 450-550 г/м2 в год.
В нейтральной среде (при достаточно чистой атмосфере) коррозия протекает с кислородной деполяризацией. Почему же скорость коррозии, прокающей с кислородной поляризацией ниже?
Для того чтобы коррозия имела место необходимо условие – электродный потенциал металла должен быть отрицательнее потенциала окислителя (деполяризатора).
Таблица 9.1
Зависимость потенциала газовых электродов от рН
| pН раствора | Е(2Н+/Н2,Pt), В | Окисляющиеся металлы | Е(О2/2ОН–), В | Окисляющиеся металлы |
| 0,0 | Pb | 1,23 | Hg | |
| –0,414 | Fe | 0,815 | Аg | |
| –0,828 | Щелочные и щ-зем., Zn, Al | 0,401 | Cu |
Как следует из данных приведенных в таблице, большинство металлов могут подвергаться коррозии с кислородной деполяризацией, но процесс этот медленный, т.к. кислород малорастворим в воде, и скорость его подвода к металлу невелика. Поступающий к поверхности металла кислород практически весь сразу же восстанавливается. При этом на поверхности некоторых металлов может образоваться защитная оксидная пленка, некоторые металлы при определенных условиях могут вообще переходить в пассивное состояние.
Дата добавления: 2017-11-21; просмотров: 2333;











