Свойства разбавленных молекулярных растворов
Растворы органических веществ представляют собой равномерное распределение в растворителе молекул растворенного вещества, поэтому их относят к молекулярным растворам. Их свойства зависят от природы растворителя, растворенного органического вещества и концентрации.
Некоторое количество молекул растворенного вещества входит в состав поверхностного слоя, вытесняя с поверхности раздела фаз (раствор-пар) молекулы растворителя, поэтому давление насыщенного пара растворителя над раствором окажется ниже, чем над чистым растворителем. Чем выше концентрация раствора, тем больше понижение давления пара растворителя над раствором. Эта зависимость описывается законом Рауля.
Закон Рауля
Относительное понижение давления пара растворителя равно отношению числа моль растворенного вещества к сумме моль растворителя и растворенного вещества:
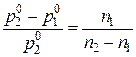 , ,
| (7.7) |
где р02 – давление пара над чистым растворителем; р1 – давление пара растворителя над раствором; 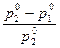 – относительное понижение давления пара растворителя; n1 – число молей растворенного вещества; n2 – число молей растворителя.
– относительное понижение давления пара растворителя; n1 – число молей растворенного вещества; n2 – число молей растворителя.
Закон Рауля можно сформулировать иначе: относительное понижение давления пара растворителя равно мольной доле растворенного вещества, так как 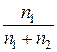 – мольная доля.
– мольная доля.
Дата добавления: 2017-11-21; просмотров: 1823;











