Сущность абсорбции. Законы Генри и Дальтона.
Абсорбция – избирательное поглощение отдельных компонентов из газовых или паровых смесей жидким поглотителем, т. е. абсорбентом.
Абсорбция делится на физическую и химическую. В процессе физической абсорбции поглощаемый компонент (абсорбтив) растворяется в абсорбенте физически. В процессе химической абсорбции (хемосорбции) физическое растворение абсорбтива сопровождается химической реакцией.
Десорбция – выделение из абсорбента ранее поглощенного абсорбтива (например, при понижении давления или повышении температуры). При этом абсорбент регенерируется (восстанавливается).
Цели абсорбции:
1) получение целевых продуктов (SO3 + H2O = H2SO4)
2) выделение ценных компонентов из газовых смесей (NH3 из коксового газа)
3) удаление вредных примесей из газов (CO и CO2 из азотоводородной смеси N2 + H2)
4) разделение газовых смесей
Требования к абсорбенту – избирательность (селективность), высокая поглотительная способность, химическая инертность, пожаро- и взрывобезопасность, отсутствие коррозионной активности, нетоксичность (неядовитость), доступность и дешевизна, регенерация.
Равновесное парциальное давление абсорбтива в газовой фазе (над раствором) 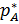 пропорционально мольной доле абсорбтива в жидкой фазе (растворе).
пропорционально мольной доле абсорбтива в жидкой фазе (растворе).
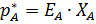 – закон Генри
– закон Генри
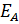 – константа (коэффициент) Генри – справочная опытная величина
– константа (коэффициент) Генри – справочная опытная величина
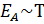
С другой стороны, это же давление 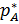 пропорционально мольной доле абсорбтива в газовой фазе.
пропорционально мольной доле абсорбтива в газовой фазе.
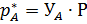 – закон Дальтона
– закон Дальтона
Р – общее давление в газовой смеси
Комбинируя эти законы, можно получить: 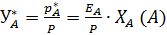
Преобразуем (А): 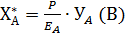
Согласно (В) равновесная растворимость газа в жидкости пропорциональна температуре, т. е. 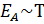
Закон Генри справедлив для идеальных (сильно разбавленных) растворов при не слишком высоких температурах и давлениях, но выше критической температуры газов.
Проиллюстрируем соотношение (В) с помощью диаграммы фазового равновесия состав – состав.
Скорость абсорбции подчиняется основному уравнению массопередач:
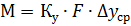
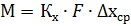
72. Материалҗный баланс абсорбера. Удельный расход абсорбента.
Рассмотрим мат. баланс противоточного вертикального абсорбера, работающего в режиме идеального вытеснения.
Расходы инертного газа и абсорбента в аппарате постоянны:
G = const, 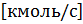 ; L = const,
; L = const, 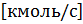
У – относительная мольная концентрация абсорбтива в газовой фазе
X – относительная мольная концентрация абсорбтива в жидкой фазе
 ;
; 
Составим мат. баланс абсорбера по абсорбтиву:
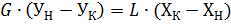
Общий расход абсорбента в аппарате: 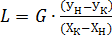
Удельный расход абсорбента: 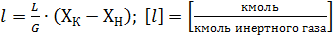
Составим мат. баланс абсорбера по абсорбтиву для верхней части аппарата (выше произвольного сечения 1 – 1)
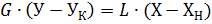
Выразим отсюда У:
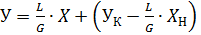 –уравнение рабочей линии противоточного абсорбера (линейное уравнение типа у = kx + b).
–уравнение рабочей линии противоточного абсорбера (линейное уравнение типа у = kx + b).
tg угла наклона рабочей линии по отношению к оси абсцисс равен удельному расходу абсорбента: 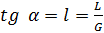
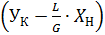 – отрезок, отсекаемый на оси ординат рабочей линии
– отрезок, отсекаемый на оси ординат рабочей линии
Нарисуем рабочую диаграмму массообмена состав – состав.
При увеличении удельного расхода абсорбента 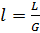
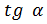 растет, т.е. рабочая линия противоточного абсорбера поворачивается вокруг точки А против часовой стрелки. При этом предельное положение рабочей линии, т.е. АВ1 достигается при
растет, т.е. рабочая линия противоточного абсорбера поворачивается вокруг точки А против часовой стрелки. При этом предельное положение рабочей линии, т.е. АВ1 достигается при 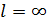 . При этом высота проектируемого абсорбера минимальна. Другое предельное положение рабочей линии, т.е. АВ3 соответствует минимальному удельному расходу абсорбента
. При этом высота проектируемого абсорбера минимальна. Другое предельное положение рабочей линии, т.е. АВ3 соответствует минимальному удельному расходу абсорбента 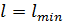 . Однако, при этом высота проектируемого абсорбера бесконечно большая.
. Однако, при этом высота проектируемого абсорбера бесконечно большая.
При 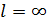 диаметр абсорбера равен
диаметр абсорбера равен 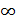 , а при
, а при 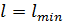 диаметр – минимальный. Т.к.
диаметр – минимальный. Т.к. 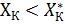 , то
, то 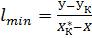 . Оптимальный удельный расход абсорбента определяется технико – экономическим расчетом. Это очень важно, потому что от удельного расхода абсорбента сильно зависят как капитальные затраты, так и эксплуатационные расходы на процесс абсорбции.
. Оптимальный удельный расход абсорбента определяется технико – экономическим расчетом. Это очень важно, потому что от удельного расхода абсорбента сильно зависят как капитальные затраты, так и эксплуатационные расходы на процесс абсорбции.
Дата добавления: 2017-09-01; просмотров: 3485;











