Химические свойства
Химические свойства моносахаридов определяются наличием карбонильной группы (в ациклической форме), полуацетального гидроксила (в циклических формах) и спиртовых ОН групп.
Восстановление
При восстановлении карбонильной группы альдоз образуются многоатомные спирты – глициты.
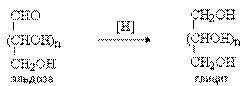
В лабораторных условиях для восcтановления используют NaBH4. В промышленности применяют каталитическое гидрирование. Таким образом получают заменители сахара: из D-глюкозы - сорбит (D-глюцит), из D-ксилозы – ксилит.
Восстановление альдоз приводит к “уравниванию” функциональных групп на концах цепи. В результате из некоторых альдоз (эритрозы, рибозы, ксилозы, аллозы, галактозы) образуются оптически неактивные мезо-соединения, например:
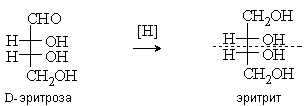
Разные альдозы при восстановлении могут дать один и тот же спирт.
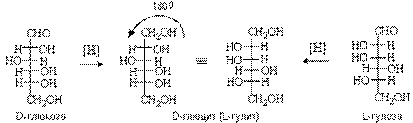
Такая конфигурационная взаимосвязь между глицитами использовалась для установления стереохимической конфигурации моносахаридов.
При восстановлении кетоз из карбонильной группы возникает новый хиральный центр и образуется смесь неравных количеств диастереомерных спиртов (эпимеров по С-2).
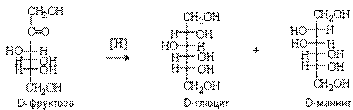
Эта реакция доказывает, что D-фруктоза, D-глюкоза и D-манноза имеют одинаковые конфигурации хиральных центров С-2, С-3, и С-4.
Окисление
Вследствие своей полифункциональности альдозы окисляются по-разному при действии различных окислителей. При этом может быть окислена карбонильная группа, оба конца углеродной цепи или расщеплена связь С-С.
Получение гликоновых кислот
При мягком окислении альдоз, например, под действием бромной воды, затрагивается только карбонильная группа и образуются гликоновые кислоты, которые очень легко образуют пяти- и шестичленные лактоны.
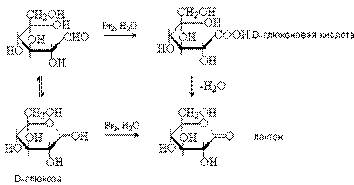
Кетозы в этих условиях не окисляются и могут быть таким образом выделены из смесей с альдозами.
Альдозы и кетозы дают реакции, характерные только для соединений, содержащих альдегидную группу: они восстанавливают в щелочной среде катионы металлов Ag+ (Ag(NH3)2OH – реактив Толенса) и Cu2+ (комплекс Cu2+ с тартрат-ионом – реактив Фелинга). При этом гликоновые кислоты образуются в незначительном количестве, так как в щелочной среде протекает деградация углеродного скелета моносахаридов.
Альдоза + Ag(NH3)2+ ----> гликоновая кислота + Ag + продукты деструктивного окисления
Альдоза + Cu2+ ----> гликоновая кислота + Cu2O + продукты деструктивного окисления
Сахара, способные восстанавливать реактивы Толенса и Фелинга, называют восстанавливающими. Кетозы проявляют восстанавливающие свойства за счет изомеризации в щелочной среде в альдозы, которые и взаимодействуют далее с окислителем. Процесс превращения кетозы в альдозу происходит в результате енолизации. Образующийся из кетозы енол является общим для нее и 2-х альдоз (эпимеров по С-2). Так, в слабощелочном растворе в равновесии с D-фруктозой находятся ендиол, D-глюкоза и D-манноза.
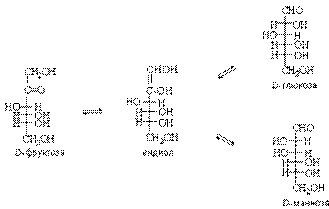
Взаимопревращения в щелочном растворе между альдозами, эпимерами по С-2, называют эпимеризацией.
Получение гликаровых кислот
При действии разбавленной азотной кислоты окисляется оба конца углеродного скелета альдоз и образуются гликаровые кислоты.
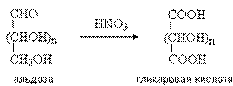
При образовании гликаровых кислот, как и в случае глицитов, происходит “уравнивание” функциональных групп на концах цепи и из некоторых альдоз образуются мезо-соединения.
Окисление кетоз азотной кислотой протекает с расщеплением С-С связей.
В природе широко распространены гликуроновые кислоты.
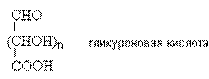
В лабораторных условиях они могут быть получены только многостадийным синтезом, так как окисление спиртовой группы в присутствии альдегидной требует предварительной защиты последней. Гликуроновые кислоты входят в состав полисахаридов (пектиновые вещества, гепарин). Важная биологическая роль D-глюкуроновой кислоты состоит в том, что многие токсичные вещества выводятся из организма с мочой в виде растворимых глюкуронидов.
Получение гликозидов
Циклические формы моносахаридов содержат несколько групп ОН, одна из которых – гликозидный (полуацетальный) гидроксил, отличается повышенной склонностью к реакциям нуклеофильного замещения.
Известно, что в присутствии кислотных катализаторов полуацетали реагируют со спиртами. При этом происходит нуклеофильное замещение полуацетального гидроксила и образуются полные ацетали.
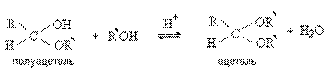
Аналогично реагирует гликозидный гидроксил в альдозах и кетозах. Спиртовые ОН группы при этом не затрагиваются. Продукты замещения гликозидного гидроксила называют гликозидами (гликопиранозидами или гликофуранозидами в зависимости от размера цикла). Например, при пропускании через раствор D-глюкозы в метаноле газообразного HCl образуется смесь метилглюкозидов, соответствующих разным таутомерным формам D-глюкозы (двум пиранозным и двум фуранозным). В условиях термодинамического контроля в реакционной смеси преобладают более стабильные метилпиранозиды.
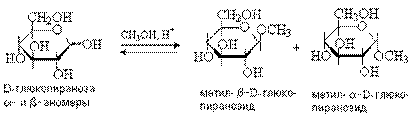
Метил-a-D-глюкопиранозид большей термодинамической стабильностью, чем b-аномер и поэтому образуется в большем количестве. Гликозиды существуют только в циклической форме, поэтому a- и b-аномеры гликозидов не могут спонтанно переходить друг в друга в результате таутомерных превращений. Гликозиды не имеют свободной альдегидной группы и являются невосстанавливающими сахарами.
Дата добавления: 2017-04-05; просмотров: 3539;











