Лекция на тему: 7 Липиды. Сложные эфиры карбоновых кислот. Жиры. Мыла.
Сложные эфиры – производные карбоновых кислот, которые можно рассматривать как результат замещения гидроксильной группы карбоновой кислоты на алкоксирадикал
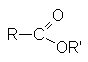
Методы получения сложных эфиров:
Этерификация карбоновых кислот (см. химические свойства карбоновых кислот).
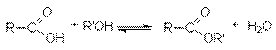
Ацилирование спиртов галогенангидридами и ангидридами карбоновых кислот.
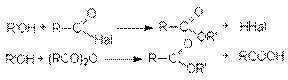
Ацилирование алкоголятов галогенангидридами и ангидридами карбоновых кислот. 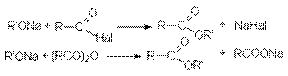
Алкилирование солей карбоновых кислот.
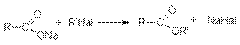
Этерификация амидов и нитрилов карбоновых кислот.
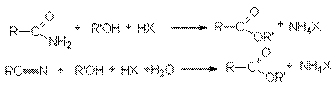
Физические свойства и строение сложных эфиров
Сложные эфиры являются бесцветными жидкостями или кристаллическими веществами с приятным запахом. Температура кипения сложных эфиров обычно ниже чем температура близких по молекулярной массе карбоновых кислот. Это свидетельствует об уменьшении межмолекулярных взаимодействий, что объясняется отсутствием межмолекулярных водородных связей.
Химические свойства
Объектами нуклеофильной атаки могут быть ацильный или алкильный углерод. В то же время кислотность водородных атомов при -углеродном атоме радикала кислоты обусловливает склонность сложность эфиров к реакции конденсации.
Реакции нуклеофильного замещения
Гидролиз.
Различают кислотнокаталитический гидролиз и основной гидролиз (омыление). Кислотный гидролиз представляет собой обратимую реакцию.
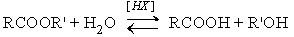
Механизм этой реакции – см в разделе Кислотно-каталитическая этерификация – Химические свойства карбоновых кислот.
Реакция омыления необратима. Основание не только ускоряет реакцию гидролиза, но выступает в качестве реагента. Эффективность реакции обусловлена высокой нуклеофильной активностью гидроксил-анионов.
RCOOR' + NaOH RCOONa + R'OH
Реакция катализируется кислотами или основаниями.
Взаимодействие с магний- и литий-органическими соединениями.
а) Реакция с магнийорганическими соединениями подобна реакции с галогенангидридами.
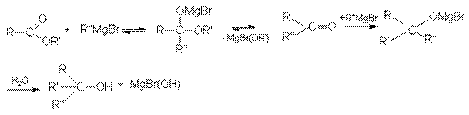
б) Взаимодействие с Li-органическими соединениями.
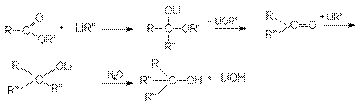
Реакции восстановления.

Реакции конденсации
Конденсация Кляйзена – наиболее важная в синтетическом отношении реакция. Ее стехиометрический результат заключается в автоконденсации этилацетата, катализируемая этилатом натрия. 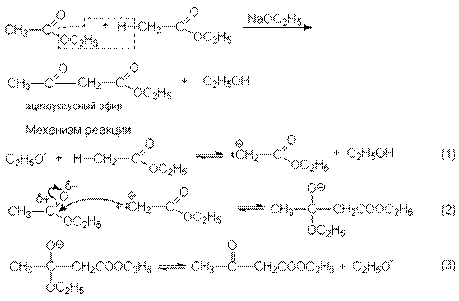
Условия равновесия неблагоприятны для всех трех стадий. Поэтому равновесие брутто-реакций существенно смещено в левую сторону.
Липиды
Липиды имеют большое значение в питании человека. Они не только выполняют роль энергетического резерва, но и входят в состав всех тканей организма.
Липидами называются неоднородные в химическом отношении вещества, большинство из которых представляют собой сложные эфиры карбоновых кислот и спиртов. В зависимости от вида спирта и органической кислоты сложные эфиры можно условно подразделить на три вида:1. фруктовые, являющиеся производными низших карбоновых кислот и низших спиртов;2. воски - производные высших спиртов и высших карбоновых кислот; 3. жиры - производные глицерина и, как правило, высших карбоновых кислот.
В молекулах липидов находится большое количество гидрофобных радикалов и группировок, поэтому общими свойствами липидов является их гидрофобность и нерастворимость в воде, но они по-разному растворяются в органических растворителях.
Сложные эфиры простейших и средних кислот и спиртов представляют собой жидкости легче воды, летучие, в большинстве случаев обладающие приятным запахом фруктов. Жиры в пищевых продуктах встречаются чаще и в больших количествах, чем другие соединения групп липидов.
Жиры в организме являются важным источником энергии, участвуют в пластических процессах организма, в них растворяются биологически активные вещества - витамины А, D, Е, К, фосфолипиды, стерины. Всостав жиров входят не синтезируемые организмом человека полиненасыщенные жирные кислоты - линолевая, линоленован, арахидоновая, которые называются незаменимыми.
По происхождению жиры делят на растительные и животные. Растительные жиры обычно называют маслами. Их добывают из семян и мякоти плодов различных растений. Растительные жиры делят на твердые и жидкие. К твердым жирам относят масло какао, кокосовое и пальмовое. Жидкие жиры отличаются высоким содержанием непредельных кислот. Наличие в растительных маслах непредельных и особенно незаменимых
полиненасыщенных кислот придает им особую пищевую ценность. Жидкие жиры в зависимости от свойств делят на невысыхающие
(оливковое, миндальное и др.), полувысыхающие (подсолнечное, хлопковое и др.) и высыхающие (льняное, конопляное, маковое и др.).
Высыхающие растительные масла содержат глицериды кислот с двумя и более двойными связями, при окислении они образуют прозрачные пленки.
Животные жиры добывают из жировых тканей различных животных, из молока. Животные жиры также подразделяют на жидкие и твердые.
Различают жидкие животные жиры наземных животных (копытный жир) и жидкие жиры морских животных и рыб (рыбий жир, жир печени китовых). К животным твердым относят жиры говяжий, бараний, свиной, а также коровье масло.
2. Содержание жиров в пищевых продуктахЖиры как запасные вещества находятся в соединительной тканиживотных и рыб, в жировой ткани, подкожной клетчатке, печени икостях, а также в семенах растений и иногда в мякоти плодов.
В растениях одного и того же вида состав и свойства жира могут колебаться в зависимости от климатических условий произрастания. Содержание и качество жиров в животном сырье также зависит от породы, возраста, степени упитанности, пола, сезона года и т.д.Жиры широко используют, при производстве многих пищевых продуктов, они обладают высокой калорийностью и пищевой ценностью, вызывают длительное чувство насыщения. Жиры являются важными вкусовыми и структурными компонентами в процессе приготовления
В жирах, полученных из растительных и животных тканей, кроме глицеридов, могут находиться свободные жирные кислоты, фосфатиды, стеролы, пигменты, витамины, вкусовые и ароматические вещества, ферменты, белки и др., которые влияют на качество и свойства жиров. На вкус и запах жиров также оказывают влияние вещества, образующиеся в жирах при хранении (альдегиды, кетоны, перекисные и другие соединения).Жиры в организм человека должны постоянно поступать с пищей. Потребность в жирах зависит от возраста, характера работы, климатических условий и других факторов, но в среднем в сутки взрослому человеку необходимо от 80 до 100 г жиров. В суточном рационе должно быть примерно 70 % животных и 30 % растительных жиров.
3.Строение и свойства жиров
По химическому составу жиры представляют собой смесь сложных эфиров трехатомного спирта глицерина С3Н5(ОН)3 и жирных кислот. Формулу триглицерида в общем виде можно представить так: О
СН2О — С — R1
О
СНО — С — R2
О
СН2О — С — R3
Жирные кислоты, входящие в состав жиров, в зависимости от характера связи углеродных атомов в углеводородной цепи делятся на предельные и непредельные.
Предельные жирные кислоты СnН2nОn не способны к реакциям присоединения. Они подразделяются на низко- и высокомолекулярные в зависимости от числа углеводородных групп в углеводородной цепи. Непредельные жирные кислоты по числу двойных связей могут быть моноеновые (с одной двойной связью), диеновые (с двумя), триеновые (с тремя), тетраеновые (с четырьмя), пентаеновые (с пятью) и гексаеновые (с шестью двойными связями). По месту двойных связей врадикале жирных кислот могут присоединяться водород, кислород, галогены, при этом изменяются свойства жирных кислот.
Большинство жиров пищевых продуктов состоит из разно кислотных триглицеридов, содержащих в молекуле две или три различные кислоты. Встречаются, но реже, и однокислотные триглицериды. В отдельных видах жиров преобладают те или иные жирные кислоты. Жиры различного происхождения отличаются друг от друга по составу жирных кислот. В природе известно около 70 различных жирных кислот, но наиболее важными и часто встречающимися в жирахявляются следующие пять:
пальмитиновая – СН3(СН2)14 СООН;
стеариновая - СН3(СН2)16 СООН;
олеиновая - СН3(СН2)7–СН=СН–(СН2)7 СООН;
линолевая - СН3(СН2)4–СН=СН–СН2–СН=СН–(СН2)7 СООН;
линоленовая - СН3–СН2–СН=СН–СН2–СН=СН–СН2–СН=СН–(СН2)7 СООН.
Из приведенных формул видно, что из пяти кислот две являются предельными и три – непредельными.
Свойства триглицеридов в основном обусловлены свойствами жирных кислот. Так, преобладание предельных или непредельных жирных кислот оказывает существенное влияние на температуру плавления жиров. При комнатной температуре жиры имеют твердую, мазеобразную и жидкую консистенцию. В глицеридах твердых жиров преобладают высокомолекулярные предельные жирные кислоты. В свином жире по сравнению с говяжьим больше полиненасыщенных жирных кислот, и его температура плавления ниже.
В растительных жирах и жирах рыб преобладают ненасыщенные жирные кислоты. Большинство растительных жиров, богатых непредельными жирными кислотами, остается в жидком состоянии при температурах, близких к 0 °С и ниже.
В жирах рыб ненасыщенные жирные кислоты составляют 62-82%,поэтому рыбий жир при комнатной температуре жидкий. Жидкие жиры при охлаждении загустевают. Твердые жиры при повышении температуры переходят в жидкое состояние в пределах некоторого интервала температур, так как они состоят из смеси различных триглицеридов.
Непредельные жирные кислоты благодаря наличию в молекуле двойных связей обладают более низкой температурой плавления по сравнению с предельными. Чем выше молекулярный вес предельных жирных кислот, тем выше температура их плавления. Предельные жирные кислоты менее активны, чем непредельные.
Температура плавления жиров при известных соотношениях в их составе жирных кислот будет ниже температуры плавления каждой из кислот. Усвояемость жиров в значительной степени зависит от их температуры плавления. Чем выше температура плавления жира, тем он труднее усваивается.
По усвояемости жиры можно разделить на три группы:
• с температурой плавления ниже 37 °С, усвояемость их составляет 97-98 %; к ним относят все жидкие растительные жиры, жиры молока, свиное топленое и гусиное сало, жиры других птиц и разных рыб;
• с температурой плавления выше 37 °С, к которым относят тканевый жир рогатого скота; усвояемость такого жира около 90 %;
• с температурой плавления 50-60 °С, такие жиры усваиваются плохо.
Растворы жиров имеют кислую реакцию. Жиры не растворимы в воде, но в присутствии белковых, слизистых или некоторых других веществ, называемых эмульгаторами, способны образовывать с водой стойкие эмульсии. На этом свойстве жиров основано получение маргарина, майонеза, различных кремов.
Сами жиры могут растворять в пределах температуры до 100 °С небольшое количество воды, не превышающее 1 % массы жира. В чистом виде жиры растворимы в растворителях - серном и петролейном эфирах, хлороформе, сероуглероде, четырехлористом углероде, бензине и др. Жиры способны растворять некоторые ароматические вещества. Жиры не летучи. При нагревании свыше 200°С жиры кипят, при нагревании до 250-300 °С они разрушаются с выделением свободных жирных кислот и различных смолообразных продуктов их полимеризации.
4. Физико-химические показатели жиров
Жиры характеризуются некоторыми общими физико-химическими показателями, к которым относятся плотность, температуры плавления и застывания, коэффициент преломления, вязкость, кислотное число, число омыления, йодное число и др. Сопоставление полученных при анализе физико-химических показателей позволяет установить природу, качество и степень свежести жира. Кислотное число показывает, сколько миллиграммов едкого калия требуется для нейтрализации свободных жирных кислот, содержащихся в 1 г жира. Увеличение кислотного числа свидетельствует об увеличении количества свободных жирных кислот, которые накапливаются в жире при его гидролизе. Число омыления характеризуется количеством миллиграммов едкого калия, необходимого для нейтрализации как свободных, так и связанных с глицерином жирных кислот, содержащихся в 1 г жира.
Чем выше йодное число, тем жир легче окисляется и менее устойчив при хранении. По йодному числу можно также судить о свежести жира. Перекисное число характеризует количество присутствующих в жире перекисей, а также степень свежести жиров, т.к. образовавшиеся органические перекиси являются первичным продуктом при прогоркании.
Жиры легче воды, плотность их составляет 0,91-0,97 кг/дм3. Коэффициент преломления (рефракции) характеризует природу жира и возрастает при наличии оксигрупп, с увеличением молекулярной массы и количества непредельных жирных кислот.
Температура плавления жиров - температура, при которой жир из твердого состояния переходит в капельно-жидкое состояние, приобретает прозрачность. Она находится в обратной зависимости от содержания ненасыщенных и низкомолекулярных насыщенных жирных кислот. Температура плавления жиров всегда на несколько градусов выше температуры застывания.
Температура дымообразования жиров – температура, при которой жиры начинают дымить и разлагаться. На температуру дымообразования влияет содержание в жире свободных жирных кислот. Вязкость жиров характеризует содержание в жире продуктов полимеризации и возрастает по мере увеличения продолжительности нагревания жира.
5. Изменения жиров при хранении. Характер и степень изменения жиров при хранении зависят от воздействия на них воздуха и воды, температуры и продолжительности хранения, а также от наличия веществ, способных вступать в химическое взаимодействие с жирами. Жиры могут претерпевать различные изменения – от инактивации содержащихся в них биологически активных веществ до образования токсичных соединений.
Гидролитическое расщепление жиров протекает в процессе изготовления и хранения жиров и жиросодержащих продуктов. Жиры при определенных условиях реагируют с. водой, образуя глицерин и жирные кислоты:
О
СН2О — С — R1 СН2ОН
О
СНО — С — R1+ 3Н2О —— СНОН +3R1 — СООН
О
СН2О — С — R1 СН2ОН
При низких отрицательных температурах гидролитическое расщепление жиров не происходит. При пониженных температурах (около 0°С) скорость гидролиза ничтожна. Реакция гидролитического расщепления жиров ускоряется с повышением температуры, а также в присутствии щелочей и кислот. Наличие сопутствующих веществ (белков, липоидов и др.) увеличивает скорость гидролиза жира. В копченых колбасах, беконе, соленом шпике наблюдается глубокий гидролиз жиров при изготовлении и особенно при хранении.
Гидролитический распад жиров является одной из причин ухудшения качества пищевых продуктов. Особенно ускоряется этот процесс с повышением влажности хранящихся продуктов, температуры и активности липазы.
Окисление жиров, или окислительное прогоркание, - это взаимодействие кислорода воздуха и остатков жирных кислот. Окисление жиров - наиболее распространенный вид порчи жиров во время хранения. Различают самоокисление (неферментативное или автоокисление) и ферментативное (называемое кетонным) окисление жиров.
Самоокисление (автоокисление) протекает с большой скоростью при обычных температурах хранения. Оно связано со способностью жиров, и особенно их высоконепредельных жирных кислот, к радикальным реакциям.
Самоокисление жиров ускоряют температура, наличие кислорода в окружающей среде, свет, особенно ультрафиолетовый, а также ионизирующие излучения. Активными катализаторами этого процесса являются металлы переменной валентности.
Процесс самоокисления можно затормозить с помощью химических веществ, вступающих в реакцию с гидроперекисями без образования свободных радикалов, т.е. веществ, способных обрывать цепную реакцию. Такие вещества называются антиокислителями. Роль естественных антиоксидантов в растительных жирах играют токоферолы (витамин Е), каротиноиды, фосфатиды, фенольные соединения, амины, меланоидины и др.
Иногда процесс окисления жиров приобретает своеобразное направление, характеризующееся исчезновением окраски, уплотнением жира, появлением салистой консистенции. Такой процесс получил название осаливания. При осаливании образуется значительное количество оксисоединений.
Для предотвращения порчи жиров необходимо по возможности уменьшить или исключить его соприкосновение с кислородом воздуха и источником энергии – светом, теплом. Жир целесообразно хранить в герметичной таре при низкой температуре. Для длительного хранения пригодны только хорошо очищенные жиры, свободные от остатков тканей, белковых, слизистых веществ. Твердые жиры имеют ряд преимуществ перед жидкими, т.к. процессы окисления в них происходят значительно медленнее.
Фосфолипиды, стерины, воски, их характеристика
Из липоидов, или жироподобных веществ, в пищевых продуктах наиболее широко распространены фосфолипиды, стеролы и воски. Фосфолипиды широко распространены в растительных и животных тканях. Основная масса фосфолипидов участвует в формировании клеточных оболочек и внутриклеточных мембран. Из фосфолипидов и пищевых продуктах содержатся прежде всего фосфоглицериды - близкие к жирам соединения, в состав которых, кроме жирных кислот и глицерина, входят остаток фосфорной кислоты и одно из азотистых оснований (холин, коламин или серин).
Фосфоглицериды растворимы в жирах и органических растворителях. Фосфоглицериды с водой образуют эмульсии и коллоидные растворы, легко гидролизуются, являются поверхностно-активными веществами. В состав фосфоглицеридов могут входить как предельные, так и непредельные жирные кислоты, от чего и зависит разнообразие их свойств.
В зависимости от строения полярной группы фосфоглицериды делят на фосфатидилхолины (старое название - лецитины), фосфатидилэтаноламины (старое название - кефалины), фосфатидилсерины и т. д.
В пищевых продуктах содержатся прежде всего фосфатидилхолины и фосфатидилэтаноламины. В молекуле лецитина две гидроксильные группы глицерина этерифицированы жирными кислотами, третий ее водный остаток соединен с фосфорной кислотой, которая в свою очередь связана с азотистым основанием – холином. В кефалине вместо холина находится азотистое основание - коламин. В чистом виде фосфатидилхолины - воскообразные вещества белого цвета, которые обладают большой эмульсионной способностью и легко гидролизуются под действием фермента липазы. Лецитины в больших количествах находятся в клетках животных тканей, в растительных - меньше. Так, содержание их составляет (в %): в яичном желтке - 9,4, в молочном жире – 1,3, в пшенице - 0,65, во ржи – 0,57.
Лецитины применяются в качестве эмульгатора в маргариновом ишоколадном производстве, в производстве мороженого, а также в медицине. Кефалины встречаются в тех же клетках и тканях что и лецитины, но в меньших количествах.
При хранении продуктов фосфоглицериды могут расщепляться под влиянием кислот, щелочей или соответствующих ферментов.
Стерины относятся к классу стероидов - эфиров, образованных высокомолекулярными одноатомными спиртами с жирными кислотами. Представители только одного класса стероидов - стерины - содержатся в клетках в заметных количествах. Стерины - высокомолекулярные гидроароматические спирты. Стерины, находящиеся в тканях животных, называют зоостеринами, в растительных - фитостеринами.
Представителем зоостеринов является высокомолекулярный спирт холестерин (С25Н45ОН). Он участвует в образовании некоторых гормонов надпочечников и других биологически активных веществ, холестерин способен также связывать и обезвреживать в организме бактериальные гемотоксины.
В организм холестерин поступает с пищей и синтезируется самим организмом.
Воски - это группа жироподобных веществ, построенных эфирообраэно из высокомолекулярных одноатомных спиртов и высших монокарбоновых жирных кислот. В отличие от жиров в образовании восков глицерин не принимает участия. Часто в состав восков входят свободные жирные кислоты и спирты, а также углеводороды, красящие и ароматические
веществ.
Все воски при обычных условиях твердые. Различают воски растительного и животного происхождения. Воски в растениях и животных выполняют главным образом защитную функцию. В растениях воски покрывают тонким слоем листья, стебли, плоды, предохраняя их от смачивания, проникновения микроорганизмов и испарения влаги, а также воски рассеяны внутри клетки, как жиры.
К представителям восков животного происхождения относятся пчелиный воск, ланолин - воск, содержащийся в овечьей шерсти, и спермацет, добываемый из черепных полостей кашалота. Различные воски широко используют при изготовлении свечей, помад, мыла, разных пластырей и др.
Дата добавления: 2017-04-05; просмотров: 4320;











