Гравиметрический анализ
Гравиметрией называют метод количественного анализа, заключающийся в точном измерении массы определяемого компонента пробы, выделенного в виде соединения известного состава. (Классическое название - весовой анализ.) Гравиметрический анализ основан на законе сохранения массы веществ при химических превращениях. Это наиболее точный из химических методов анализа, его характеристики: предел обнаружения - 0,10%; правильность - 0,2 отн. %. В гравиметрии используют реакции обмена, замещения, разложения и комплексообразования, а также электрохимические процессы.
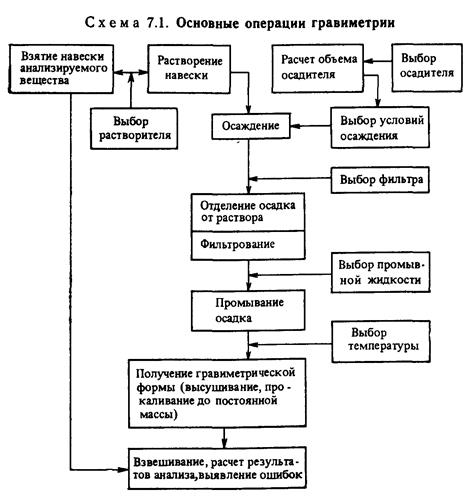
Наиболее распространен метод осаждения (схема), при котором навеску анализируемого вещества растворяют и прибавляют 1,5-кратный избыток реагента-осадителя, соблюдая необходимые условия осаждения. Полученный осадок называют осаждаемой формой. Соединение, в виде которого определяемый компонент осаждается из раствора, называется формой осаждения. Осадок отделяют от раствора (чаще всего фильтрованием), промывают, затем высушивают или прокаливают, получая гравиметрическую (весовую) форму. Соединение, в виде которого производят взвешивание, называют гравиметрической формой. Например, при осаждении сульфата формой осаждения является BaSO4, при осаждении железа (III) - соответствующий гидроксид Fе(ОН)3. При высушивании и прокаливании осадков могут происходить химические процессы, например
2Fе(ОН)3=Fе2О3+ЗН2О
Гравиметрическая форма по составу может отличаться от формы осаждения. В случае BaSО4 форма осаждения и гравиметрическая форма совпадают.
Массу определяемого компонента ma рассчитывают по формуле
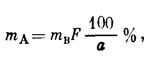
где mв - масса высушенного или прокаленного осадка, г; F - гравиметрический фактор, определяемый по химической формуле гравиметрической формы; a - навеска анализируемого вещества, г. Гравиметрические факторы, называемые также аналитическими множителями или факторами пересчета, вычисляют как отношение молекулярной массы определяемого компонента к молекулярной массе гравиметрической формы с учетом стехиометрических коэффициентов. Их значения обычно приводят в справочниках.
В ходе гравиметрического анализа определяемое вещество может отгоняется в виде какого-либо летучего соединения (метод отгонки). Методом отгонки определяют, например, содержание кристаллизационной воды в кристаллогидратах. Для определения содержания SiO2 часто используют реакцию с фтороводородной кислотой, в результате которой образуется летучий SiF4. Метод отгонки применяют также при анализе карбонатов, некоторых нитратов и других соединений, образующих летучие продукты реакции. Содержание анализируемого компонента определяют по изменению массы вещества в результате термической обработки или по увеличению массы поглотителя газообразных продуктов реакции.
Реагент-осадитель, осаждаемая и гравиметрическая формы должны отвечать определенным требованиям. Определяемый компонент должен осаждаться по возможности более полно, при этом остальные компоненты должны оставаться в растворе. Необходимо, чтобы осаждаемая форма легко и полностью превращалась в гравиметрическую, а последняя имела бы строго постоянный, точно известный химический состав и была бы устойчива на воздухе. Для уменьшения погрешностей анализа желательно, чтобы гравиметрическая форма имела возможно большую молярную массу, а содержание определяемого элемента в молекуле было меньшим. Эти требования могут быть выполнены путем правильного выбора реагента-осадителя, условий осаждения, фильтрования, промывания и прокаливания осадка.
Гравиметрический анализ - один из наиболее универсальных методов. Он применяется для определения почти любого элемента. В большей части гравиметрических методик используется прямое определение, когда из анализируемой смеси выделяется интересующий компонент, который взвешивается в виде индивидуального соединения.
Наиболее существенным достоинством гравиметрического метода является высокая точность анализа. Обычная погрешность гравиметрического определения составляет 0,1...0,2%. При анализе пробы сложного состава погрешность возрастает до нескольких процентов за счет несовершенства методов разделения и выделения анализируемого компонента. К числу достоинств гравиметрического метода относится также отсутствие каких-либо стандартизации или градуировок по стандартным образцам, необходимых почти в любом другом аналитическом методе. Для расчета результатов гравиметрического анализа требуется знание лишь молярных масс и стехиометрических соотношений.
Селективность гравиметрического анализа невысока в связи с отсутствием соответствующих реагентов на большинство ионов и, как правило, требуют предварительного химического разделения с целью выделения анализируемого компонента.
Существенным недостатком гравиметрического метода является длительность определений.
Чаще всего гравиметрический метод применяют для определения основных компонентов пробы, когда на выполнение анализа отводится несколько часов или десятков часов, для анализа эталонов, используемых в других методах, в арбитражном анализе.
Дата добавления: 2017-04-05; просмотров: 3030;











