Пиразол и его производные
Пиразол можно рассматривать как пиррол, в котором метиновая группа (–СН=) замещена атомом азота; отсюда и произошло название.
Пиразол получают конденсацией ацетилена с диазометаном по механизму синхронного циклоприсоединения с участием биполярной структуры диазометана:
 Н 4 3
Н 4 3













 НС СН2 НС СН HC CH
НС СН2 НС СН HC CH



 + 5
+ 5






 НС N HC N HC N2
НС N HC N HC N2
 | |||
 | |||
 N N N1
N N N1
H
Производные пиразола получают двумя общими методами:
1) конденсацией гидразина или его производных (например, алкил- или арилгидразинов) с β-дикетонами через гидразон и его последующую циклизацию:







 C H2 – C – CH3 CH – C – CH3 NH2
C H2 – C – CH3 CH – C – CH3 NH2


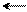

 H3C – C H3C – C + NH
H3C – C H3C – C + NH
O O OH O C6H5 –2H2O
ацетилацетон фенилгидразин







 HC C – CH3
HC C – CH3
 H3C – C N
H3C – C N
N
C6H5
3,5-диметил-1-фенилпиразол
2) взаимодействием гидразина с α, β-ацетиленовыми карбонильными соединениями:













 С – С – СН3 H2N HC CH – CH3
С – С – СН3 H2N HC CH – CH3
 C6H5 – C +
C6H5 – C +
O HNH –H2O C6H5 – C N
N
H
фенилацетилацетилен гидразин 3-метил-5-фенилпиразол
Пиразол – кристаллическое соединение (темп. пл. 700С). В парообразном состоянии пиразол мономерен, а в растворе ассоциирован, по-видимому, в результате образования межмолекулярных водородных связей. Эта связь благоприятствует таутомерным превращениям пиразола, что объясняет невозможность выделения в виде индивидуальных соединений изомерных 3- и 5-замещенных пиразола, например:

 СН3 СН3
СН3 СН3


















 H H
H H



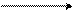


 N N N N
N N N N
 |  |  |







 N N N N
N N N N

 H H
H H
CH3 CH3
3-метилпиразол 5-метилпиразол
Пиразол, подобно пирролу, является слабым основанием и одновременно слабой кислотой.
Пиразол образует соли с металлами, превращаясь в анион, обладающий ароматическими свойствами:
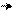






























 H+ KOH
H+ KOH
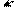




 K K
K K




 •• N •• N׃ –H2O N N
•• N •• N׃ –H2O N N
 N H N N N
N H N N N
H H
катион пиразола пиразол пиразол-калий
Пиразол устойчив в кислой среде, так как присоединение протона к неподеленной паре электронов азота (не содержащего водорода, а именно, в положении 2, потому что эта пара электронов находится вне кольца, в результате чего данный атом азота несет отрицательный заряд) не нарушает π-электронного секстета кольца.
Вследствие электроноакцепторного действия второго атома азота пиразол менее реакционноспособен, чем пиррол к реакциям электрофильного замещения, но также обладает многими свойствами ароматических соединений: он устойчив к различным химическим воздействиям, не изменяется при действии водного раствора перманганата калия, не полимеризуется.
Пиразол легко вступает в реакции электрофильного замещения в четвертое положение. Нитрование и сульфирование идет менее активно, по-видимому, из-за образования пиразолом солей с минеральными кислотами, которые с трудом подвергаются реакциям замещения:
 Br
Br

Br2
 N
N








 –HBr N
–HBr N
H
 •• N 4-бромпиразол
•• N 4-бромпиразол

 N HNO3 O2N
N HNO3 O2N






 H –H2O
H –H2O
пиразол
N
 N
N
H
4-нитропиразол
 Н2SO4 HO3S
Н2SO4 HO3S







 –H2O
–H2O
N
N
H
4-пиразолсульфокислота
Интересен кетон – 5-пиразолон, который существует в таутомерных кетонной и енольной формах:








 H2C CH HC CH
H2C CH HC CH



 O = C N HO – C N
O = C N HO – C N

 N N
N N
H H
5-пиразолон- кетонная форма 5-пиразолон- енольная форма
Из производных пиразолона в медицинской практике применяют антипирин, пирамидон, анальгин.
Антипирин или 2,3-диметил-1-фенил-5-пиразолон – бесцветное кристаллическое соединение, представляющее собой биполярный ион (I):


 (CH3)2N CH3 H3C
(CH3)2N CH3 H3C















 HC C – CH3 C C N CH3
HC C – CH3 C C N CH3










 NaO2SOH2C C C
NaO2SOH2C C C
O – C N – CH3 O = C N – CH3
 O = C N-CH3
O = C N-CH3

 N N
N N
C6H5 C6H5 N
C6H5
I II III
Пирамидон или 4-диметиламино-2,3-диметил-1-фенил-5-пиразолон – кристаллическое соединение горьковатого вкуса, является более эффективным лекарственным средством, чем антипирин, и обладает более продолжительным действием (II).
Анальгин или 2,3-диметил-1-фенил-5-пиразолон-4-метиламино-N-метиленсульфит натрия (III), является лучшим лекарственным препаратом среди соединений пиразолонового ряда. По интенсивности и быстроте действия он превосходит антипирин и пирамидон.
Дата добавления: 2017-01-16; просмотров: 3235;











