Структуры и действия.
НФ- группа а/б средств. К НФчувствительны грамм(+) и грамм(-)бактерии, а также хламидии и некот. простейшие (трихомонады, лямблии).

 НФ–группа ЛВ противомикробногодействия, в основе которых лежат структуры: →→→→→→→→
НФ–группа ЛВ противомикробногодействия, в основе которых лежат структуры: →→→→→→→→
СВЯЗЬ стру-ры и действия:
1.Наличие противомикробной активности
2.Различия активности в спектре действия
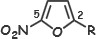
| Механизм действия:
-Нитрогруппа – акцептор кислорода. Нарушают процесс клеточного дыхания. Ингибируют различныеО-В ферменты.
-Под дейст-ем микробных флавопротеинов –NO2 восст-ется до продуктов, обладающих цитотоксическим действием.

|
| Спектр действия: грам(-) и грам(+) аэробные бактерии; патогенные грибы; простейшие. НЕАКТИВНЫ в отношении анаэробов и псевдомонад. |
 Нитрофурантоин:ИЮПАК: (E)-1-((5-нитро-2-
Нитрофурантоин:ИЮПАК: (E)-1-((5-нитро-2-
фуранил)метилен)амино-2,4- имидазолидиндион
Лек. форма: таблетки по 50 и 100 мг
Фуразолидон:ИЮПАК: 3-[[(5-нитро-2-
фурани)метилен]амино]- оксазолидин -2-он.
Лек. форма: таблетки по 50 мг Нифурател:
ИЮПАК: 5-[(метилтио)метил]-3-
{[(1E)-(5-нитро-2-
фурил)метилен]амино}-1,3- оксазолидин-2-он
Лек. форма: таблетки по 200 мг, крем вагинальный ( на 30г – 3г+1200000 ЕД); суппозитории вагинальные 500мн+200000 ЕД)
Нифуроксазид:
ИЮПАК: 1-(4-гидроксибензиол)-2-[(5-нитрофуран-2-ил)метилен]диазан Лек. форма: капсулы, таблетки (покрытые пленочной оболочкой) 100 и
200 мг; суспензия для приема внутрь 200 мг/5 мл
141. Нитроимидазолы: метронидазол, тинидазол, орнидазол. Производные 8-гидроксихинолина: нитроксолин, хлорхинальдол. Химическое строение. Связь структуры и действия.
 Нитроимидазолы. Группа противомикробных ЛВ, являющихся производными 2-
Нитроимидазолы. Группа противомикробных ЛВ, являющихся производными 2-
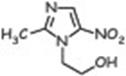
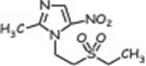
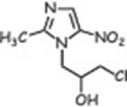
метил-5-нитроимидазола. Влияют на МО, восстанавливающие нитрогруппу (большинство анаэробов, многие простейшие). Образующиеся токсичные продукты нарушают репликацию ДНК, синтез белка, угнетают тканевое дыхание.
| Метронидазол | Тинидазол | Орнидазол |
|
|
|
Производные 8-гидроксихинолина
 Группа ЛВ, в основе которых лежит структура: 8-гидроксихинолин (8-хинолинол). Обладают антибактериальным, противогрибковым и противопаразитарным действие. Противомикробное действие обусловлено способностью образовывать хелаты с катионами металлов.
Группа ЛВ, в основе которых лежит структура: 8-гидроксихинолин (8-хинолинол). Обладают антибактериальным, противогрибковым и противопаразитарным действие. Противомикробное действие обусловлено способностью образовывать хелаты с катионами металлов.
Хинозол используется только наружно (растворы, присыпки, мази). У произв. 8- ГХ область применения зависит от особенностей фармакокинетики.
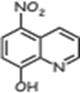
| Нитроксолин. Хорошо всасывается в ЖКТ и выводится с мочой в неизменённом виде. Концентрация в моче 100 мкг/мл и выше. Используется при бактериальных заболеваниях мочеполовых путей. |
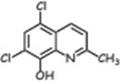
| Хлорхинальдол. Незначительно всасывается при приёме внутрь. Используется при: гинекологических заболеваниях (вагинальные таблетки); микробных и грибковых заболеваниях полости рта (таблетки для рассасывания). дизентерии, сальмонеллёзе, пищевых токсикоинфекциях (таблетки, гранулы); |
 |
142.  Фторхинолоны: ципрофлоксацина гидрохлорид, пефлоксацина мезилат, норфлоксацин, офлоксацин, левофлоксацин, ломефлоксацина гидрохлорид, моксифлоксацина гидрохлорид. Химическое строение. Связь структуры и действия.
Фторхинолоны: ципрофлоксацина гидрохлорид, пефлоксацина мезилат, норфлоксацин, офлоксацин, левофлоксацин, ломефлоксацина гидрохлорид, моксифлоксацина гидрохлорид. Химическое строение. Связь структуры и действия.
Фторхинолоны - группа ЛВ, обладают противомикробной активностью, применяющихся в качестве антибиотиков широкого спектра действия. Они не имеют природных аналогов. Механизм: Ингибируя два жизненно важных фермента микробной клетки - ДНК-гиразу (у Гр-) и топоизомеразу-4 (у Гр+), фторхинолоны нарушают синтез ДНК, что приводит к гибели бактерий (бактерицидный эффект). У человека аналогичные ферменты имеют другое строение и не катализируют процесс суперспирализации ДНК. Бактериальные топоизомеразы, являющиеся мишенью действия хинолонов, состоят из четырёх субъединиц: по две субъединицы А и B у ДНК-гиразы и по две субъединицы ParC и ParE у топоизомеразы
IV. Фторхинолоны I поколения и нефторированные хинолоны, взаимодействуют с ДНК- гиразой. Фторхинолоны II и III поколения большее с топоизомеразе IV, чем фторхинолоны I поколения. Фторхинолоны связываются с ДНК с образованием сложного комплекса (4 молекулы лекарственного вещества, молекула ДНК и ингибируемый фермент). Антибактериальная активность - влияние на РНК бактерий, на стабильность их мембран.
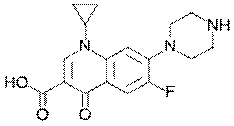
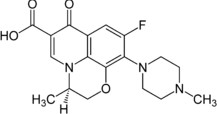
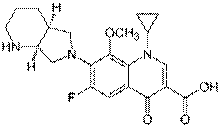
| Ципрофлоксацина гидрохлорид: | Офлоксацин: фторхинолон II поколения. | моксифлоксацина гидрохлорид: фторхинолон ІV |
| Антибактериальное широкого | Антибактериальная | поколения. Действует |
| спектра, бактерицидное, | активность - L-энантиомер. | бактерацидно |
| антибактериальное. | Инфекции дых. путей | (грамположительных и |
| Показания: Инфекции | (бронхит, пневмония), ЛОР- | грамотрицательных |
| мочевого тракта, нижних | органов (синусит, фарингит); | микроорганизмы, анаэробные, |
| дыхательных путей, кожи, | почек (пиелонефрит), | кислотоустойчивые и |
| костей и суставов, ЖКТ, | мочевыводящих путей | бактерии). Инфекции верхних |
| острые системные инфекции, | (цистит, уретрит), менингит, | и нижних дых. путей: острый |
| гинекологические, глазные | инфекционно-воспалит. | синусит, бронхит, пневмония; |
| инфекции, инфекции у | заболевания кожи, мягких | инфекции кожи и мягких |
| онкологических больных. | тканей, костей, суставов. | тканей. |
| 
| 
|
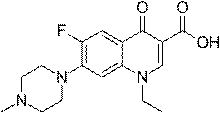
| пефлоксацина мезилат: | левофлоксацин: | норфлоксацин: II поколения |
| противомикробное действие. | фторхинолоны ІІІ поколения. | инфекционные заболевания |
| инфекции почек и | Представляет собой L- | мочевыводящих путей |
| мочевыводящих путей, ЖКТ, | энантиомер офлоксацина с | (уретрит, цистит); половых |
| желчного пузыря и | антибактериальной | органов: цервицит, |
| желчевыводящих путей | активностью вдвое | эндометрит;гонорея; |
| (холецистит, холангит), | большей, чем у | бактериальный гастроэнтерит |
| органов малого таза | офлоксацина. Инфекции | (сальмонеллёз); профилактика |
| (простатит); костей, суставов, | нижних дых. путей | рецидивов инфекций |
| кожи и мягких тканей, | (хронический бронхит, | мочевыводящих путей; |
| инфекции нижних дых. путей | пневмония), ЛОР-органов | профилактика диареи |
| и ЛОР-органов, глаз; гонорея, | (синусит, средний отит), | путешественников |
хламидиоз.
| мочевыводящих путей и почек (пиелонефрит), туберкулёз. | 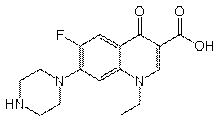
|
 - Это общая форма хинолонов. Хинолоны II поколения обладают широким спектром антимикробного действия и хорошо проникают в различные ткани и органы. Недостатком второго поколения является низкая активность против микроорганизмов, вызывающих пневмонии. Хинолоны III поколения называют
- Это общая форма хинолонов. Хинолоны II поколения обладают широким спектром антимикробного действия и хорошо проникают в различные ткани и органы. Недостатком второго поколения является низкая активность против микроорганизмов, вызывающих пневмонии. Хинолоны III поколения называют
«респираторными» (при пневмании). Хинолоны IV поколения - «респираторные» +
 |
«антианаэробными».
| Влияние на активность | |
| N(1) | Играет важную роль в проявлении антибактериальной активности. Замена на С, О, S приводит уменьшению активности. Оптимальным углеводородным остатком, связанным с N(1) является этильный или циклопропильный, могут присутствовать один или два атома F |
| С(2) | Не содержит заместителей. Введение в данное положение CH3 или SCH3 группы из-за стерического влияния дезактивирует молекулу фторхинолона |
| С(3) | В данном положении обязательно должна присутствовать карбоксильная группа.Замена такой группы на атом водорода, ацил, остатки гидроксамовой, уксусной, фосфоновой, сульфиновой, сульфоновой кислот и т.д. приводит к резкому снижению антибактериальной активности или полной её потере. |
| С(4) | Оксогруппа в 4-м положении является обязательной для связывания фторхинолонов с ферментом-мишенью.Замена данной группы на любую другую приводит к полному исчезновению антибактериальной активности. |
| С(5) | Различные заместители, связанные с данным атомом углерода могут уменьшать или увеличивать антибактериальную активность. Например, введение NH2-группы приводит к значительному повышению активности, а CH3NH-группы снижает её. |
| С(6) | Атом галогена (особенно фтора) в данном положении оказывает благоприятное действие на антибактериальную активность, но вовсе не обязателен для получения высокоактивных соединений. |
| С(7) | Практически все фторхинолоны содержат в 7 положении C-N связь. Большинство фторхинолонов содержат в 7 положении остатки 4 – 6 членных насыщенных азотсодержащих гетероциклов. Данные заместители необходимы для придания фторхинолонам амфотерных свойств и улучшения их фармакокинетики.При физиологических значениях рН лекарственное вещество будет существовать в виде цвиттер-иона и хорошо проникать в различные ткани и органы, а также в микробные клетки. |
| С(8) | Увеличивают активность атомы галогенов, метоксигруппа, а также замещение C(8) на атом азота. |
144. Противомалярийные средства: хинные алкалоиды (соли хинина), производные 4-аминохинолина (хлорохина фосфат, гидроксихлорохина сульфат). Химическое строение. Связь структуры и действия.
Противомалярийные средства– группа ЛС, используемых для
 этиотропного лечения и профилактики малярии. Малярия – группа трансмиссивных инфекционных заболеваний, вызываемых паразитическими простейшими рода Plasmodium и передаваемая человеку при укусах комаров рода Anopheles.
этиотропного лечения и профилактики малярии. Малярия – группа трансмиссивных инфекционных заболеваний, вызываемых паразитическими простейшими рода Plasmodium и передаваемая человеку при укусах комаров рода Anopheles.
Хинные алкалоиды– группа природных
соединений, свойственных определенным видам хинного дерева и ремиджии семейства мареновых. В их основе структура цинхонана (см. рис.).
Можно рассматривать как производные метанола.
Хинин обладает гематошизонтоцидным
д-ем.
Применяют при тропической малярии в случаях устойчивости малярийного плазмодия к хлорохину и др. ЛС.
Аминопроизводные хинолина.Выделяют 8-амино- (плазмохин, примохин) и
 4-аминопроизводные(хлорохина фосфат, гидроксихлорахина сульфат).
4-аминопроизводные(хлорохина фосфат, гидроксихлорахина сульфат).
Где Х–ОСН3 у 8-амино-, -Clу 4- аминопроизвадных.
Мех-м д-я:Малярийный плазмодий часть жизненного цикла проводит в эритроците, питается глобином. Гем накапливается в пораженном эритроците и при его разрыве высвобождается. Гем – сильный яд, который и вызывает лихорадку. Объект д-я 4-аминопроизводных и хинина – гематин (образуется из гема в пищеварительной вакуоли плазмодия).
Хлорохин образует π-комплекс с гематином и ингибирует образование гемозоина (малярийный пигмент).→ P uuʓ 6 ak6 6 u 6 k66ʁ # ʗ ʁ пищеварительной вакуоли и ингибирует фосфолипазы и образование пептидов у плазмодия.
Связь структуры и д-я:π-комплекс с гематином образуют только 2- и 4- аминопроизводные хинолина. В положении 7 – атом Сl или другой небольшой электроноакцепторный заместитель. Необходим для связывания с гематином. Третичные амины необходимы для накапливания в пищеварительной вакуоли.
Хлорохин и гидроксихлорохин связываются с нуклеиновыми кислотами и обладают цитотоксическим (иммунодепрессивным) действием. Используются для базисной терапии аутоиммунных заболеваний.
145. Противовирусные средства: антиретровирусные средства (зидовудин, ставудин, ламивудин); противогерпетические средства (ацикловир, ганцикловир, пенцикловир и их пролекарства); противогриппозные средства (осельтамивира фосфат, римантадина гидрохлорид), другие средства (арбидол, рибавирин).Вирус иммунодефицита человека (ВИЧ) относится к семейству ретровирусов, роду лентивирусов. Клетками-мишенями для данного вируса являются CD4+ лимфоциты, макрофаги и др. Средства, влияющие на ВИЧ: - ингибиторы проникновения ВИЧ в клетку-мишень; - ингибиторы обратной транскриптазы и др.; Ингибиторы обратной транскриптазы– группа антиретровирусных средств, которые связываются с вирусной ДНК и препятствуют завершению транскрипции либо непосредственно ингибируют фермент обратную транскриптазу.
В зависимости от химического строения выделяют две группы ингибиторов обратной транскриптазы: - нуклеозидные аналоги ингибиторов обратной транскриптазы; - ингибиторы обратной транскриптазы ненуклеозидной природы. Ингибиторы первой группы связываются с вирусной ДНК и препятствуют завершению транскрипции. Ингибиторы, относящиеся ко второй группе, связываются непосредственно с ферментом, нарушая его транскрипционную активность.
К группе нуклеозидных аналогов относятся производные пиримидин-2,4-диона (аналоги дТТФ), 4-амино-пиримидин-2-она (аналоги дЦТФ) и др. В состав молекул данных веществ входит остаток азотистого основания и углеводный остаток, модифицированный таким образом, чтобы в третьем положении в нём отсутствовала OH -группа. В процессе синтеза ДНК происходит присоединение нуклеотидов к её 3’-концу. Если в 3’-положении появляется другая группа, дальнейшее удлинение цепи ДНК становится невозможным и синтез заканчивается.
Первым ингибитором обратной транскриптазы нуклеозидной природы является зидовудин. Данное вещество синтезировано в качестве средства для лечения ВИЧ-инфекции и используется. У зидовудина OH-группа в 3’-положении заменена азидной. В клетке зидовудин превращается в трифосфат, который включается в 3’
-конец растущей цепи ДНК и прекращает её синтез. К ингибиторам обратной трансриптазы, содержащим в молекуле остаток цитидина, относятся также залцитабин и ставудин. У первого вещества в углеводной части молекулы в положениях 2’ и 3’ отсутствуют гидроксильные группы, у второго – кроме отсутствия данных групп имеется ещё и двойная связь. Ламивудин является производным 4-амино-пиримидин-2-она (аналог дЦТФ). В 3'-положении молекулы данного вещества содержится атом серы.
Все имеющие практическое применение противогерпетические средства
являются производными гуанина. Первым и наиболее широко применяющимся ЛС из данной группы является ацикловир, полученный при удалении группы –СH2
-CH(OH)- из остатка дезоксирибозы молекулы дезоксигуанозина. Активной формой ацикловира является трифосфорный эфир данного вещества. Процесс его образования включает три стадии, причём первая стадия – образование монофосфорного эфира катализируется только вирусной тимидинкиназой. Далее этот эфир с помощью киназ клетки-хозяина превращается последовательно в дифосфорный и трифосфорный эфиры. Трифосфат ацикловира включается вместо дезоксигуанозина в ДНК вируса и подавляет репликацию. Кроме того, он является конкурентным ингибитором ДНК-полимеразы. Ацикловир может применяться перорально, парентерально и местно. Молекула ацикловира
полярна, поэтому данное вещество обладает низкой биодоступностью при пероральном применении. Вследствие этого таблетки ацикловира принимают 5 раз в сутки.
Ацикловир высоко активен в отношении вирусов простого герпеса I и II типов, а также вируса ветряной оспы (опоясывающего герпеса). Он практически не влияет на цитомегаловирус. Этот тип вируса герпеса не содержит фермент, способный фосфорилировать ацикловир. Ганцикловир отличается от ацикловира гидроксиметильной группой. В отличие от ацикловира данное вещество способно превращаться в клетках, заражённых цитомегаловирусом, в активный трифосфорный эфир. Основное показание для применения ганцикловира – различные заболевания, вызванные цитомегаловирусом. Данное лекарственное вещество хорошо проникает в ЦНС. Ещё одним противогерпетическим средством
– производным гуанина – является пенцикловир. В молекуле данного лекарственного вещества содержится остаток 2-этилпропандиола-1,3. Пенцикловир обладает очень низкой биодоступностью при пероральном введении, поэтому применяется только наружно. Пролекарством пенцикловира является фамцикловир, представляющий собой диацетат исходного лекарственного вещества (биодоступность 75–80%). Форма выпуска фамцикловира – таблетки.
В настоящее время известно только две группы противогриппозных средств с доказанной эффективностью действия: - ингибиторы нейраминидазы; - блокаторы М2-каналов. Нейраминидаза и гемагглютинин являются поверхностными белками вируса гриппа. Роль гемагглютинина заключается в прикреплении вирусной частицы к поверхности клетки-хозяина. Нейраминидаза является ферментом и катализирует обратный процесс - отсоединение вируса от поверхности клетки хозяина.
При ингибировании нейраминидазы "новорождённый" вирион не сможет оторваться от поверхности клетки-хозяина, в которой он образовался, и инфицировать другую клетку.
В настоящее время в качестве лекарственных средств применяют два ингибитора нейраминидазы - занамивир и осельтамивир. Осельтамивир является пролекарством - сложным эфиром. Это вещество, в отличие от занамивира, вводится в организм пероральным путём. Форма выпуска осельтамивира - капсулы.
Блокаторы М2 каналов:М2-канал – протон-селективный белок-ионный канал, проходящий через липидную оболочку вируса А. Состоит из идентичных субъединиц. Активируется при уменьшении рН.Протоны проникают через М2- канал внутрь вириона. Это приводит к уменьшению рН внутри вируса и к отщеплению вирусного матричного белка М1 от рибонуклеопротеина («раздевание» вируса).
Блокаторы, M2-каналов являются аминопроизводными адамантана. Данные вещества способны "затыкать" M2-каналы, что нарушает процесс проникновения протонов через них и блокирует "раздевание" вируса. Блокаторы М2 каналов активны только в отношении вирусов гриппа А. Но большинство штаммов и этого вируса в настоящее время являются устойчивыми к действию производных адамантана, поэтому практическая ценность данных соединений как противогриппозных лекарственных средств невелика (Амантадин, Римантадин).
ДРУГИЕ ПРОТИВОВИРУСНЫЕ СРЕДСТВА
Рибавирин - гликозид D-рибозы с производным 1,2,4-триазола. Обладает
расширенным спектром противовирусного действия. Используется для лечения: гепатита С (совместно с пегиллированными интерферонами), заболеваний вызванных респираторным синцитиальным вирусом (эффективность не доказана), некоторых геморрагических лихорадок и др.
Механизм действия комплексный:
В организме рибавирин фосфорилируется с образованием моно-, ди- и трифосфатов –
РНК-вирусы. Моно-, ди- и трифосфаты рибавирина являются ингибиторами РНК- зависимых РНК-полимераз. Трифосфат включается в РНК и вызывает мутации в РНК- зависимой репликации вирусов.
ДНК-вирусы. Ингибирует клеточную дегидрогеназу монофосфата инозина и уменьшает концентрацию ГТФ внутри клетки.
Это как бы противовирусное средство (вирусы гриппа, парагриппа, аденовирусы). По данным разработчиков и производителей арбидол:
- подавляет процесс слияния липидной оболочки вируса с клеточными мембранами;
- является иммуномодулятором и индуктором интерферона.
146. Противогрибковые средства (ПГС): азолы (клотримазол, миконазола нитрат, кетоконазол, флуконазол); производные аллиламина (тербинафина гидрохлорид), противогрибковые антибиотики (гризеофульвин, нистатин). Химическое строение. Связь структуры и действия.
Азолы− группа ПГС, в молекулах которых содержатся остатки имидазола или 1,2,4- триазола.
 Классификация: производные имидазола(клотримазол, миконазол, кетоконазол) обладают высокой специфичностью и активностью (не зависящей от длительности их применения), широким спектром действия. Фунгистатики, легко проникают в роговой слой эпидермиса, низко токсичны для человека. Производные триазолов(флуконазол, итра-
Классификация: производные имидазола(клотримазол, миконазол, кетоконазол) обладают высокой специфичностью и активностью (не зависящей от длительности их применения), широким спектром действия. Фунгистатики, легко проникают в роговой слой эпидермиса, низко токсичны для человека. Производные триазолов(флуконазол, итра-
коназол) имеют более высокую противогрибковую активность, многие можно принимать внутрь. Механизм их действия окончательно не изучен. Производные тиокарбаминовой к-ты(абафунгин). Азолыингибируют цитохром Р450-зависимые ферменты, участвующие в синтезе эргостерина − компонента клеточной мембраны грибов (нарушение целостности клеточной мембраны грибов).
Аллиламины− группа ПГС, являющихся производными метил(1 - нафтилметил) аллиламина. Являются гидрохлоридами.
 Аллиламины ингибируют процесс синтеза эргостерина. В результате уменьшения содержания эргостерина изменяются свойства и нарушаются функции клеточной мембраны. Сквален в больших концентрациях сам по себе токсичен для грибов. Первый представитель аллиламинов нафтифин.
Аллиламины ингибируют процесс синтеза эргостерина. В результате уменьшения содержания эргостерина изменяются свойства и нарушаются функции клеточной мембраны. Сквален в больших концентрациях сам по себе токсичен для грибов. Первый представитель аллиламинов нафтифин.
Используется для лечения грибковых заболеваний кожи, ногтей и волос. Применяется только местно (при первом прохождении через печень подвергается интенсивному метаболизму). Тербинафинприменяется местно и перорально. При пероральном применении перераспределяется из плазмы крови в ногтевое ложе и накапливается в ногтевой пластинке. Используется для лечения онихомикозов и дерматомикозов.
Противогрибковые антибиотики: гризеофульвин− антибиотик, продуцируемый плесневым грибом Penicillium nigricans (griseofulvum). Производное бензофурана. Активен только (+)-энантиомер. Активен только при пероральном применении. Действует на активно растущие грибы. Влияет на процесс митоза в метафазе. Вызывает дезориентацию микротубул. Обладает фунгистатической активностью в отношении различных дерматофитов. Не действует на дрожжевые грибы.
Полиеновые антибиотики− группа АБ гликозидной природы, основу составляет лактонное кольцо, содержащее систему сопряжённых двойных связей. Число атомов в лактоном цикле: 26 (Натамицин), 38 (Нистатин,
Амсротерицин). Содержат в одной части кольца определённое количество -ОН групп и -СООН группу, в другой − сопряжённые двойные связи. Углеводная часть представлена микозамином-3-амино-3,6-дидезокси-β-D-маннопиранозой. Имеют «полярную головку» и «неполярный хвост». Обладают высоким сродством к эргостерин содержащим клеточной мембраны, могут непосредственно в них встраиваться. КМ становится более проницаемой, и клетка теряет ионы К+ и небольшие органические молекулы. Полиеныв малых концентрациях обладают фунгистатическим действием, в больших - фунгицидным. Нистатин− смесь полиеновых антибиотиков (нистатины Al, А2, A3). Основной компонент − нистатин А1.
147. Противоопухолевые средства: алкилирующие средства (мелфалан, циклофосфамид, комплексные соединения платины); природные соединения и противоопухолевые антибиотики (паклитаксел, доксорубицина гидрохлорид); антагонисты гормонов (флутамид, ципротерона ацетат, тамоксифена цитрат). Химическое строение. Связь структуры и действия.
Злокачественные новообразования (опухоли) – заболевания, характериз. появлением бесконтрольного деления клеток, способность к инвазии в прилежащие ткани и метастазированию в отдаленные органы.
Алкилирующие средства– ЛС, которые образуют ковалентные связи с ДНК, что препятствует делению клетки и запускает апоптоз.
Мелфалан– остаток азотистого иприта (R-N-(C2H4Cl)2) связан с остатком L- фенилаланина. Переносчик через КлетМембр. Бензольное кольцо уменьшает электр потенциал на атоме азота – уменьшение реакционной способности и токсичности. 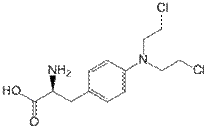 Циклофосфамид – является пролекарством.
Циклофосфамид – является пролекарством. 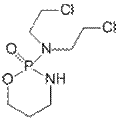 Комплексные соединения платины - Активен только цис-изомер. Транс-изомер токсичен и не обладает активностью (быстро разрушается). Попадает в пазму →ʁ
Комплексные соединения платины - Активен только цис-изомер. Транс-изомер токсичен и не обладает активностью (быстро разрушается). Попадает в пазму →ʁ
цитоплазму →ʁŒ 6a ʃ #ʁ # # #6 a 6 % u6u P →ʁ66ʖʏ # a u6Œa
репарации (устранение повреждений) ДНК→ k k# Œ. 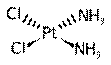
Таксаны– группа дитерпеноидных соединений, продуцируемыми растениями рода Tис. Природное соединение: паклитаксел. Противоопухолевое действие связано с влиянием на процесс митоза: стимулирует сборку микротрубочек из димеров тубулина и стабилизирует микротрубочки за счёт подавления деполимеризации, что приводит к подавлению нормального процесса динамической реорганизации сети микротрубочек; индуцирует образование аномальных скоплений или «связок» микротрубочек на протяжении клеточного цикла и вызывает образование множественных звёзд микротрубочек во время митоза. Используется для лечения рака МолочнЖелез, яичников, немелкоклеточного РакЛегких, саркомы Капоши.
Противоопухолевые антибиотики (ПОА)– группа природных соединений и их полусинтетических производных, блокирующих процесс транскрипции ДНК, вызывая точечные мутации в цепи ДНК и (или) ингибируя ферменты, необходимые для процесса репликации ДНК. Механизм действия ПОА: взаимодействие с молекулой ДНК – включение в молекулу ДНК между парами нуклеиновых оснований и прочное нековалентное взаимодействие с ними; ингибирование топоизомеразы II –– фермента, ответственного за поддержание нормальной структуры ДНК во время репликации и транскрипции; образование в процессе метаболизма цитотоксичных свободных радикалов, повреждающих молекулу ДНК.
Доксорубицина гидрохлорид - антроциклиновые антибиотики – группа
противоопухолевых антибиотиков гликозидной природы, содержащих в качестве агликона антрациклинон, а в качестве углеводного компонента – даунозамин. Механизм действия: включение молекулы между парами азотистых оснований; ингибирование топоизомеразы II; нарушение метаболизма железа; образование цитотоксичных свободных радикалов. Доксорубицин –– липофильное соединение накапливается в печени, лимфатических узлах, мышечной ткани, костном мозге, жировой ткани и коже. Выводится с калом. Исп. для лечения злокачественных
новообразований: гемобластозы, опухоли молочной железы, яичников, желчного
пузыря, щитовидной железы, саркомы и др. 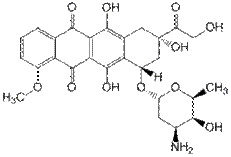
Антагонисты гормонов– группа противоопухолевых средств, нарушающих процесс образования гормонов в организме или препятствующих их взаимодействию с соответствующими рецепторами. Исп. Для лечения гормональнозависимых опухолей (молочные, предстателная железы и др).
Флутамид (нестероид стр-ра)и Ципротерона ацетат (стероиды) – антагонисты
андрогенов – соединения, способные конкурентно блокировать рецепторы андрогенов в андрогенчувствительных органах и тормозить проявления биологических эффектов эндогенных андрогенов. Используются для лечения рака предстательной железы (ПЖ). Ципротерона ацетат 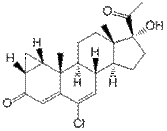 обладает гестагенным действием (появление и поддержание беременности) в малых дозах. В больших дозах обладает антиандрогенным действием - применяется для лечения рака ПЖ. Флутамид
обладает гестагенным действием (появление и поддержание беременности) в малых дозах. В больших дозах обладает антиандрогенным действием - применяется для лечения рака ПЖ. Флутамид 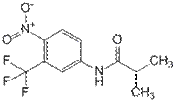 -конкурентно блокирует взаимодействие андрогенов с их клеточными рецепторами; препятствует проявлению биологических эффектов мужских половых гормонов в андрогенчувствительных тканях (например, клетках рака ПЖ). Используется для паллиативного лечения рака ПЖ с метастазами (облегчение состояния чел-ка).
-конкурентно блокирует взаимодействие андрогенов с их клеточными рецепторами; препятствует проявлению биологических эффектов мужских половых гормонов в андрогенчувствительных тканях (например, клетках рака ПЖ). Используется для паллиативного лечения рака ПЖ с метастазами (облегчение состояния чел-ка).
Тамоксифена цитрат – антиэстрогены –– группа ЛС, тормозящая процесс
образования эстрогенов, либо влияющие на процесс их взаимодействия с соответствующими рецепторами. Исп. для лечения рака молочной железы. Структура похожа на агонистов ЭстрогенРецептор нестероидной структуры – производные стильбена (С6Н5-СН=СН-С6Н5). Обладает высокой аффинностью по отношению к ЭР. Предотвращают транслокацию комплекса эстроген - рецептор в ядро клетки мишени, влияют на процесс связывания ЭРК с хроматином. 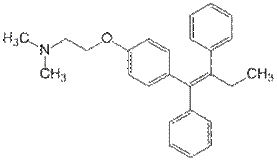
148. Противоопухолевые средства: антиметаболиты (фторурацил и его пролекарства, метотрексат, флударабина фосфат, меркаптопурин). Лекарственные средства, полученные при модификации структуры меркаптопурина: азатиоприн, аллопуринол. Химическое строение. Связь структуры и действия.
Фторурацил –аналоги пиримидиновых оснований.Противоопухолевое действие обусловлено их превращением в опухолевых клетках в активные ингибиторы ферментов – тимидилатсинтетазы. Активность фторурацила обусловлена его биотрансформацией в тканях в активные формы. Вводят в/в, имеет высокую токсичность.
Пролекарства фторурацила:1. Тегафур –фтористое производное пиримидина, который в организме гидролизуется с образованием фторурацила. Является менее токсичным соединением. 2. Капецитабин– производное фторпиримидина. Применяется перорально. В организме под влиянием тимидинфосфорилазы превращается в 5-фторурацил. Пролекарства перорально!
Метотрексат– является структурным аналогом и антагонистом фолиевой кислоты.
Ингибирует дигидрофолатредуктазу, тем самым подавляет синтез тимидиновой и инозиновой кислот, необходимых для образования ДНК.
Флударабина фосфат– ингибирует синтез ДНК. Взаимодействует рибонуклеотидредуктазой и ДНК-полимеразой. Применяется в виде флударабина фосфата, представляющий собой водорастворимый предшественник флударабина. Обладает цитотоксическим и иммуносупрессивным действием. Используется для лечения различных видов лейкозов.
Азатиоприн –получен при модификации 6-меркаптопурина (защита меркаптогруппы от гидролиза и окисления). По сравнению с меркаптопурином обладает более выраженным
Иммуносупрессивным действием и менее выраженным цитостатическим. Исп. Для лечения аутоиммунных заболеваний.
Аллопуринол –производное пиразолопиримидина. Ингибитор ксантиноксидазы, предотвращает переход гипоксантина в ксантин и образование из него мочевой кислоты. Гипоурекимическое средство (применяется при подагре).
 Фторурацил Флударабин Метотрексат
Фторурацил Флударабин Метотрексат
 |  |
Дата добавления: 2021-03-18; просмотров: 539;











