Ковалентной связью называется связывание атомов с помощью общих (поделенных между ними) электронных пар.
Рассмотрим связывание двух атомов хлора 17Cl (заряд ядра Z = 17) в двухатомную молекулу с позиций строения электронных оболочек хлора. Для этого запишем формулу Льюиса для атома хлора и конфигурацию его внешней электронной оболочки:

На внешнем электронном уровне хлора содержится s2 + p5 = 7 электронов. Поскольку электроны нижних уровней не принимают участия в химическом взаимодействии, точками мы обозначили только электроны внешнего, третьего уровня. Эти внешние электроны (7 штук) можно расположить в виде трех электронных пар и одного неспаренного электрона.
После объединения атомов в молекулу из двух неспаренных электронов атомов получается новая электронная пара:
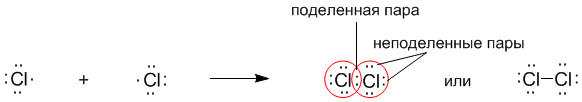
При этом каждый из атомов хлора оказывается в окружении ОКТЕТА электронов. В этом легко убедиться, если обвести кружком любой из атомов хлора.
Ковалентную связь образует только пара электронов, находящаяся между атомами. Она называется поделенной парой. Остальные пары электронов называют неподеленными парами. Они заполняют оболочки и не принимают участие в связывании.
Льюис не только предложил теорию ковалентной связи, но и первым сформулировал правило октета-дублета, которым мы уже пользовались в прошлой главе для объяснения устойчивости атомов. Это правило применительно к химическим связям можно сформулировать так:
Атомы образуют химические связи в результате обобществления такого количества электронов, чтобы приобрести электронную конфигурацию, подобную завершенной электронной конфигурации атомов благородных элементов.
Два атома водорода, объединившись в молекулу, приобрели “завершенную” молекулярную оболочку, подобную завершенной электронной оболочке атома благородного газа гелия (1s2). Атомы хлора в молекуле приобрели молекулярную оболочку, похожую на завершенную оболочку атома аргона (...3s23p6).
Познакомимся теперь с ионной связью. Как ни удивительно, она ничем принципиально не отличается от ковалентной связи. Движущей силой ее образования является все то же стремление атомов к октетной оболочке. Но в ряде случаев такая “октетная” оболочка может возникнуть только при передаче электронов от одного атома к другому. Поэтому ионная связь, в отличие от ковалентной, возникает только между атомами разного вида.
Рассмотрим конкретный пример: реакцию между атомами натрия (Z = 11) и фтора (Z = 9). При образовании связи между ними оба элемента приобретают внешнюю электронную оболочку благородного газа неона (Z = 10). Для того, чтобы убедиться в этом, надо записать электронные формулы всех трех элементов:
Na: 1s2 2s2 2p6 3s1
F: 1s2 2s22p5
Ne: 1s2 2s22p6
В электронных формулах нам важны только электронные конфигурации внешних уровней (они подчеркнуты). Запишем реакцию с помощью формул Льюиса:
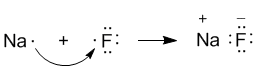
Натрий, отдав фтору свой 3s1-электрон, становится ионом Na+ и остается с заполненной 2s22p6 оболочкой, что отвечает электронной конфигурации атома неона. Точно такую же электронную конфигурацию приобретает атом F, приняв один электрон, отданный натрием. Теперь это ион F-. Разумеется, при этом ионы F- и Na+ продолжают оставаться все теми же элементами фтором и натрием, потому что никакие электронные переходы не могут изменить природу элемента - число протонов в его ядре.
Теперь в дополнение к ковалентной составляющей химической связи в молекуле Na+:F- добавляется еще и электростатическое притяжение между ионами натрия и фтора. Это увеличивает прочность химической связи. Однако ковалентная составляющая (стремление к октету) продолжает играть большую роль и в ионных соединениях.
Полярная ковалентная связьзанимает промежуточное положение между чисто ковалентной связью и ионной связью. Так же, как и ионная, она может возникнуть между двумя атомами разных видов. В полярной ковалентной связи электроны смещаются от атома к атому не так сильно, как в ионной. Это происходит тогда, когда атомам энергетически невыгодно далеко “отпускать” свои собственные электроны, отданные в общую “копилку” - молекулярную орбиталь. Если электроны слишком далеко сдвинутся к одному из атомов, молекулярная орбиталь перестанет быть похожей на “октетную”. В то же время у разных атомов разные донорные и акцепторные свойства, поэтому связывающая электронная пара не располагается точно посередине между ядрами, как в ковалентной связи.
В качестве примера рассмотрим образование воды в реакции между атомами водорода (Z = 1) и кислорода (Z = 8). Для этого удобно сначала записать электронные формулы для внешних оболочек водорода (1s1) и кислорода (...2s2 2p4). Затем на помощь приходят формулы Льюиса, которые наглядно показывают, как образуются “завершенные” электронные оболочки рядом с атомами водорода и кислорода в молекуле воды:
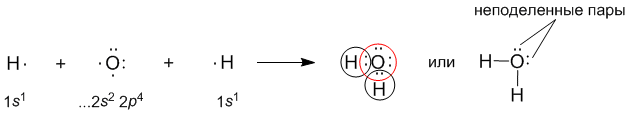
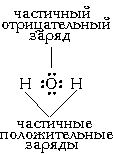
Оказывается, для этого необходимо взять именно два атома водорода на один атом кислорода. Однако природа такова, что акцепторные свойства атома кислорода выше, чем у атома водорода (о причинах этого чуть позже). Поэтому связывающие электронные пары в формуле Льюиса для воды слегка смещены к ядру атома кислорода. Связь в молекуле воды - полярная ковалентная, а на атомах появляются частичные положительные и отрицательные заряды.
О том, как предсказать акцепторные свойства атомов и где проходит “граница” между полярной ковалентной и ионной связями мы поговорим в параграфе 3.4.
По теории Льюиса и правилу октета связь между атомами может осуществляться не обязательно одной, но и двумя и даже тремяподеленными парами, если этого требует правило октета. Такие связи называются двойными и тройными. Например, только что рассмотренный нами кислород может образовывать двухатомную молекулу с октетом электронов у каждого атома только тогда, когда между атомами помещаются две поделенные пары:
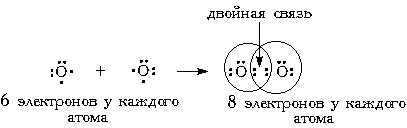
** В специальной главе, посвященной элементу кислороду, мы еще раз вернемся к вопросу о том, как правильно изображать связь в его молекуле. А пока (в первом приближении) можно остановиться на приведенной выше формуле с двойной связью.
Атомы азота (...2s2 2p3 на последней оболочке) также связываются в двухатомную молекулу, но для организации октета электронов им требуется расположить между собой уже три поделенные пары:
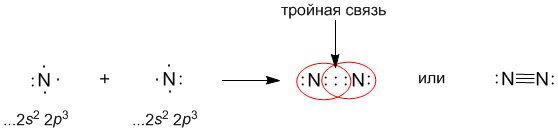
В настоящее время принято изображать электронные пары (то есть химические связи) между атомами черточками. Каждая черточка - это поделенная пара электронов. В этом случае уже знакомые нам молекулы выглядят так:

Формулы с черточками между атомами называются структурными формулами. Чаще в структурных формулах не изображают неподеленные пары электронов, но в ряде случаев (мы столкнемся с ними при обсуждении донорно-акцепторных связей) неподеленные пары играют важную роль.
Структурные формулы очень хороши для изображения молекул: они четко показывают - как атомы связаны между собой, в каком порядке, какими связями.
Дата добавления: 2016-11-04; просмотров: 2496;











