Связывающая пара электронов в формулах Льюиса - то же самое, что одна черточка в структурных формулах.
Двойные и тройные связи имеют общее название - кратные связи. О молекуле азота говорят, что она имеет порядок связи, равный трем. В молекуле кислорода порядок связи равен двум. Порядок связи в молекулах водорода и хлора - один. У водорода и хлора уже не кратная, а простая связь.
Порядок связи - это число обобществленных поделенных пар между двумя связанными атомами. Порядок связи выше трех не встречается.
Таблица 3-1. Длины и прочности связей между атомами азота в различных соединениях.
| Связь | Длина связи в ангстремах 1А = 10-8см | Прочность связи в кДж на одинаковое число молекул |
| Проcтая N–N | 1,45 | 58,5 |
| Двойная N=N | 1,25 | |
Тройная
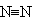
| 1.098 |
** Рассмотрим данные по длинам и прочностям связей между атомами азота в различных его соединениях. В таблице 3-1 длины связей приведены в специальных единицах - ангстремах (1А = 10-8см). Относительную прочность связей можно оценить по энергии, которая необходима для разрыва связей между атомами азота в разных соединениях. Эта энергия дается для одинакового числа молекул таких соединений. Чем выше кратность связи, тем она короче и прочнее.
Чем выше порядок связи, тем прочнее связаны между собой атомы и тем короче сама связь.
Задачи.
3.1. Исходя из строения атомов 6C, 1H и правила октета, составьте формулу Льюиса для соединения этих двух элементов, в составе которого 1 атом углерода. Нарисуйте для него структурную формулу.
3.2. Напишите (с указанием величины и знака заряда) символы ионов натрия, кислорода, фтора, магния, алюминия, электронные оболочки которых такие же, как у благородного газа неона.
3.3. Напишите электронные формулы внешних электронных уровней атомов 13Al и 17Cl. Один атом алюминия и три атома хлора дают соединение, в котором атомы этих элементов приобретают завершенные оболочки инертных газов. Какие это инертные газы? Напишите формулу Льюиса соединения между алюминием и хлором. Нарисуйте для него структурную формулу.
3.4.Составьте формулу Льюиса для соединения, включающего один атом 20Ca и два атома 9F. Сколько связывающих (поделенных) и несвязывающих (неподеленных) электронных пар в этом соединении? Какова его структурная формула?
3.5. Исхода из электронного строения атомов и правила октета, составьте формулы Льюиса для соединений, состоящих: а) из двух атомов 6C и четырех атомов 1H; б) из двух атомов 6C и двух атомов 1H. Каковы кратности связей между атомами углерода в этих двух соедиениях? Нарисуйте их структурные формулы (первое из них называется этилен, второе - ацетилен).
3.6. По структурным формулам составьте формулы Льюиса с указанием всех неподеленных электронных пар:

Дата добавления: 2016-11-04; просмотров: 2397;











