Уравнение Шредингера.
Основной характеристикой состояния атомов, молекул, элементарных частиц является y-функция. Аналитическое выражение y-функции в каждом конкретном случае можно получить путем решения волнового уравнения – основного уравнения квантовой механики, предложенного Э. Шредингерам в 1920 г.
Применительно к стационарным состояниям уравнение Шредингера имеет вид:
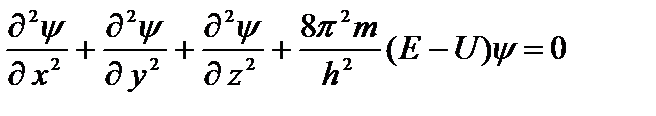 . (4.1)
. (4.1)
где т – масса частицы; Е и U – ее полная и потенциальная энергии.
Если частица перемещается только вдоль некоторой линии, например, вдоль оси ОХ (одномерный случай), то уравнение Шрёдингера упрощается и принимает вид:
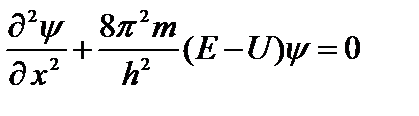 (4.2)
(4.2)
Одним из наиболее простых примеров использования уравнения Шрёдингера является решение задачи о движении частицы в одномерной потенциальной яме.
Пусть электрон перемещается вдоль оси ОХ только в пределах 0<х<l (рис. 4.1). Это означает, что в указанном интервале y-функция отлична от нуля, а вне интервала (х < 0, х³ l) равна нулю.
Так как на частицу в выделенном интервале силовые поля не действуют, то ее потенциальная энергия может иметь любое постоянное значение (наиболее удобно принять U=0). Вне этого интервала электрона нет, поэтому следует считать его потенциальную энергию бесконечно большой. На рис. 4.1 показана графическая зависимость U = f(x). Интервал 0<х<l, удовлетворяющий сформулированным выше условиям, называют одномерной прямоугольной потенциальной ямой с бесконечно высокими стенками. С учетом U=0 уравнение Шрёдингера (4.2) для интервала 0<х<l имеет вид:
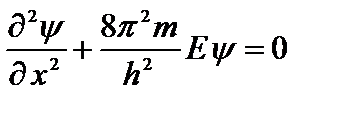 . (4.3)
. (4.3)
Введем обозначение: 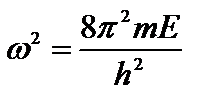 , (4.4)
, (4.4)
тогда: 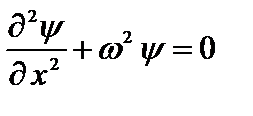 (4.5)
(4.5)
Это уравнение аналогично дифференциальному уравнению гармонического колебания, решение которого:
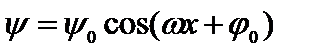 , (4.10)
, (4.10)
где 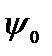 –амплитуда волновой функции,
–амплитуда волновой функции, 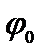 –ее начальная фаза. Чтобы найти две постоянные
–ее начальная фаза. Чтобы найти две постоянные 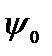 и
и 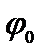 , а также возможные значения
, а также возможные значения 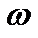 или Е, рассмотрим граничные условия:
или Е, рассмотрим граничные условия:
1) при х =0 y = 0. Подставляя эти значения в (4.10), получаем
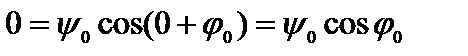
Физический смысл здесь имеет только одно значение: 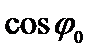 = 0, откуда
= 0, откуда 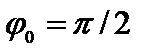 .
.
2) при х =l y = 0. C учетом 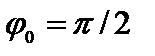 из (4.10) имеем:
из (4.10) имеем:
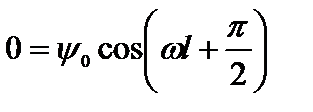
Физический смысл здесь имеет только одно значение:
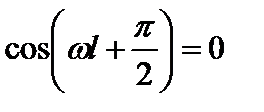 , или
, или 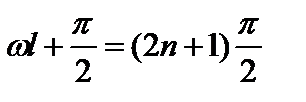 , откуда
, откуда
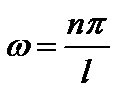 , (4.7)
, (4.7)
где п – целое число, оно принимает значения 1, 2, 3, ...; п ≠ 0, так как в противном случае y= 0 при любом х, что означает отсутствие электрона в потенциальной яме. Число n называют квантовым числом. Из (4.4) находим энергию 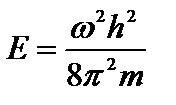 , что с учетом (4.7) дает:
, что с учетом (4.7) дает:
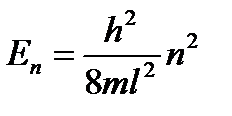 . (4.8)
. (4.8)
Индекс n при Е показывает, что различным значениям квантового числа n соответствует и разная энергия.
Подставляя w (4.7) в (4.5) и учитывая 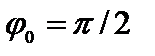 , получаем
, получаем
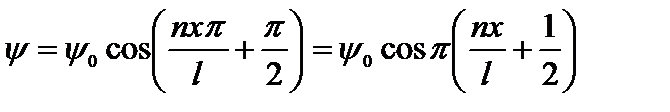 . (4.9)
. (4.9)
Из (4.8) следует, что решение уравнения Шредингера для электрона в потенциальной яме без каких-либо дополнительных постулатов приводит к дискретным, квантованным значениям энергии:
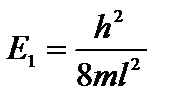 ;
; 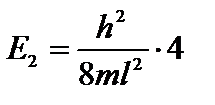 и т.д.
и т.д.
Возведя (4.9) в квадрат, получим плотность вероятности 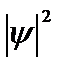 нахождения электрона в разных точках потенциальной ямы. На рис.4.2. показана графическая зависимость
нахождения электрона в разных точках потенциальной ямы. На рис.4.2. показана графическая зависимость 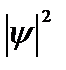 от х при разных дискретных состояниях, то есть разных квантовых числах. Как видно из рисунка, электрон может с разной с разной вероятностью находиться в разных местах потенциальной ямы. Есть такие точки, в которых вероятность нахождения электрона вообще равна нулю. Это существенно отличается от представлений классической физики, согласно которым равновероятно нахождение частицы в разных местах потенциальной ямы
от х при разных дискретных состояниях, то есть разных квантовых числах. Как видно из рисунка, электрон может с разной с разной вероятностью находиться в разных местах потенциальной ямы. Есть такие точки, в которых вероятность нахождения электрона вообще равна нулю. Это существенно отличается от представлений классической физики, согласно которым равновероятно нахождение частицы в разных местах потенциальной ямы
Дата добавления: 2016-10-26; просмотров: 1624;











