Системы производства азотной кислоты.
ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ ПРОИЗВОДСТВА НЕКОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ
Производство NN03 при атмосферном давлении.
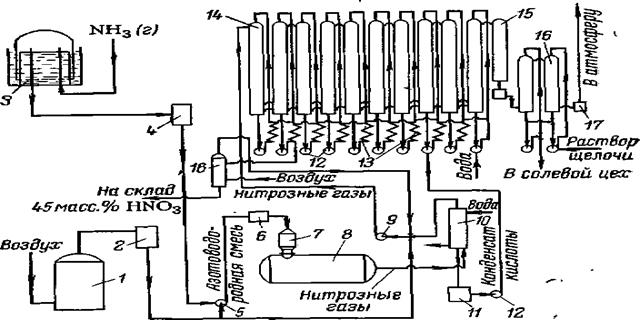
Технологическая схема производства азотной кислоты при атмосферном давлении показана на рис.1.
Воздух, загрязненный пылью и кислыми газами, очищается в скруббере орошаемом водой или щелочным раствором; от пыли он очищается в рукавном фильтре 2.
Газообразный аммиак фильтруют через матерчатые фильтры или промывают жидким аммиаком от паров масла и механических примесей (катализаторной пыли из колонн синтеза аммиака). После очистки аммиак и воздух смешиваются в вентиляторе 5 с образованием аммиачно-воздушной смеси, содержащей 10,5—11,5 объемн. % аммиака. Смесь через картонный фильтр поступает в контактный аппарат 7. Здесь на платиновых сетках при 750—850 °С протекает окисление NН3 до оксида азота. Газы, содержащие N0, 02, N2 и водяные пары, а также
также
 | |||
|
NH3, не окислившийся в N0, поступают далее в котел-утилизатор 8, где охлаждаются до температуры 160—170°С. При этом образуется пар давлением до 4 МПа и температуре450 °С. Затем, пройдя холодильник 10 и сборник кислого конденсата 11, нитрозные газы при 40 °С вентилятором9 подают на абсорбцию в систему, состоящую из 6—8 абсорбционных башен 14из нержавеющей стали. Башни содержат насадку в виде колец Рашига и расположены последовательно одна другой.
В холодильнике 10 при охлаждении газа происходит частное окисление N0 в ,N02 и образование кислого конденсата содержащего 2—3 масс. % NО3, а в холодильнике 11 — конденсата, содержащего 25—30% НNO3. Конденсат насосом подают в башню 14, где протекают два процесса — окисле N0 в N02 и поглощение N02 водой с образованием азот кислоты. Поглощение оксидов азота осуществляется по принципу противотока, причем в последнюю башню подается вода, а остальные башни орошаются кислотой соответствующей концентрации. Образующаяся в последней башне очень разбавленная кислота перетекает из башни в башню и, встречая более концентрированные нитрозные газы, поглощает их. При этом ее концентрация достигает 45—48 масс. %
Окисление N0 в N02 и поглощение N02 водой протекает с выделением тепла , поэтому кислоту, орошающую башни, охлаждают в кислотных холодильниках 13. Для подачи кислоты на орошение башен служат центробежные насосы 12.
Продукционная 45—48%-ная кислота, как правило, выдается из второй абсорбционной башни и содержит растворенные оксиды, для удаления которых ее нагревают до 50—55 °С и продувают воздухом в отбелочной башне 18. Выделившиеся оксиды азота возвращают в абсорбционную систему. Поскольку абсорбционная система обеспечивает поглощение N02 только на 92—94%, нитрозные газы поступают далее в две последовательно установленные насадочные башни, орошаемые нитрит - нитратными растворами натрия или кальция. В результате общая степень поглощения оксидов азота составляет 96—97%, а содержание их в выхлопных газах равно 0,2—0,1 объемн. %. Производительность системы, работающей при атмосферном давлении до 250 тыс. т/год HN03.
Комбинированная схема производства.
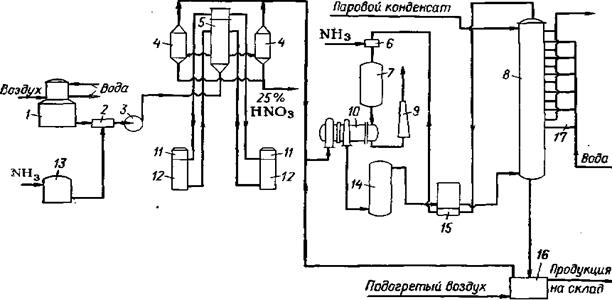
На рис. 2 приведена технологическая схема получения 45—50%-ной кислоты комбинированным методом производительностью 45 тыс. т/год. Комбинированная схема производства неконцентрированной азотной кислоты основана на окислении аммиака, проводимом при атмосферном давлении, и на абсорбции оксидов азота, осуществляемой под давлением 3,5*105 Па.
 | |||
|
Первая такая система была пущена в СССР в /1959 г. и выгодно отличалась от подобных систем, работающих в Западной Европе: высокой степенью конверсии, низким расходом платиноидного катализатора 0,047 г/т НN03 и 0,028—0,032 г/т НNO3 для двухступенчатого катализатора и простотой управления процессом.
Воздух предварительно очищают от вредных примесей, "отравляющих платиновый катализатор (SО3, SО3, Н3Р и др.), и от пыли.
Аммиачно-воздушная смесь, содержащая 10—11 объемн. % NН3 подается в теплообменник, где нагревается до 90—100 °С нитрозными газами, поступающими из котла-утилизатора 12. В картонном фильтре, расположенном в верхней части контактного аппарата[1], подогретая аммиачно-воздушная смесь проходит дополнительную тонкую очистку, и поступает в контактный аппарат 11. Здесь при атмосферном давлении и температуре 800—840 °С аммиак окисляется с образованием N0 и паров воды. Для использования тепла реакции окисления аммиака нитрозные газы проходят котел-утилизатор 12, где образуется пар с температурой 450 °С и давлением 3,8—4 МПа, в результате чего температура нитрозного газа снижается до 170 °С. Далее нитрозный газ охлаждается в теплообменнике 5, отдавая тепло аммиачно-воздушной смеси. При температуре 110—120°С нитрозный газ поступает в холодильники-промыватели барботажного типа 4, где одновременно с охлаждением нитрозных газов происходит конденсация водяных паров. Помимо образования воды в результате окисления NН3 водяные пары вносятся также в систему с воздухом, поступающим на окисление аммиака.
Одновременно с охлаждением газа в холодильнике-промывателе происходит частичное окисление N0 в N02 с образованием 25—30%-ной азотной кислоты, так называемого конденсата азотной кислоты. Нитрозные газы, поступающие в нижнюю часть холодильника 4, проходят слой образующегося конденсата НNO3 и отмываются от нитрит-нитратных солей аммония, образующихся в результате проскока аммиака в нитрозный газ. После холодильников-промывателей 4нитрозные газы сжимаются в турбокомпрессоре 10 до (3,2—3,4) * 105 Па и направляются на окисление в полую башню 14. В результате окисления N0 до N02 нитрозные газы нагреваются от 110—120 до 320 °С. Выделившееся тепло реакции окисления используется для нагревания хвостовых нитрозных газов после абсорбционной колонны, направляемых на каталитическое восстановление до N2. После окислительного объема нитрозные газы охлаждаются от 320 до 35—37 °С в теплообменнике 15 и поступают вниз абсорбционной колонне 8.
Для орошения абсорбционной колонны на верхнюю тарелку подают паровой конденсат. Концентрация образующейся азотной кислоты по мере перетекания с тарелки на тарелку постепенно увеличивается за счет поглощения оксидов азота, идущих ей навстречу. На выходе из абсорбера кислота должна содержать не менее 47—50 масс. % НNO3. Азотнокислый конденсат из холодильника-промывателя с содержанием 25— 30 масс. % НNO3 поступает на одну из тарелок абсорбционной колонны, где находится кислота такой концентрации.
Продукционная кислота по выходе из абсорбера содержит растворенные оксиды азота, которые удаляются из нее в отбелочной башне 16 при пропускании воздуха. Отбеленная кислота поступает на склад самотеком. Выделившиеся при отбеливании азотной кислоты нитрозные газы направляются в компрессор.
Хвостовые газы, содержащие не более 0,16 объемн. % оксидов азота, нагреваются в теплообменнике 15до 260—280 °С, смешиваются с аммиаком и поступают в реактор 7, где на катализаторе АВК-10 происходит восстановление оксидов до элементарного азота по реакциям:
4 NН3 + 6 NО = 5 N2 + 6Н2О + Q
8 NН3 + 6 NО2 = 7 N2 + 12Н2О + Q
В соответствии с нормами технологического режима производства азотной кислоты комбинированным методом предусмотрено содержание в хвостовых газах 3—5 объемн. % кислорода для окисления избыточного аммиака (подаваемого в хвостовые газы для каталитического восстановления оксидов азота):
4 NН3 + 3О2 = 2N2 + 6Н20
Хвостовые газы, содержащие не более 0,01 объемн. % оксидов азота после каталитической очистки при 250—290 °С, поступают в газовую турбину, совмещенную на одном валу с турбокомпрессором. После расширения нитрозные газы, содержащие 0,008 объемн. % оксидов азота, под давлением (1,02— 1,03) • 105 Па выбрасываются в атмосферу через трубу высотой 100 м.
Дата добавления: 2016-10-26; просмотров: 4053;











