Реакции метаболической трансформации
Окисление
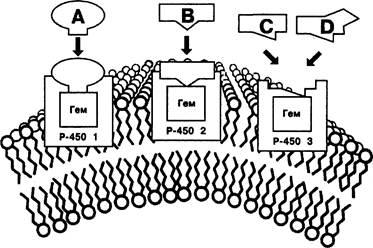
В ЭПР функционируют НАДФ•Н- и НАД•Н-зависимые дыхательные цепи. В НАДФ•Н-зависимой системе терминальным переносчиком электронов является цитохром Р-450 — мембраносвязанный липофильный фермент группы многоцелевых монооксигеназ[2], гемопротеин, состоящий из белка и системы порфирина с трехвалентным железом. буква Р в названии происходит от слова пигмент, число 450 означает, что восстановленный, связанный с окисью углерода цитохром максимально поглощает свет с длиной волны 450 нм.
Цитохром Р-450 глубоко погружен в липидный бислой мембраны ЭПР и функционирует совместно с НАДФ•Н-зависимой цитохром Р-450-редуктазой (коферменты — флавинадениндинуклеотид и флавинаденин-мононуклеотид). Соотношение количества молекул цитохрома Р-450 и редуктазы составляет 10:1. Активный центр этих ферментов ориентирован на цитоплазматическую поверхность ЭПР. Цикл окисления лекарственных средств при участии цитохрома Р-450 состоит из следующих реакций (рис. 1):
· окисленный цитохром Р-450 присоединяет лекарственное средство;
· бинарный комплекс цитохром — лекарство восстанавливается цитохром Р-450-редуктазой, используя электрон НАДФ•Н;
· восстановленный комплекс цитохром Р-450 — лекарство связывается с молекулярным (триплетным) кислородом;
· происходит активация кислорода электроном НАДФ•Н (триплетный кислород становится синглетным);
· на финальном этапе один атом кислорода включается в молекулу окисляемого лекарственного средства, второй — включается в молекулу воды;
· 
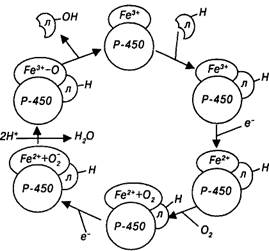 цитохром Р-450 регенерирует в исходную окисленную форму.
цитохром Р-450 регенерирует в исходную окисленную форму.
 |
 НАД•Н-зависимая электрон-транспортная цепь включает цитохром b5, НАД•Н-цитохром b5-редуктазу и стероид-КоА-десатуразу. Гемсодержащий фермент цитохром b5представляет собой двухдоменный белок. Глобулярный цитозольный домен связывается с редуктазой, короткая спирализованная гидрофобная цепь погружена в мембрану ЭПР. Электроны от НАД•Н переносятся редуктазой на окисленное железо цитохрома bs. Стероил-КоА-десатураза катализирует образование двойных связей в жирных кислотах.
НАД•Н-зависимая электрон-транспортная цепь включает цитохром b5, НАД•Н-цитохром b5-редуктазу и стероид-КоА-десатуразу. Гемсодержащий фермент цитохром b5представляет собой двухдоменный белок. Глобулярный цитозольный домен связывается с редуктазой, короткая спирализованная гидрофобная цепь погружена в мембрану ЭПР. Электроны от НАД•Н переносятся редуктазой на окисленное железо цитохрома bs. Стероил-КоА-десатураза катализирует образование двойных связей в жирных кислотах.
Суперсемейство цитохромов Р-450 поражает своими почти неограниченными метаболическими возможностями. Оно включает более 1000 клонированных вариантов, способных катализировать около 60 типов энзиматических реакций с тысячами потенциальных субстратов. В клетках человека обнаружено 17 семейств цитохрома Р-450, разделенных на 39 подсемейств. Изоферменты обозначаются следующим образом: первая цифра обозначает семейство, затем латинская буква указывает на подсемейство, последняя цифра соответствует конкретному изоферменту. В молекулах изоферментов одного семейства идентичны более 40 % аминокислот, в молекулах одного подсемейства — более 55 %.
Метод фенотипирования позволяет установить субстратную специфичность изоферментов цитохрома Р-450 по соотношению концентраций неизмененного вещества и его метаболитов в крови. Методом генотипирования с помощью полимеразной цепной реакции (ПЦР) изоферменты идентифицируют по их генам, так как каждый изофермент кодируется одним из 53 генов, локализованных в разных локусах хромосом. Большинство реакций катализируют изоферменты цитохрома Р-450 семейств 1, 2 и 3 (рис. 2, табл. 7).
Реакция окисления ксенобиотиков при участии цитохрома Р-450 расщепляется с образованием свободных радикалов кислорода и токсических промежуточных продуктов (эпоксиды, N-, S-окиси, альдегиды). свободные радикалы и активные интермедиаты, инициируя перекисное окисление мембранных липидов, вызывают некроз клеток, появление неоантигенов, тератогенный, эмбриотоксический эффекты, мутации, канцерогенез и ускорение старения. По этой причине не существует абсолютно безвредных ксенобиотиков.
Таблица 7.Содержание изоферментов цитохрома Р-450 в печени человека, их вклад в окисление лекарственных средств, локализация в хромосомах, индукторы и ингибиторы
| Изоферменты цитохрома Р-450 | Содержание в печени, % | Вклад в окисление, % | Локус в хромосоме (первая цифра — номер хромосомы) | Индукторы | Ингибиторы | |
| 1А1 | <1 | 2,5 | 15q22-q24 | Полициклические ароматические углеводороды (в легких преобразуются в канцерогенные метаболиты) | ||
| 1А2 | 8,2 | 15q22-qter | Фенобарбитал, гексамидин, дифенин, рифампицин, полициклические ароматические углеводороды, никотин | Амитриптилин, имипрамин, такрин, мексилетин, верапамил, дилтиазем, тиклопидин, эритромицин, кларитромицин, фторхинолоны (ципрофлоксацин, норфлоксацин, эноксацин), препараты интерферона, фурацилин | ||
| 1В1 | <1 | Не установлен | 2q22-q22 | |||
| 2А6 | 2,5 | 19q13.2 | Фенобарбитал | Ритонавир | ||
| 2В6 | <1 | 3,4 | 19q13.2 | Фенобарбитал, гексамидин, дифенин | Орфенандрин | |
| 2С8 | Не установлено | Не установлен | 10q24.1 | Фенобарбитал, гексамидин | ||
| 2С9 | 15,8 | 10q24.1-24.3 | Дифенин, рифампицин | Бутадион, диклофенак, кетопрофен, амиодарон, флувастатин, зафирлукаст, тетурам, сульфаметоксазол, дапсон | ||
| 2С18 | Не установлено | Не установлен | Локус в хромосоме 10 | Циметидин | ||
| 2С19 | 8,3 | 10q24.1-24.3 | Фенобарбитал, гексамидин, дифенин, рифампицин | Имипрамин, флувоксамин, флуоксетин, омепразол | ||
| 2D6 | 2,5 | 18,8 | 22q13.1 | Тиоридазин, галоперидол, имипрамин, кломипрамин, флувоксамин, флуоксетин, пароксетин, сертралин, хинидин, пропафенон, амиодарон, циметидин | ||
| 2Е1 | 4,1 | 10q24.3qter | Этиловый спирт, пиразол, пиридин | Тетурам, ритонавир | ||
| ЗА4 | 34,1 | 7q22.1 | Фенобарбитал, гексамидин, дифенин, карбамазепин, глюкокортикоиды, рифампицин, рифабутин, сульфинпразон | Флуоксетин, флувоксамин, пароксети н, хинидин, дилтиазем, циметидин, зафирлукаст, эритромицин, кларитромицин, флуконазол, итраконазол, клотримазол, индинавир, нелфинавир, метронидазол | ||
| ЗА5 | Не установлено | 7q22.1 | Фенобарбитал, гексамидин, дифенин, рифампицин | Кетоконазол, клотримазол, миконазол, метронидазол |
Токсические продукты биотрансформации обезвреживаются конъюгацией с восстановленным глутатионом и ковалентным связыванием с альбуминами. Повреждение молекулы альбумина не опасно для организма, так как этот белок синтезируется в печени со скоростью 10 — 16г в сут. и присутствует в высоких концентрациях в ЭПР.
Ксенобиотики в процессе окисления могут разрушать цитохром Р-450. Такие вещества получили название «суицидные субстраты». Свойствами «суицидных субстратов» обладают четыреххлористый углерод, фторотан, парацетамол, преобразуемые цитохромом Р-450 в свободные радикалы. Их эффект можно рассматривать не только как токсический, но и как защитный — элиминируются молекулы цитохрома Р-450, генерирующие реакционноспособные метаболиты.
Восстановление
Реакции восстановления характерны для альдегидов, кетонов и карбоновых кислот. В ряде случаев восстановление и окисление катализируются одним и тем же ферментом и являются обратимыми (восстановление — окисление продукта метаболизма спирта этилового — уксусного альдегида). Восстанавливаются окисленные метаболиты лекарственных средств — кетоны и карбоновые кислоты (фенамин превращается в фенилизопропанол через стадию фенилацетона).
Ароматические соединения, содержащие нитрогруппу, подвергаются в анаэробных условиях нитроредукции. Промежуточные продукты этой реакции — нитрозо- и гидроксиламиносоединения. В печени функционируют микросомальная и цитоплазматическая нитроредуктазы, в кишечнике — бактериальная нитроредуктаза.
Лекарственные средства с азогруппой восстанавливаются в первичные амины в микросомах печени и кишечной микрофлорой, например, салазопиридазин, применяемый для терапии неспецифического язвенного колита, расщепляется по азосвязи с освобождением сульфапиридазина и кислоты 5-аминосалициловой.
Гидролиз
Гидролиз необходим для биотрансформации лекарственных средств, имеющих строение сложных эфиров и замещенных амидов. Происходит в цитозоле и ЭПР эпителия кишечника и гепатоцитов, а также в крови при участии эстераз и амидаз. При гидролизе молекулы лекарственных средств распадаются на фрагменты, один из которых — кислотный или спиртовый — может проявлять фармакологическую активность.
В медицине используют пролекарства, активируемые гидролазами организма, например, левомицетина стеарат, не обладающий горьким вкусом левомицетина, в кишечнике освобождает активный антибиотик.
Растворимый препарат для инъекций левомицетина сукцинат образует левомицетин под влиянием гидролаз тканей.
Таблица 8. Изоферменты УДФ-глюкуронилтрансферазы, их субстраты, локализация генов изоферментов
| Изоферменты | Субстраты | Локализация генов | |
| хромосома | локус | ||
| UGT1A1 | Билирубин, бупренорфин | 1q21-q23 | |
| UGT1A2P | — | ||
| UGT1A3 | — | ||
| UGT1A4 | Имипрамин, амитриптилин, доксепин, хлорпромазин, ламотриджин, ципрогептадин, кетотифен | ||
| UGT1A5 | — | ||
| UGT1A6 | Парацетамол, ибупрофен, буметанид, вальпроаты, фенол | ||
| UGT1A8 | Пропофол | ||
| UGT12B4 | Хиодезоксихолевая кислота | 4q13 | |
| UGT12B7 | Морфин, ибупрофен, кетопрофен, фенопрофен, оксазепам | ||
| UGT12B8 | Андростендиол | ||
| UGT12B9 | — | ||
| UGT12B10 | — | ||
| UGT12B11 | — | ||
| UGT12B15 | — |
Конъюгация
Наибольшее значение имеет глюкуронирование — присоединение активированной уридиндифосфатом (УДФ) глюкуроновой кислоты к алифатическим, ароматическим спиртам, карбоновым кислотам, веществам с аминогруппой и сульфгидрильной группой. Глюкуронирование катализирует УДФ-глюкуронилтрансфераза. Этот фермент функционирует в ЭПР и цитозоле клеток печени, почек, кишечника, кожи. Семейство глюкуронилтрансфераз включает более 20 изоферментов.
О-, N- и S-глюкурониды хорошо растворяются в воде и подвергаются экскреции с мочой и желчью. Глюкурониды, экскретируемые с желчью, в кишечнике под влиянием фермента бактерий β-глюкуронидазы превращаются в исходные липофильные вещества и повторно всасываются в кровь, что дает начало энтерогепатической циркуляции (сердечные гликозиды наперстянки, левомицетин).
Таблица 9. Реакции трансформации ксенобиотиков
| Реакции | Примеры лекарственных средств | |
| ОКИСЛЕНИЕ | ||
| Алифатическое гидроксилирование Ароматическое гидроксилирование О-деалкилирование N-деалкилирование Окислительное дезаминирование | 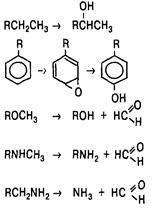
| Этаминал, ибупрофен, бутамид, циклоспорин Фенобарбитал, дифенин, бутадион, анаприлин Кодеин, индометацин Морфин, кодеин, сибазон, имипрамин, теофиллин, эритромицин Норадреналин, адреналин, гистамин, сибазон, фенамин |
| ВОССТАНОВЛЕНИЕ | ||
| Восстановление альдегидов, кетонов, кислот Нитроредукция Азоредукция | 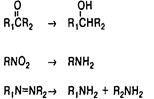
| Варфарин Нитразепам, левомицетин, нитрофураны, метронидазол Салазопиридазин |
| ГИДРОЛИЗ | ||
| Гидролиз эфиров Гидролиз амидов | 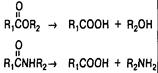
| Кислота ацетилсалициловая, новокаин, дитилин Лидокаин, новокаинамид, индометацин |
| КОНЪЮГАЦИЯ | ||
| Глюкуронирование | 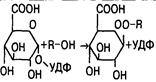
| Морфин, парацетамол, сибазон |
| Сульфатирование | 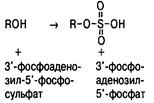
| Парацетамол, метилдопа, стероиды |
| Ацетилирование | 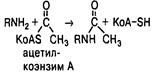
| Клоназепам,апрессин, cульфаниламиды, изониазид |
| Метилирование | 
| Норадреналин, адреналин, морфин, гистамин |
Сульфатирование представляет собой перенос неорганического сульфата от 3'-фосфоаденозил-5'-фосфосульфата на гидроксил алифатических спиртов и фенолов при участии фермента цитозоля — сульфотрансферазы.
Некоторые лекарственные средства в малых дозах образуют сульфоконъюгаты, в больших дозах — глюкурониды.
При ацетилированш уксусная кислота ацетилкоэнзима А присоединяется к аминам, гидразинам, сульфаниламидам. Реакция катализируется ацетилтрансферазой цитозоля клеток. Ацетилированные метаболиты плохо растворяются в воде и элиминируются медленно.
Метилирование — перенос метила от S-аденозилметионина на лекарственное средство под влиянием метилтрансферазы. Это единственная реакция, которая не сопровождается образованием полярных метаболитов.
В последнее время установлено, что в реакциях конъюгации могут появляться токсические метаболиты — N-сульфоэфиры, N-ацетоксиариламины. Они алкилируют ДНК и вызывают мутагенез и канцерогенез.
Примеры реакций биотрансформации ксенобиотиков приведены в табл. 9.
Дата добавления: 2016-07-27; просмотров: 3050;











