Вклад различных видов энергии в общую энергию притяжения молекул
| Молекула | μˉ 10 30, Кл м | α 1030, м3 | Энергия взаимодействия (Е 1067), Дж | ||
| Еор | Еинд | Едисп | |||
| He | 0,203 | 1,2 | |||
| CO | 0,33 | 1,926 | 0,0034 | 0,057 | 67,5 |
| HCl (г) | 3,47 | 1,444 | 18,96 | 5,4 | |
| H2O (г) | 6,10 | 1,48 | |||
| С6Н6 | |||||
| С6Н5NО2 | 13,110 |
Из приведенных данных видно, что наименьший вклад в межмолекулярное взаимодействие вносят индукционные силы. Для сильно полярных молекул значителен вклад ориентационного взаимодействия (Н2О), С6Н5NО2, а в основном молекулы взаимодействуют за счет дисперсионного взаимодействия.
Наряду с силами притяжения между молекулами возникают и силы отталкивания. Теоретических моделей, описывающих эти силы, нет. Известно, что они действуют на ещё более близких расстояниях, чем силы притяжения. Существует удачное эмпирическое приближение:
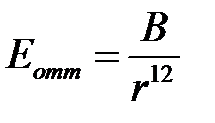 (2.5)
(2.5)
Суммарное выражение для описания сил межмолекулярного взаимодействия можно выразить, например, уравнением Леннарда-Джонса(*): 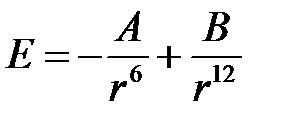 (2.6)
(2.6)
На сравнительно далёких расстояниях превалируют силы притяжения, а на малых – силы отталкивания. На определенном расстоянии эти силы должны быть равны, т.к. это отвечает минимуму энергии:
E
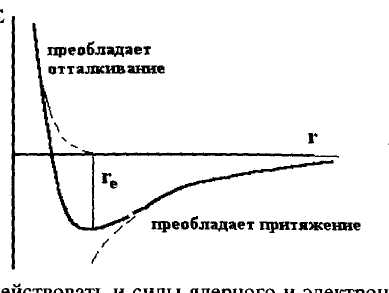
Рис. 2.1. Зависимость потенциальной энергии взаимодействия двух молекул от расстояния между ними
2.2. Поверхностное натяжение
Дата добавления: 2016-07-27; просмотров: 2501;











