Катализ и катализаторы. Ферменты как особые представители катализаторов
Каждая химическая реакция характеризуется энергией активации (AG), т. е. свободной энергией, которую нужно придать реагирующим молекулам, чтобы произошло химическое превращение. Если осуществляется столкновение молекул с недостаточной свободной молекулой – химическая реакция не происходит. Таким образом, энергия активации – это энергетический барьер, который нужно преодолеть, чтобы произошла реакция.
В процессе химических реакций молекулы вступают в так называемое переходное состояние, характеризующееся менее устойчивой структурой и наибольшей свободной энергией. Катализаторы снижают свободную энергию переходного состояния и, стабилизируя его, облегчают протекание реакции.
Следует учитывать, что в энергии активации присутствует не только энтальпийная (DH, тепловая) составляющая, но и энтропийная (DS, мера упорядоченности системы). Высокая энтальпийная составляющая свидетельствует о том, что для формирования переходного состояния необходимо существенное ослабление химических связей. Для многих химических реакций механизм активации молекул, по-видимому, сходен, так как DH для них практически совпадает и составляет около 50 кДж ´ моль-1. Высокая энтропийная составляющая встречается реже и означает, что в процессе формирования переходного состояния молекулы должны принять строго определенную конформацию.
Таким образом, катализатором называется вещество, ускоряющее химическую реакцию, но само в этой реакции не расходующееся. Функция катализатора состоит в том, что он реагирует с исходными веществами, образуя промежуточное соединение (новое переходное состояние), которое подвергается дальнейшему превращению с пониженной энергией активации. В результате образуются продукты реакции и регенерируется катализатор.
Следует напомнить, что катализатор только ускоряет достижение равновесия в химической реакции, но не изменяет его положения (т.е. соотношения субстрата и продуктов). Присутствие катализатора не вызывает термодинамически невозможной реакции и не влияет на выход продуктов, поскольку катализатор не взаимодействует с продуктами реакции:
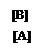
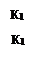 Некатализируемая А ⇄ В Кр= ¾
Некатализируемая А ⇄ В Кр= ¾
реакция
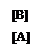
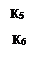
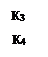 Катализируемая А + Cat ⇄ X ⇄ В + Cat Кр= ¾
Катализируемая А + Cat ⇄ X ⇄ В + Cat Кр= ¾
реакция
Из этих уравнений следует, что константа равновесия реакции (К) не зависит от присутствия катализатора, а следовательно, изменению константы скорости прямой реакции в присутствии катализатора всегда сопутствует соответствующее изменение константы скорости обратной реакции.
Ферменты являются белковыми катализаторами биохимических реакций, большая часть которых в отсутствие ферментов протекала бы крайне медленно. В отличие от небелковых катализаторов (Н+, ОН-, ионы металлов) каждый фермент способен катализировать лишь очень небольшое число реакций, часто только одну. Таким образом, ферменты представляют собой реакционно специфические катализаторы.
Механизмы химического и ферментативного катализа принципиально не различаются. Однако при нормальных «физиологических» условиях (рН и температуре) в водных растворах ферменты значительно более эффективны (сильнее снижают свободную энергию переходного состояния), чем химические катализаторы. Кроме того, ферменты, как правило, катализируют только один из возможных путей превращения субстратов, тогда как в ходе обычных химических реакций образуется смесь продуктов.
Еще более существенным моментом является то, что ферменты обладают чрезвычайно высокой стереоспецифичностью, различая, например, оптические изомеры и даже изотопы одного и того же элемента. Это связано с особенностями структуры активных центров ферментов и конформационной «гибкостью» их молекул. Д. Кошланд сформулировал концепцию индуцированного соответствия, согласно которой при связывании специфического субстрата происходит такое изменение конформации фермента, которое перемещает каталитические группы в положение, обеспечивающее эффективное протекание реакции.
Доказательства конформационных изменений в молекуле фермента при взаимодействии с субстратом получены методами ядерного магнитного резонанса (ЯМР) и рентгеноструктурного анализа (РСА). Например, при взаимодействии карбоксипептидазы А с «плохими» (отличающимися по химической структуре) субстратами происходит перемещение остатков двух аминокислот: тирозина и глутаминовой кислоты, которые предположительно участвуют в каталитическом процессе, на 15 и 2 Å соответственно. Этих перемещений достаточно для проявления макрофизических изменений. Такие конформационные изменения могут быть имитированы веществом, не являющимся субстратом данного фермента. Отсюда становятся понятными факты стимулирующего/ингибирующего влияния молекул, не участвующих непосредственно в ферментативной реакции.
Дата добавления: 2020-10-01; просмотров: 844;











