Физические свойства
Моносахариды – кристаллические вещества, очень легко растворимые в воде. Характеризуются высокой гигроскопичностью. Растворы подавляющего большинства моносахаридов сладки на вкус.
Наличие нескольких гидроксигрупп способствует сильной сольватации моносахаридов в водных растворах. Следствием этого является их способность к образованию концентрированных растворов (40-80%), именуемых сиропами. Из сиропов кристаллизовать моносахарид всегда затруднительно.
Растворы моносахаридов характеризуются оптической активностью и значение [α]D20 является одним из важных параметров для идентификации этих соединений.
Химические свойства моносахаридов
Химические свойства моносахаридов как гетерофункциональных соединений могут быть разделены на три группы: реакции с участием карбонильной группы; реакции спиртовых гидроксилов; реакции, обусловленные взаимным влиянием и взаимным участием карбонильной и гидроксильных групп.
Реакции с участием карбонильной группы
В растворе моносахарида благодаря цикло-цепной таутомерии всегда присутствует определённое количество ациклической (альдегидной или кетонной) формы. Поэтому реакция по карбонильной функции будет проходить так, будто вещество в растворе имеет только ациклическую форму. Это обеспечивается процессом таутомерии: по мере вовлечения в реакцию ациклической формы таутомерное равновесие будет смещаться в её сторону.
В первую очередь следует напомнить, что по карбонильной группе будут протекать реакции окисления и восстановления, нуклеофильного присоединения, присоединения-отщепления.
Окисление.
- альдозы легко окисляются реактивами Фелинга (комплексная соль Cu2+)и Толленса (гидроксид аммиаката серебра [Ag(NH3)2]OH);
- при мягком окислении альдоз (Br2/H2O) образуются одноосновные альдоновые кислоты с таким же числом углеродных атомов: из глюкозы образуется глюконовая кислота; маннозы – манноновая кислота;
- при более жёстком окислении (например, конц. HNO3) одновременно с альдегидной группой окисляется и концевая – первичная спиртовая функция, что приводит к двухосновным аровым кислотам: из глюкозы образуется глюкаровая кислота, из галактозы – галактаровая кислота. В этих реакциях могут произойти и более глубокие окислительные процессы, сопровождающиеся разрывом углерод-углеродных связей.
Следует иметь в виду, что альдоновые и аровые кислоты из-за отсутствия карбонильной группы уже не способны к цикло-цепной таутомерии.
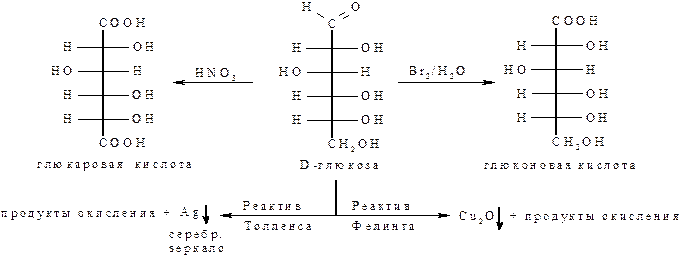
Восстановление. Альдозы при восстановлении переходят в соответствующие многоатомные спирты – альдиты. В этой реакции альдегидная группа превращается в первичноспиртовую группу: например, из глюкозы образуется сорбит, а из ксилозы – ксилит:
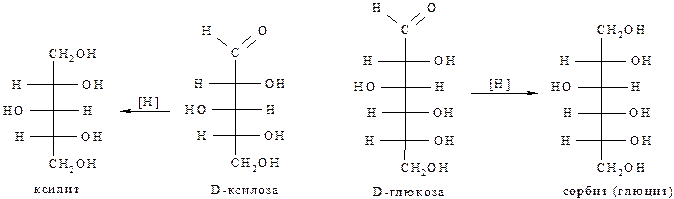
При восстановлении кетоз образуется смесь эпимеров по положению С-2:
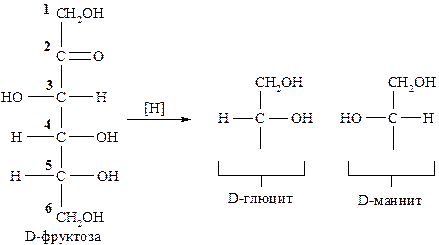
Присоединение HCN к карбонильной группе приводит к соответствующим циангидринам (оксинитрилам), которые при гидролизе превращаются в альдоновые кислоты, содержащие на один атом углерода больше, чем исходный альдегид.
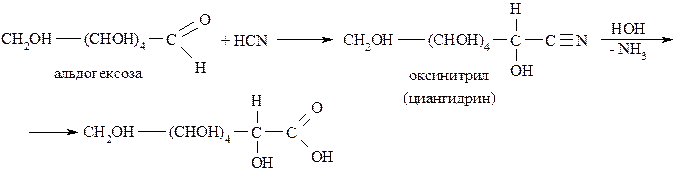
Образование оксимов происходит при взаимодействии моносахаридов с гидроксиламином:
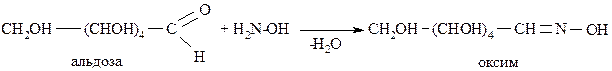
Дата добавления: 2020-10-01; просмотров: 619;











