Реакции в ПРПП, катализируемые ферментами
В зависимости от способа обеспечения ферментативной активности при осуществлении катализируемых ферментами реакций используются ПРПП различных конструкций (рис. 3). В проточном реакторе простейшей конструкции ферменты постоянно вводятся в реактор и выводятся из него по соответствующим линиям (рис. 3, а). Очевидно, такая конструкция оправдана только в том случае, если ферменты настолько дешевы, что их расходом можно пренебречь.
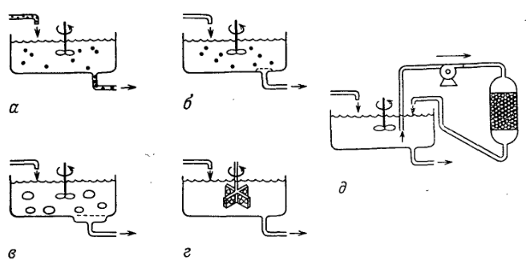
РИС. 3. Схематическое изображение ПРПП различного типа, применяемых для проведения катализируемых ферментами реакций.
а — реактор с непрерывной подачей раствора ферментов; б — реактор с удерживанием ферментов в растворе с помощью полупроницаемой мембраны; в — реактор с удерживанием гранул иммобилизованного фермента с помощью сетчатого фильтра; г — реактор с удерживанием гранул иммобилизованного фермента в контейнерах, размещенных на валу мешалки; д—реактор с рециркуляцией реакционной массы через короткую колонну, наполненную иммобилизованным ферментом.
Более дорогостоящие ферменты необходимо удерживать в реакторе или возвращать в него путем рециркуляции. Ознакомившись в гл. 4 с методами иммобилизации ферментов, мы уже знаем, что эту цель можно достигнуть несколькими путями.
Во-первых, (рис. 3, б) на пути вытекающего из реактора потока можно установить ультрафильтрационную мембрану с порами, диаметр которых позволяет удерживать относительно большие молекулы ферментов в растворе. Если фермент иммобилизован на частицах нерастворимого носителя, суспендированного в реакционной смеси, то для предотвращения потери фермента с вытекающим из реактора потоком достаточно установки простого сетчатого фильтра (рис. 3,6). Принцип другого подхода к удерживанию иммобилизованных ферментов в реакторе схематично изображен на рис 3, г; здесь фермент удерживается в сетчатых контейнерах, укрепленных на валу мешалки. Реакторы такой конструкции, широко применявшиеся также для изучения реакций в газовой фазе на металлических катализаторах на носителях, позволяют свести к минимуму сопротивление массопередаче между жидкой фазой и гранулами иммобилизованного фермента. Та же цель может быть достигнута и более удобным путем — посредством циркуляции реакционной смеси в системе реактор с полным перемешиванием — короткая колонна с насадкой иммобилизованного фермента (рис. 3, d). Если скорость рециркуляции достаточно высока и в каждом цикле при однократном прохождении реакционной смеси через колонну превращению подвергается небольшая часть субстрата (менее 1%), то вся система становится эквивалентной проточному реактору с полным перемешиванием. Отсюда следует, что эта конструкция реактора особенно удобна для изучения кинетики реакций в лабораторных исследованиях.
Рециркуляция фермента возможна только при условии, что фермент легко выделить из вытекающего из реактора потока продуктов реакции. Есть два перспективных подхода к решению этой задачи, один из которых связан с включением фермента в мембрану из жидкого поверхностно-активного вещества или фосфолипида, а второй — с иммобилизацией ферментов на магнитных носителях.
Независимо от типа и конструкции реактора основная задача всегда сводится к поддержанию заданной концентрации фермента в ПРПП. Если эта задача решена, то мы можем сконцентрировать наше внимание на расчете концентраций субстрата и продукта реакции в вытекающем из реактора потоке. Здесь применимы рассмотренные выше общие принципы и уравнения материального баланса, используемые для описания роста популяции микроорганизмов, а также дополнительные ограничения, налагаемые относительно простой стехиометрией изучаемых реакций.
Например, для простой реакции 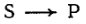 из каждого моля прореагировавшего вещества S образуется один моль вещества Р, и, следовательно, концентрации этих веществ на входе в реактор (s0, p0) и на выходе из реактора (s, р) связаны соотношением
из каждого моля прореагировавшего вещества S образуется один моль вещества Р, и, следовательно, концентрации этих веществ на входе в реактор (s0, p0) и на выходе из реактора (s, р) связаны соотношением
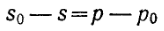 (5)
(5)
Если условие уравнения (9.5) выполнено, то скорость реакций v(s, p), которая является функцией как s, так и р, можно выразить только через s, что упрощает соответствующие выражения. В этом случае уравнение материального баланса по субстрату принимает форму
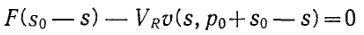 (6)
(6)
В табл. 1 даны решения этого уравнения для различных типов кинетики реакций. Приведенные в таблице уравнения проще использовать непрямым путем; для этого нужно в правую часть уравнения перенести необходимые параметры превращения субстрата и рассчитать искомое время пребывания и (или) концентрацию фермента. Аналогичными способами можно получить уравнения для более сложных реакций и типов кинетики превращений.
Таблица 1. Зависимости между степенью превращения субстрата δ=(s0-s)/s0, средним временем пребывания и концентрацией катализатора в случае катализируемых ферментами реакций в ПРППа

Дата добавления: 2020-10-01; просмотров: 679;











