СТРУКТУРА И ФУНКЦИИ ИММУННОЙ СИСТЕМЫ 4 глава
Эти конкретные взаимосвязи мы проследим в той мере, в которой они известны в настоящее время.
Чтобы понять место иммунитета, ещё раз вспомним и рассмотрим способы (механизмы, уровни) защиты от инфекций, имеющиеся у человека.
· Покровные ткани (кожа, слизистые оболочки).
· Микробоцидные экзосекреты (соляная кислота желудка, бактерицидные компоненты слюны, литические пищеварительные ферменты кишечника и т.п.).
· Сосудистые реакции с целью не пропустить во внутреннюю среду внешние факторы (быстрый локальный отёк в очаге повреждения).
· Белки острой фазы — C–реактивный белок и связывающий маннозу лектин (СМЛ). Их синтезируют клетки печени (гепатоциты). Эти белки обладают способностью (и предназначены для этого) связывать широко распространённые бактерии, вирусы и одноклеточные грибы, попавшие в кровь. На фагоцитах есть специальные Рц, связывающие комплексы микроорганизмов с белками острой фазы, т.е. белки острой фазы являются опсонинами.
· Доиммунный (или первичный) фагоцитоз микробных тел нейтрофилами и макрофагами. Этот способ клеточной защиты происходит от пищеварительной функции одноклеточных организмов. Одна и та же клетка — фагоцит будет пытаться поглотить с целью переваривания разные предложенные ей объекты.
· Лимфоцитарный иммунитет.
· Ментальная поведенческая защита (избегать контактов с заражёнными, мыть руки, правильно стерилизовать медицинские инструменты, одеваться по погоде и т.п.).
Предметом иммунологии как отдельной науки являются не все перечисленные способы защиты организма от инфекций, а в первую очередь лимфоцитарный иммунитет и тесно связанные с ним филогенетически, онтогенетически и морфологически фагоцитоз, белки острой фазы и сосудистые реакции, которые совместно осуществляют такую объединенную защитную реакцию, которую называют воспалением. Каждый отдельный способ защиты от инфекций является предметом изучения других наук (психологии, психиатрии, социологии, педагогики, юриспруденции, дерматологии, гастроэнтерологии и т.д.). При этом, имея дело с конкретным пациентом, врачу следует твёрдо помнить, что организм един и поэтому в каких-то ситуациях полезен, необходим, а подчас и единственно возможен только системный анализ.
Чтобы понять, чем лимфоцитарный иммунитет отличается от других (доиммунных) биологических защитных механизмов, например от фагоцитоза (гидролитических ферментов, радикалов–окислителей и т.п.), необходимо понять, чем отличается распознавание Аг лимфоцитами от распознавания объектов воздействия фагоцитами (ферментами, радикалами и т.п.). В подробностях это описано в главах 3–7 и др. Отличия лимфоцитов в их отношениях с Аг от других клеток и молекул защитного назначения количественные и уже вследствие этого имеют особое качество. Любое биологическое распознавание — это комплементарные взаимодействия двух молекул. Комплементарными называют нековалентные взаимодействия молекул, в которых участвуют 4 типа химических связей — ионные, водородные, ван-дер-ваалъсовы и гидрофобные. Сила связи молекул характеризуется константой диссоциации. Сильные комплементарные взаимодействия называют специфичными, слабые — неспецифичными.
Все клетки многоклеточных организмов, кроме лимфоцитов, претерпевают в онтогенезе консервативную дифференцировку от клетки–предшественницы (зиготы или стволовых клеток регенерирующих тканей) до зрелой функционирующей специализированной клетки. При этом, например, разные макрофаги в одном организме отличаются друг от друга возрастом (стадией развития), степенью активации, макрофаги разной локализации имеют особенности тканевой морфологии. Но если учесть эти различия и «привести их к общему знаменателю», то все макрофаги потенциально способны распознавать одно и то же, так как на поверхности всех макрофагов потенциально экспрессируется одно и то же множество Рц (см. главу 3).
И только лимфоциты дифференцируются так, что на разных лимфоцитах (и их митотических потомках, совокупность которых называют клоном лимфоцитов) экспрессируются разные антигенраспознающие Рц. Общее число вариантов антигенраспознающих Рц лимфоцитов оценивают по-разному — от 1018 до 109 на организм млекопитающего. Сколько разных Аг потенциально может связать один вариант Рц лимфоцита для Аг? Сколько вариантов Рц для Аг на одном лимфоците? В течение последних примерно 50 лет исходили из постулата, что для каждого варианта Рц лимфоцита потенциально существует один свой Аг. Это соотношение идеализировали до «один к одному» с оговоркой о перекрестной реактивности, в основе которой предполагают гомологию структуры молекул разных Аг. Полагали также, что на единичном лимфоците имеется единственный вариант Рц для Аг. Именно этим объясняли суть иммунологической специфичности.
Явление иммунологической специфичности не «отменяют» и сейчас. Но в последние годы появились новые методы исследования вопроса о специфичности Рц лимфоцита для Аг, и в работах 1996–1999 гг. нескольких солидных научных коллективов (в том числе лауреата Нобелевской премии Питера Дохерти) было показано, что специфичность лимфоцита по Аг не «один к одному». Рц живой и гибкий и способен устанавливать комплементарные контакты ионными, водородными, ван–дер–ваальсовыми и гвдрофобными связями со множеством Аг. Подсчитать число конкретных Аг, которые может связать конкретный Рц, в принципе невозможно, как невозможно опытным путём перебрать все вещества на Земле и в Космосе. Поэтому оценки ориентировочные и колеблются от 103 до 107 разных Аг на один вариант Рц. Но в каждом конкретном случае исследователи и врачи имеют дело с конечным и небольшим числом различных веществ, по отношению к которым оценивают реактивность антигенраспознающих Рц лимфоцитов. Например, при получении моноклональных гибридомных АТ исследуют их связывание, кроме целевого Аг, ещё всего лишь с несколькими посторонними молекулами и отбирают только такие АТ, которые связывают заданный Аг и не связывают несколько других. Поэтому в «локальных» работах с конкретным материалом можно исходить из привычных представлений — «одному Аг одно АТ» (или T–лимфоцит). Но при анализе более сложных систем адекватным является как раз современное представление о множественной специфичности антигенраспознающих Рц лимфоцитов.
1.3.2. Антигены
Самое простое и по сути точное определение Аг — это определение его как некоего вещества, которое по своей химической природе способно связать какие–либо антигенраспознающие Рц лимфоцитов — T или В. Тем не менее оно недостаточно удовлетворяет прикладным интересам биологов, иммунологов и врачей разных специальностей. Чтобы лимфоциты имели возможность что–либо распознавать во внутренней среде, человек сначала должен нечто ввести в организм или констатировать самопроизвольное попадание этого нечто в организм. Процедуру введения Аг в организм называют иммунизацией. В патологическом аспекте аллергологи иммунизацию называют сенсибилизацией. Ту форму вещества, которую вводят в организм с целью индукции иммунного ответа, называют иммуногеном или, что бывает чаще, тоже Аг. Таким образом, в прикладном смысле Аг называют вещества или те формы веществ, которые при введении во внутреннюю среду организма способны индуцировать на себя иммунный ответ в виде выработки специфических АТ и/или иммунных T–лимфоцитов. Это не те же самые формы, которые способны связывать, например, Рц T–лимфоцитов для Аг. Другие клетки — антигенпредставляющие (АПК), предварительно перерабатывают внутри себя иммуноген, превращая его в «видимую» для T–лимфоцита форму — комплекс пептида с молекулами MHC. Иммуноглобулины (АТ) же в отличие от T–лимфоцитов способны распознавать, т.е. связывать, эпитопы на нативных, непереработанных молекулах веществ. Какие же формы внешних веществ способны индуцировать иммунный ответ в организме млекопитающих, т.е. являются Аг в прикладном смысле? Опыт показывает, что иммуногенны достаточно крупные молекулы с молекулярной массой в несколько десятков тысяч дальтон, но в конкретных случаях можно индуцировать иммунный ответ и на относительно небольшие молекулы с относительной молекулярной массой порядка сотен. По химической природе иммуногенны белки, полисахариды, фосфолипиды и их комбинации. Можно получить специфические АТ, связывающие малые молекулы, например, ароматических веществ, но для этого перед введением в организм животного эти малые молекулы необходимо конъюгировать с какой–либо макромолекулой. Малую молекулу в данном случае называют гаптеном, макромолекулу — носителем.
Главным свойством, определяющим, может или не может то или иное вещество быть Аг для данного организма, является способность этого вещества прочно связываться с клетками или/и межклеточным матриксом (т.е. тканями) данного организма и при этом быть доступным для распознавания лимфоцитами.
В прикладных аспектах Аг (точнее, иммуногены) классифицируют в соответствии с теми свойствами, которые важны для конкретного прикладного аспекта. Например, аллергологи классифицируют Аг (аллергены) на пищевые, пыльцевые, эпидермальные, бытовые, инсектные и т.п., т.е. в соответствии с источником происхождения и путями попадания в организм человека. Врачи, занимающиеся профессиональными болезнями, выделяют иммуногенные вещества «на рабочем месте»: латекс, красители, ксенобиотики и т.д. Трансплантологи классифицируют тканевые Аг на алло–, ксено– или сингенные, ткане–, органоспецифичные. Микробиологи классифицируют Аг микроорганизмов в соответствии с таксономической классификацией последних на видо–, типо–, подтипо– и группоспецифичные и т.д. Онкологи выделяют опухолеспецифичные Аг, раково-эмбриональные Аг, маркёрные Аг. Биологи, занимающиеся морфогенезом, выделяют стадиоспецифические тканевые Аг, эмбриоспецифические Аг. И так в любой частной специальности вещества, способные индуцировать иммунный ответ, классифицируют по признакам, имеющим наибольшее значение именно для данной специальности.
Индукция иммунного ответа — сложный физиологический процесс. На одну и ту же форму иммуногена в одном и том же организме можно индуцировать иммунный ответ разной интенсивности в зависимости от применения или неприменения неких сопутствующих воздействий. Речь идёт об адъювантах — веществах, способных усиливать иммунный ответ на заданный иммуноген. Адъювантными свойствами обладают вещества, способные индуцировать доиммунное воспаление в тканях, а медиаторы доиммунного воспаления — цитокины дендритных клеток, макрофагов, фибробластов, кератиноцитов (TNF–a, ИЛ–1, ИЛ–12 и др.) способствуют развитию реакций лимфоцитарного иммунитета, т.е. собственно иммунного ответа. Классическими адъювантами являются адъювант Фройнда (смесь вазелиновых масел с инактивированными микобактериями туберкулёза — это полный адъювант или без микобактерий — это неполный адъювант), гидроокись алюминия (алюминиевые квасцы), мурамилди– или трипептиды — синтетические аналоги компонентов бактериальных стенок. Большое количество работ выполнено отечественными исследователями в Институте иммунологии МЗ РФ по разработке новых полимерных синтетических адъювантов или носителей на основе поливинилпиридинов, азоксимера и других соединений полиэлектролитной/полиионной природы.
Как будет показано в дальнейшем, Аг могут быть вовсе не только чужеродные, но в той же, если не в большей мере и молекулы своего собственного организма. Антигенраспознающий Рц лимфоцита формируется в процессе дифференцировки, которую называют иммунопоэзом. Иммунопоэз большинства лимфоцитов происходит во внутренней среде организма, без доступа экзогенных субстанций, на территории лимфопоэтических органов (костного мозга, тимуса, барьерных слизистых оболочек). Таким образом, дифференцировка и отбор антигенраспознаюших Рц, в том числе предназначенных для связывания потенциальных чужеродных Аг, проходят при взаимодействиях исключительно со своими эндогенными антигенами.
Конкретные исследования показывают, что по природе Аг, т.е. то, что распознаёт иммунная система, а именно антигенраспознающие Рц лимфоцитов — это молекулы наружных мембран клеток и клеточные продукты, секретированные из клетки. По биохимической природе Аг относятся к белкам, их производным — гликопротеинам, липопротеинам. Кроме того, Аг бывают чистые углеводы, липополисахариды, фосфорилированные производные различных органических молекул.
Иммунитет не контролирует собственно генетический гомеостаз организма. Геном как таковой не объект действия для иммунитета. Иммунная система по своей природе распознаёт то, что в классической генетике называют фенотипом, т.е. молекулы поверхности клеток и межклеточного матрикса.
1.3.3. Определение иммунитета. «Формула» иммунного ответа
Иммунитет — особое биологическое свойство многоклеточных организмов, в норме предназначенное для защиты от инфекций и иных внешних патогенов, способных при попадании во внутреннюю среду вступать в прочные связи с клетками и/или межклеточным веществом. Носителями этого свойства служат специализированные клетки — лимфоциты. Уникальным и отличительным свойством лимфоцитов как множества клеток является способность распознавать широкое множество (»1018) разнообразных молекулярных объектов (Аг). Распознавание есть физическое связывание. После распознавания лимфоцит инициирует и мобилизует как собственные, так и общевоспалительные механизмы деструкции повреждённых патогеном тканей, после чего наступает их элиминация из организма. Такимобразом,кратко:
Иммунитет = распознавание + деструкция повреждённых тканей.
Иммунитет — по предназначению защитное свойство, но как процесс он реализуется только относительно внутренних свойств организма и свойств Аг(ов), на которые реагирует иммунная система.
Ниже, подробно разбирая этапы иммунного ответа, мы увидим, что до того, как будет возможно распознавание Аг лимфоцитом, происходят процессы, «подготавливающие» эту возможность лимфоцитарного распознавания. И эти процессы — доиммунные воспалительные реакции в тканях, в первую очередь покровных, если внешний агент проникает в организм через покровные ткани. Это сосудистые реакции, реакции клеток покровных тканей, реакции лейкоцитов крови общевоспалительного назначения — нейтрофилов, моноцитов, базофилов, тучных клеток, эозинофилов. Это естественно, ибо иммунная система входит в состав целостного организма, «вплетена» в него не как посторонняя и опирается в своём функционировании на другие системы клеток и тканей своего организма. Иммунный ответ как процесс можно определить и представить следующей схемой.
Такое понимание иммунитета помогает ясно разобраться в связях иммунной системы с различными патологическими процессами в организме. В итоге любого правильного, нормального, иммунного ответа происходит деструкция, т.е. альтерация собственных клеток, повреждённых инфекцией. Альтерация всегда сопровождается сосудистыми реакциями, рассчитанными на тампонаду или рассасывание очага, и активным действием клеточных и внеклеточных ферментативных расщепительных систем, что и называют термином «воспаление», т.е. иммунный ответ в норме обязательно и начинается и заканчивается воспалением. Доиммунное воспаление организуют эпителиальные и соединительнотканные клетки покровных тканей, а именно кератиноциты, фагоциты и макрофаги, дендритные клетки, тучные клетки, активируемые, например, белками комплемента (C5a), которые в свою очередь приобретают активное состояние от контакта с широко распространёнными в земной биосфере микробными компонентами.
В кратце процесс иммунного ответа можно определить и представить следующей схемой:

· Доиммунное воспаление: выделяются цитокины и хемокины, активирующие поглощающие Аг клетки, в частности дендритные (ДК), и эндотелиальные.
· Распознавание Аг происходит в периферических лимфоидных органах (начало иммунного ответа — пролиферация и дифференцировка эффекторных и регуляторных лимфоцитов).
· Деструкция Аг и тканей, повреждённых патогеном (иммунное воспаление, при котором одни лимфоциты (регуляторные) «нанимают» для деструкции другие лимфоциты (эффекторные) и/или лейкоциты общевоспалительного назначения — нейтрофилы, моноциты, базофилы, тучные клетки, эозинофилы или гуморальные литические системы типа комплемента)
· Выведение продуктов распада общеорганизменными системами выделения.
В послесловии будет приведена расширенная схема иммунного ответа, отражающая прогрессивное развитие наших знаний; при этом все положения данной схемы остаются верными.
Иммунное воспаление организуют лимфоциты, распознавшие свой Аг. На деструкцию лимфоциты «нанимают» лейкоциты — все существующие их разновидности. Разные типы лимфоцитов имеют в качестве партнёров разные типы лейкоцитов, что будет подробно рассмотрено далее.
Если количество Аг относительно невелико, то его деструкция и элиминация проходят под порогом чувствительности анализаторов ЦНС и организм не чувствует боли, отёка, потепления, покраснения и нарушения функции того или иного органа. Если же количество распознаваемого и удаляемого Аг относительно велико, то организм начинает чувствовать rubor, tumor, calor, dolor et functio lesae. Так же «с болью» проходит иммунный ответ на любое количество Аг при нарушенных пропорциях или «неправильном» качестве компонентов иммунной системы — наример при аллергических и истинно аутоиммунных заболеваниях.
Глава 2
КОМПОНЕНТЫ ИММУННОЙ СИСТЕМЫ
2.1. Лимфоидная ткань
Анатомический синоним иммунной системы — лимфоидная система. Однако понять устройство и функционирование иммунной системы можно, только проследив конкретные взаимосвязи лимфоидной системы с другими системами организма, по крайней мере с системой клеток крови и кровеносных сосудов, а также покровными тканями (слизистыми оболочками и кожей). Эти системы — ближайшие партнёры, на которые в своей работе опирается система лимфоцитарного иммунитета. Более того, гистогенетически собственно лимфоциты — компонент системы крови: лимфоциты происходят из общей для всех клеток крови стволовой кроветворной клетки. Как мы увидим дальше, нельзя избежать рассмотрения иммунных подсистем барьерных тканей — кожи и слизистых оболочек, печени, что и понятно, учитывая такие функции иммунитета, как защиту от инфекций и реакции на пищевые и ингаляционные внешние вещества.
В организме взрослого здорового человека содержится около 1013 лимфоцитов, т.е. примерно каждая 10-я клетка тела — лимфоцит. Как они расположены в организме? Анатомо-физиологический принцип устройства иммунной системы — органно-циркуляторный. Это значит, что есть ряд специализированных органов с организованной внутренней структурой. При этом лимфоциты не «сидят» в лимфоидных органах постоянно (в отличие от, например, гепатоцитов в печени), а интенсивно рециркулируют между лимфоидными органами и нелимфоидными тканями через лимфатические сосуды и кровь: через один лимфатический узел за один час проходит »109 лимфоцитов. Из общего количества лимфоцитов организма в каждый момент времени в крови находится только 0,2–2%. Миграция лимфоцитов из крови в ткани и из тканей в кровь происходит сквозь стенку сосудов за исключением эфферентных лимфатических сосудов лимфоидных органов, и механизм этой миграции включает в себя специфические взаимодействия определённых молекул на мембране лимфоцита с определёнными молекулами на мембране клеток эндотелия стенки сосудов (такие молекулы называют адгезинами, селектинами, интегринами, хоминг–Рц (от англ. home — «дом» в смысле место, предназначенное данному лимфоциту природой). Эти взаимодействия происходят не в каком придётся месте сосуда, а в определённых местах, например в лимфатических узлах — это эндотелий посткапиллярных венул. Процесс миграции лимфоцитов, конечно же, не носит характер случайного передвижения, а строго регулируется рядом факторов, зависящих от местных тканевых и системных физиологических «задач» организма.
Выделяют следующие органы и ткани иммунной системы(рис. 2.1).
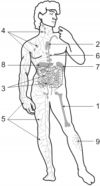
Рис. 2.1. Локализация иммунной (лимфоидной) системы в организме человека. 1 — кроветворный костный мозг; 2 — тимус; 3 — неинкапсулированная лимфоидная ткань слизистых оболочек; 4 — лимфатические узлы; 5 — сосуды лимфодренажа покровных тканей (афферентные лимфатические сосуды); 6 — грудной лимфатический проток [впадает в системную циркуляцию (кровь) через верхнюю полую вену]; 7 — селезёнка; 8 — печень; 9 — внутриэпителиальные лимфоциты.
à Кроветворный костный мозг — место обитания стволовых кроветворных клеток (СКК).
à Инкапсулированные органы: тимус, селезёнка, лимфатические узлы, печень.
à Неинкапсулированная лимфоидная ткань.
Ä Лимфоидная ткань слизистых оболочек (MALT — Mucosal–Аssociated Lymphoid Tissue). В том числе:
Ú Лимфоидная ткань, ассоциированная с ЖКТ (GALT — Gut–Associated Lymphoid Tissue) — миндалины, аппендикс, пейеровы бляшки, а также субпопуляция внутриэпителиальных лимфоцитов слизистой оболочки ЖКТ.
Ú Лимфоидная ткань, ассоциированная с бронхами и бронхиолами (BALT — Bronchus–Associated Lymphoid Tissue), а также внутриэпителиальные лимфоциты слизистой оболочки дыхательной системы.
Ú Лимфоидная ткань, ассоциированная с женскими половыми путями (VALT — Vulvovaginal–Associated Lymphoid Tissue), а также внутриэпителиальные лимфоциты их слизистой оболочки.
Ú Лимфоидная ткань, ассоциированная с носоглоткой (NALT — Nose–Associated Lymphoid Tissue), а также внутриэпителиальные лимфоциты её слизистой оболочки.
Ä Субпопуляции лимфоцитов печени, которая в качестве лимфоидного барьера «обслуживает» кровь воротной вены, несущей все всосавшиеся в кишечнике вещества.
Ä Лимфоидная подсистема кожи (SALT – Skin-Associated Lymphoid Tissue) диссеминированные внутриэпителиальные лимфоциты и региональные лимфатические узлы и сосуды лимфодренажа.
à Периферическая кровь — транспортно–коммуникационный компонент иммунной системы.
Кроветворный костный мозг и тимус называют центральными органами иммунной системы потому, что на их территории происходит дифференцировка лимфоцитов из стволовой кроветворной клетки, так называемый лимфопоэз. Лимфопоэз — это дифференцировка лимфоцитов от стволовой кроветворной клетки до зрелого неиммунного лимфоцита. Зрелые неиммунные лимфоциты локализуются в периферических лимфоидных органах и циркулируют между ними через кровь. На территории периферических лимфоидных органов зрелые неиммунные лимфоциты вступают в контакты с АПК (АПК). Если антигенраспознающий Рц лимфоцита связывает комплементарный Аг на территории периферических лимфоидных органов, где в норме создаются все необходимые условия (корецепторные взаимодействия) для начала развития иммунного ответа, то лимфоцит вступает на путь додифференцировки в режиме иммунного ответа, т.е. начинает пролиферироватъ и продуцировать эффекторные молекулы (цитокины, перфорин, гранзимы и др. в зависимости от субпопуляции лимфоцита). Дифференцировку лимфоцитов на периферии после распознавания Аг называют иммуногенезом. Зрелые неиммунные лимфоциты в англоязычной литературе называют naive (наивные),или virgine (девственные).
Обязательным процессом в начале иммуногенеза в периферических лимфоидных органах является пролиферация клонов лимфоцитов, распознавших Аг. В результате иммуногенеза развиваются клоны иммунных или эффекторных лимфоцитов, которые в англоязычной литературе называют armed (вооружённые) или effector (эффекторные) лимфоциты. Иммунные лимфоциты распознают Аг и организуют деструкцию различных периферических тканей организма, где этот Аг присутствует.
В костном мозге проходит дифференцировка всех лейкоцитов крови. По выходе из костного мозга в периферические ткани лейкоциты в норме уже никогда не будут пролиферировать (в отличие от лимфоцитов). В ответ на адекватные сигналы извне они лишь будут активированы к выполнению своих предопределённых в процессе дифференцировки функций.
Строма костного мозга поддерживает пролиферацию и дифференцировку эритроидного (в итоге эритроциты), миелоидного (лейкоциты) и мегакариоцитарного ростков кроветворения. На территории костного мозга из стволовой кроветворной клетки образуется общая клетка — предшественник всех лимфоцитов, из которой также на территории костного мозга проходят поэз 3 из 4 её потомков: В2–лимфоциты, нормальные киллеры (NK) и дендритные клетки (ДК). Четвертый потомок, коммитированный (запрограммированный) к дифференцировке в T–лимфоциты, мигрирует для прохождения поэза из костного мозга в тимус, и какая-то часть — в слизистые оболочки, в основном ЖКТ. Схема кроветворения и лимфопоэза представлена в табл. 2.1.
Из табл. 2.1 видно, какие клетки входят в состав иммунной системы. Собственно иммуноциты — это все варианты лимфоцитов — T, B, NK. Непосредственные клетки — сотрудники лимфоцитов — все варианты лейкоцитов —·дендритные клетки, нейтрофилы, моноциты/макрофаги, эозинофилы, базофилы, тучные клетки. И даже эритроциты вносят свой вклад в деструктивное завершение иммунного ответа — транспортируют иммунные комплексы «Аг+АТ+комплемент» (на эритроцитах есть Рц для комплемента) в печень и селёзенку для фагоцитоза и разрушения.
Кроме названных клеток мезенхимного происхождения, в состав лимфоидных органов входят клетки стромы, это преимущественно эпителиальные клетки эктодермального и энтодермального происхождения, а также эндотелий сосудов, с которым взаимодействуют все клетки — участники иммунного ответа как целого и сквозь который происходит экстравазация лимфоцитов и лейкоцитов при их миграциях.
Таблица 2.1. Схема кроветворения из стволовой кроветворной клетки и схема лимфопоэза
| Схема кроветворения | |||||||||||||||||||||
| Стволовая кроветворная клетка, ростки | |||||||||||||||||||||
| Эрит-роид-ный | Миелоидный | Мега-карио-цитарный | Клетка-редшественник B1–лимфоцитов (автономизируется в эмбриональном периоде) | Общая лимфоидная клетка–предшественница | |||||||||||||||||
| Коммитированные клетки–предшественницы для дифференцировки в: | |||||||||||||||||||||
| Эритробласты, незрелые эритроциты | Общая клетка–предшественница фагоцитов — нейтрофилов и моноцитов | Общая клетка–предшественница эозинофилов и базофилов | Клетка-предшест–венница тучных клеток | Мега-карио-бласты | — | T | В2 | ДК2 | NK | ||||||||||||
| T | T | ||||||||||||||||||||
| Зрелые клетки в периферической крови | |||||||||||||||||||||
| Эритроциты | Нейтро-филы | Моноциты | Эози-но-филы | Базо-филы | ? | Тромбоциты | В1 –лимфоциты (мало) | T | T | В2 | ДК 2–лимфоидные дендритные клетки | субпопуляция NK крови | |||||||||
| Оседлые потомки в тканях (в норме, вне воспаления) | |||||||||||||||||||||
| — | — | Макрофаги | DC1-миелоидные дендритные клетки | — | — | Тучные клетки | — | В1–лимфоциты в брюшной и плевральной полостях | T | T | Плазмоциты (в лимфоузлах, костном мозге, слизистых) | ДК 2 (интердигитирующие клетки в тимусе, в лимфоузлах; клетки Лангерганса в коже) | NK тканевые (в печени, в деци-дуальной оболочке матки) | ||||||||
| Схема лимфопоэза | |||||||||||||||||||||
| Стволовая кроветворная клетка (костный мозг)
| |||||||||||||||||||||
| Коммитированная к лимфопоэзу клетка–предшественница (общая для всех лимфоцитов)
| |||||||||||||||||||||
| ДК 2 крови, стромы тимуса, клетки Лангерганса | В2 |
T–лимфоциты
| Нормальные киллеры | ||||||||||||||||||
| АПК ДК 2 | В2 (в костном мозге) | T | T | ||||||||||||||||||
| CD4+ | CD8+ | CD4– CD8– | ЦТЛ | Th(?) | |||||||||||||||||
| Функционально зрелые субпопуляции иммунных лимфоцитов и дендритные клетки | |||||||||||||||||||||
| Активированные АПК | Продуценты IgM IgG IgA IgE | NK1.1 + Th0 Тh1 Th2 (Th3) тчцтл | ЦТЛ | Ранние продуценты ИЛ–4 | ЦТЛ; [Th0, Тh1, Th2, (Тh3)] (?) | Клетки–эффекторы IgG–опосредованной АЗКЦТ | |||||||||||||||
Помимо клеток, «иммунологическая материя» представлена растворимыми молекулами — гуморальными факторами. Это продукты B–лимфоцитов — АТ (они же иммуноглобулины) и растворимые медиаторы межклеточных взаимодействий — цитокины. Цитокины — это та молекулярная «материя», посредством которой лимфоцитарный иммунитет «встроен», интегрирован в организм в целом. Цитокины вырождены относительно тканевой дифференцировки клеток–продуцентов, т.е. одни и те же гены цитокинов могут экспрессироваться в клетках разной дифференцировки. Цитокины (от греческих корней cyto — клетка, kinos — движение) — молекулы, секретируемые клетками во внеклеточную среду с целью воздействовать на другие клетки или на себя же, подать сигнал к запуску тех или иных процессов в клетках–мишенях. Цитокины — молекулярный «язык» межклеточного общения, для большинства цитокинов — локального, близкодействующего взаимодействия, ещё один «язык» наряду с нейромедиаторами и эндокринными гормонами (последние два — дистантного действия).
Дата добавления: 2016-07-18; просмотров: 3441;











