СТРУКТУРА И ФУНКЦИИ ИММУННОЙ СИСТЕМЫ 3 глава
Фрэнк Бёрнет сформулировал «теорию селекции клонов», объединив мысли и находки нескольких учёных:
1) естественные АТ представлены в виде Рц на поверхности неких мезенхимных клеток;
2) Аг при попадании в организм связывают эти Рц;
3) наступает пролиферация клона клеток, Рц которых связались с Аг;
4) часть клеток клона становится клетками памяти;
5) иммунологическая толерантность — результат «выброса клона» («clonal abortion»), что происходит в определённые критические периоды эмбрионального развития.
Бёрнету же принадлежит выдвинутая им в середине 60-х годов XX в. гипотеза об «иммунологическом надзоре» в организме, в которой он предположил, что иммунная система следит не только за инфекционными микробами во внутренней среде, но и за собственными мутантными клетками. Гипотеза теоретически привлекательна, но на практике до настоящего времени она все-таки не нашла пока устойчивой опоры в фактическом материале. Бёрнет вместе с Медаваром удостоены Нобелевской премии за открытие и исследование феномена индуцированной иммунологической толерантности и за понимание того, что толерантность есть свойство клеток иммунной системы, в естественных условиях развивающееся во время эмбриогенеза.
Эксперименты Дэвида Толмейджа и Джошуа Ледерберга в 60-х годах XX в. поддержали клеточную селективную теорию иммунитета. Толмейдж мыслил количественно и сопоставил спектр разнообразия антигенсвязывающих свойств АТ и количество клеток в организме. Он пришел к выводу (который современные иммунологи подтвердили только в работах 2000 г. и далеко не все принимают это до сих пор), что ограниченное множество АТ (клонотипов, по терминологии автора) способно связывать гораздо большее множество разнообразных Аг. Это была нетривиальная мысль, которую пока не воспринимают многие профессиональные иммунологи; им легче думать, что каждому Аг — своё АТ, и наоборот. Дж. Ледерберг сосредоточился на генетике и подошел к мысли о том, что разнообразие АТ определяется высокой скоростью соматических мутаций в «иммуноглобулиновом гене» (фактически это предсказание соматической рекомбинации ДНК иммуноглобулиновых генов).
Развивая клеточную клональную теорию иммунитета, Бёрнет полагал, что все, что требуется для начала иммунного ответа — это чтобы мезенхимные клетки (как потом стало известно, лимфоциты) определённого клона связали свой Аг (single signal — единственный сигнал). Авторитет Бёрнета был настолько высок, а его представления настолько просты, что на многие годы эта мысль стала общепринятой. Но действительность опять оказалась не так проста. Чем дальше, тем больше накапливалось фактов, показывающих, что лимфоциту, чтобы начать иммунный ответ, обязательно нужно получить из внешней для него среды и другие сигналы, кроме связывания Аг. Впервые двусигнальную модель (two–signal) предсказали, а затем и участвовали наряду с другими исследователями в её фактическом доказательстве П. Бретчер и М. Кон в 1969 г., чуть позже к ним присоединился Р. Лангман. Они ввели понятие и термин T–лимфоцитов–хелперов для антителопродуцирующих B–лимфоцитов. В 1972 г. К. Лафферти и А. Каннингам показали, что и активация самих T–лимфоцитов требует двух (c точкb зрения того времени) сигналов: 1) Аг и 2) обязательного костимуляторного сигнала. На самом деле и по сегодняшний день в исчерпывающей мере неясно, какие именно условия необходимы и достаточны для инициации лимфоцитарного иммунного ответа, нормального его развития и завершения. Существует лишь ряд гипотез на эту тему.
Выделим историю развития иммунологии в России, начиная с XVIII в. До И.И. Мечникова были известны по крайней мере три имени. М.М. Тереховскийодним из первых занялся экспериментальной микробиологией: он изучал размножение и дыхание микроорганизмов, влияние на них разных температур, электрических разрядов, химических веществ. Похоже, что уже за 100 лет до Л. Пастера этот исследователь знал методы аттенуации, но его работы не были известны миру. Зато выдающийся отечественный врач Д.С.Самойлович был избран членом 12 зарубежных академий наук. Самойлович вошёл в историю как первый «охотник» за возбудителем чумы. Он работал на вспышках чумы в Москве (1771), Херсоне и Кременчуге (1784), Тамани (1796), Одессе (1797), Феодосии (1799), был главным доктором карантинов (как тогда называли таких врачей) юга России. Самойлович разработал и сам применял на практике комплекс противочумных мероприятий. На собственных наблюдениях он пришел к выводу, что переболевшие чумой люди приобретают иммунитет к ней, и высказывал идею создания искусственных прививок против этой болезни.
Л.С. Ценковский, профессор Харьковского университета, описал 43 новых вида микроорганизмов и написал работу по систематике «О низших водорослях и инфузориях», в которой высказал идею, что бактерии ближе к растениям, чем к простейшим. Независимо от Пастера Ценковский получил эффективную сибиреязвенную вакцину; организовал в Харькове пастеровскую станцию.
Открытие такой новой формы жизни, как вирусы, сделал русский учёный Д.И. Ивановский. Его именем назван и ныне действующий московский Институт вирусологии. В 1892 г. Ивановский сделал доклад на заседании Российской академии наук о том, что возбудителем мозаичной болезни табака является фильтрующийся микроорганизм — вирус!
Вошли в историю ученики Мечникова: A.M. Безредка (метод десенсибилизации при серотерапии), Л.А. Тарасевич (организовал службу контроля вакцин и сывороток), И.Г. Савченко (установил стрептококковую этиологию скарлатины, первым использовал антитоксическую сыворотку для её лечения, вместе с Мечниковым изучал механизмы фагоцитоза, создал школу микробиологов в Казани).
Иммунология как наука развивалась и в XX в. В XX в. Россия пережила на своей территории две войны невиданной разрушительной силы, унесшие лучшие человеческие ресурсы — десятки миллионов — и колоссальные материальные. Кроме того, Россия пережила уничтожение русской школы генетики и генетиков в 20-х годах XX в. — лучших в мире в то время. Объективно стране было не до такой «роскоши», как наука. И тем не менее во все эти годы были люди, которые не уезжали за рубеж, работали и делали открытия в области микробиологии, вирусологии и иммунологии. Всякий человек, хоть сколько-нибудь учившийся медицине, знает такие имена, как Н.Ф. Гамалея (открыл бактериолизины, трансмиссию возбудителей тифов с насекомыми), Г.Н. Габричевский (бактериологическое производство), Е.И. Марциновский (малярия и тропические болезни), Н.Я. Чистович (первая клиника инфекционных болезней в России), П.Ф. Здродовский (тропические болезни, бруцеллёз, риккетсиозы), Л.А. Зильбер (вирус клещевого энцефалита, вирусная теория генеза опухолей), З.В. Ермольева (получила первые отечественные антибиотики — пенициллин и стрептомицин), М.П. Чумакови А.А. Смородинцев (разработали полиомиелитную вакцину), В.М. Жданов (наладил вирусологическую службу по всей территории страны), А.А. Богомолец (роль соединительной ткани в иммунитете), А.Д. Адо (советская аллергологическая школа). И среди ныне живущих наших соотечественников немало отдавших не одно десятилетие своей жизни иммунологии и сказавших, кто громче, кто тише, новое слово в этой науке.
С конца 80-х годов XX в. наступила пора новейшей истории иммунологии, в этой области работают многие тысячи исследователей и врачей во всем мире и не в последнюю очередь в России, быстро накапливаются новые факты. Постепенно, медленно, но происходит поворот в понимании роли современной науки в жизни общества, в том числе иммунологии в медицине, от преобразовательной к сохранительной в отношении природы, ибо только Наука содержит в себе потенциальные возможности понять и объяснить обществу, чего нельзя делать, чтобы окончательно не погубить не нами созданную жизнь на планете.
Таким образом, крупным планом в истории иммунологии последних 120 лет можно выделить три смены концепций во времени.
I. В конце XIX — начале XX в. иммунология выросла из медицинской бактериологии, в первую очередь развивалась серология, её клинические приложения. В это время (и по сегодняшний день) иммунология сопряжена также с патологической физиологией в исследованиях аллергичеких реакций и анафилаксии и воспаления в любом его проявлении.
II. Со времени первой мировой войны в иммунологии набирают силу химические идеи и до середины 60-х годов XX в. преобладает методически и теоретически иммунохимия.
III. С 60-х годов XX в. и до настоящего времени иммунология все больше превращается в системную дисциплину — иммунобиологию. Идеи и методы иммунологии проникли во все без исключения, в том числе самые частные, медицинские специальности. На сегодня по объёму добытых знаний иммунологию признают наиболее разработанной областью биологии и медицины среди всех прочих разделов науки о живом.
В заключение исторического очерка приведём список лауреатов Нобелевской премии по биологии и медицине за работы по иммунологии. Напомним, что Нобелевская премия учреждена с 1901 г. и за исключением нескольких первых премий, как правило, её не присуждают раньше чем через 15–20 лет после первой публикации авторов. Эти 15–20 лет отводят для проверки и перепроверки заявляемого открытия.
Эмиль Беринг (Emil A. von Behring, 1854–1917, Германия) — Нобелевская премия 1901 г. за открытие антитоксинов, впоследствии АТ, и серотерапию дифтерии. Это первая в истории Нобелевская премия.
Роберт Кох (Robert Koch, 1843–1910, Германия) — Нобелевская премия 1905 г. за исследования по туберкулёзу.
Илья Ильич Мечников (1845–1916, Россия) — Нобелевская премия 1908 г. за открытие защитной роли фагоцитоза и клеточную теорию иммунитета.
Пауль Эрлих (Paul Ehrlich, 1854–1915, Германия) — Нобелевская премия 1908 г. (совместно с И.И. Мечниковым) за гуморальную теорию иммунитета.
Шарль Рише (Charles Richet, 1850–1935, Франция) — Нобелевская премия 1913 г. за работы по анафилаксии и открытие того, что иммунный ответ может не только защитить, но и повредить организм.
Жюль Борде (Jules Bordet, 1870–1961, Бельгия) — Нобелевская премия 1919 г. за экспериментальные работы по комплементзависимому бактериолизу, специфическому гемолизу, за разработку метода фиксации комплемента для диагностики инфекционных болезней.
Карл Ландштайнер (Karl Landsteiner, 1868–1943, Австрия) — Нобелевская премия 1930 г. за открытие групп крови и фундаментальную книгу «The Specificity of Serologiс Reactions». Сам Ландштайнер считал, что не открытие групп крови — его главное дело жизни, а исследования реакции Аг с АТ.
Макс Тэйлер (Max Theiler, 1899–1972, ЮАP–Великобритания–США) — Нобелевская премия 1951 г. за создание вакцины против жёлтой лихорадки.
Дэниэль Бовэ (Daniel Bovet, 1907, Италия) — Нобелевская премия 1957 г. за открытие роли гистамина в патогенезе аллергических реакций и разработку антигистаминных ЛС для лечения аллергических болезней. Кроме того, он разработал курареподобные релаксанты, транквилизаторы и ряд анестетиков.
Фрэнк Бёрнет (F. Macfarlane Burnet, 1899–1985, Австралия) и Питер Медавар (Peter В. Medawar, 1915–1987, Великобритания) — Нобелевская премия 1960 г. за исследования по искусственной индукции иммунологической толерантности.
Родни Портер (Rodney R. Porter, 1917–1985, Великобритания) и Джеральд Эдельман (Gerald M. Edelman, 1929, США) — Нобелевская премия 1972 г. за установление химической структуры молекул АТ.
Розалин Ялоу (Rosalyn Yalow, 1921) — Нобелевская премия 1977 г. за разработку конкурентного радиоиммунологического анализа, позволившего определять нано- и пикограммовые количества пептидных гормонов.
Барух Бенацерраф (Baruj Benacerraf, 1920, США), Жан Доссе (Jean Dausset, 1916, Франция) и Джордж Д. Снелл (George D. Snell, 1903, США) — Нобелевская премия 1980 г. за открытие генов и главного комплекса гистосовместимости.
Нилье Йерне (Niels К. Jerne, 1911–1994, Дания) — Нобелевская премия 1984 г. за разработку теории идиотипических сетей. Кроме того, Йерне разработал метод количественного подсчёта антителообразующих клеток. Именно Йерне является первым, кому принадлежит самая фундаментальная и по сей день основная идея иммунологии — идея клональности лимфоцитов, следовательно, клональности любого иммунного ответа.
Георг Кёлер (Georges F. Kohler, 1946–1995, Германия) и Цезарь Мильштейн (Cesar Milstein, 1927–2002, Аргентина–Великобритания) — Нобелевская премия 1984 г. за разработку революционного биотехнологического метода — получения гибридом и моноклональных АТ.
Сузуму Тонегава (Susumu Tonegawa, 1939, Япония) — Нобелевская премия 1987 г. за работы по молекулярной биологии генов иммуноглобулинов и раскрытие механизмов, обеспечивающих разнообразие антигенсвязывающих участков молекул АТ — рекомбинацию ДНК в соматических клетках (лимфоцитах).
Питер Дохерти (Peter Doherty, 1940, США) и Рольф Цинкернагель (Rolf Zinkernagel, 1944, Швейцария) — Нобелевская премия 1996 г. за открытие двойного распознавания в иммунологии — природной функции молекул главного комплекса гистосовместимости.
Стенли Прусинер (Stanley Prusiner, США) — Нобелевская премия 1997 г. за открытие прионов — возбудителей инфекций нового типа, не похожих на известные ранее медицине. К прионным инфекциям относят возбудителей губчатого энцефалита — бешенства коров, заразного и для человека, в том числе по пищевым путям, всколыхнувшего Европу в 1996–1997 гг. Его первые публикации на эту тему были сделаны в 1982 г.
Лиланд Хартуэлл (L. Hartwall, 1939, США), Тимоти Хант (Т. Hunt, 1943, Великобритания), Пол Нерс (P. Nerth, 1949, Великобритания) — Нобелевская премия 2001 г. за исследования генов и их продуктов, контролирующих пролиферацию клеток. Хартуэлл ввел понятие CDC — cell division cycle, оценил количество генов, обеспечивающих деление клетки как не менее 100 и идентифицировал стартовый ген (start), инициирующий переход клетки из фазы G1 в фазу S. Нерс нашёл гены, кодирующие ферменты киназы, обеспечивающие переход клетки в фазу митоза — Хант нашёл в клетке белки — циклины, приводящие в активное состояние киназы Нерса (CDK), каждой киназе — свой циклин. Эти открытия существенным образом способствовали пониманию того, что этиология и патогенез злокачественных опухолей есть проблемы повреждения системы генов CDK.
По прогнозу одного из наиболее уважаемых современных теоретиков иммунологии Чарльза Джанвея, который является также исследователем и преподавателем (он ведущий автор отличного учебника «Immunobiology: immune system in health and disease», переиздаваемого ежегодно с 1994 г.), ближайшей Нобелевской премии по иммунологии заслуживают авторы исследований по молекулярным механизмам эволюционного происхождения процессов перестройки ДНК генов Рц лимфоцитов для Аг. Две независимые группы исследователей получили фактические данные, наводящие на мысль, что инициаторные гены перестройки ДНК — RAG1 и RAG2 — это транспозоны, т.е. ретровирусы по происхождению (отсутствие интронов, характерные последовательности нуклеотидов и т.д.). Инфицировние этими древними вирусами гамет каких-то древних челюстных рыб привнесло полезные для выживания свойства, которые закрепились отбором и превратились со временем в такое биологическое свойство всех вышестоящих многоклеточных, как лимфоцитарный иммунитет.
1.3. Определение понятия «иммунитет»
Латинское слово immunis в современном словаре имеет порядка 10 значений. В медицинском смысле этот термин употребляли ещё до нашей эры в значениях: неприкосновенный, чистый, не затронутый болезнью, невредимый, находящийся под хорошей защитой, устойчивый к заразной болезни. Глагол immunio — укреплять, защищать. Защита от инфекций — главное природное предназначение иммунитета и в нашем понимании. Но иммунитет не единственный биологический механизм защиты организма от инфекций. Есть и другие. Определить именно иммунитет — значит выделить его среди других защитных механизмов как особый, показать его строго уникальные признаки, найти и описать его место и взаимосвязи с другими защитными системами организма.
Из раздела об истории предмета должно было возникнуть ощущение, что иммунитет — некое защитное биологическое свойство живых многоклеточных организмов, предохраняющее эти организмы от инфекционных болезней.
Несмотря на то что как медицинский термин «immunis» употребляли врачи до нашей эры, принципиально в том же смысле, что и сейчас, в современной иммунологии как науке и медицинской специальности отнюдь нет ясного и общепринятого понимания, чтo же такое именно иммунитет. Всякое ли защитное биологическое свойство — иммунитет? Сразу скажем — нет. Какие ещё есть защитные биологические свойства и чем иммунитет отличается от них и как с ними взаимосвязан? Нередко иммунитету приписывают то, что по сути иммунитетом не является, а относится к другим биологическим свойствам защитного назначения. Иммунитет — это особое свойство организма. Есть определённые признаки, по которым иммунитет можно отличить от других защитных свойств того же организма, сосуществующих с иммунитетом и находящихся с ним также в весьма определённых взаимоотношениях. От чего необходимо защищаться многоклеточному организму в целях сохранения своей жизни как целостности? Во-первых, от проникновения во внутреннюю среду травмирующих собственные клетки субстанций из внешней среды. Во-вторых, от внешних веществ, уже проникших во внутреннюю среду. B–третьих, от собственных повреждённых клеток или выполнивших свою биологическую программу клеток.
Существует несколько биологических механизмов защиты многоклеточных организмов от патогенов внешней среды. Из множества этих механизмов лишь один является иммунитетом. Поскольку организм — единое целое, разные защитные механизмы взаимосвязаны и дополняют друг друга, но это не значит, что они неотличимы один от другого. Мы неоднократно привлекаем внимание к чёткому выделению понятий потому, что в подавляющем большинстве специальной литературы по иммунологии термин «иммунитет» применяют к разным, подчас любым проявлениям защиты организма от внешних патогенов. Это побуждает упорядочить наши понятия и определить иммунитет так, чтобы его можно было отличить от любого другого защитного механизма (поведенческих реакций, покровных тканей, сосудистых реакций, бактерицидных компонентов жидких секретов, белков острой фазы, фагоцитоза — все это существует и у организмов, у которых нет иммунной системы, следовательно, и иммунитета). Начиная с челюстных рыб, у многоклеточных появились особые клетки — лимфоциты, с ними и особый новый механизм защиты — иммунитет.
Собственно иммунитетом мы будем называть только и исключительно те защитные процессы, которые реализуются с участием лимфоцитов. Остальные защитные механизмы связаны и с иммунитетом, и между собой в едином организме, работают вместе. Но они различимы, и каждый характеризуется особыми признаками, позволяющими отличать один от другого.
Иммунитет — эволюционно самое новое и самое тонконастраивающееся из подсознательных защитных свойств многоклеточных. Носителем нового свойства стали тоже новые, особые дифференцированные клетки — лимфоциты.Появившись последним, иммунитет опирается и вписывается, сопрягается со всеми остальными защитными системами многоклеточных, работает не отдельно от них, а исключительно вместе с ними.
Лимфоцитарный иммунитет появился, начиная с челюстных рыб, и закрепился отбором. Таким образом, лимфоцитарный иммунитет существует примерно у 1,5% видов многоклеточных организмов, но именно у тех видов, особи которых оставляют относительно малое количество потомков и поэтому для сохранения вида существенны выживание и здоровье каждой особи.
Поскольку наш курс иммунологии целенаправлен на медицину, мы не будем отвлекаться на конкретные свойства иммунной системы у животных разных видов: все, о чем мы будем говорить, относится только к человеку и млекопитающим. Из млекопитающих исключительным «иммунологическим» видом являются мыши — непревзойденные и незаменимые экспериментальные животные в иммунологии. Удобство мышей как экспериментальных животных в иммунологии объясняется 3 главными причинами. Первая — высокая степень гомологии биологических свойств иммунной системы у человека и мыши. Вторая — короткий срок беременности у мышей (21 сут) по сравнению с периодом трудоспособности естествоиспытателя и число потомков у одной самки от одной беременности от 5 до 7 позволили вывести множество инбредных линий мышей с теми или иными заданными свойствами. Третья — малые размеры и неприхотливость в еде обусловливают относительно невысокую стоимость их содержания, т.е. экономическую рентабельность.
Итак, что же такое иммунитет как защитное свойство многоклеточных организмов? От чего защищает иммунитет многоклеточных? Что нового появилось у многоклеточных по сравнению с одноклеточными, от чего многоклеточных надо защищать в целях выживания и сохранения собственной целостности единого организма? Многоклеточный организм надо защищать (очищать) в первую очередь от агрессивных инфекционных микроорганизмов и гельминтов. Кроме того, защищать от онтогенетически отживших и повреждённых, травмированных собственных клеток, от агрессивного проникновения во внутреннюю среду через барьерные ткани (ЖКТ, слизистые оболочки дыхательной и выделительной систем, кожу) пищевых веществ и ингаляционных и аппликаторных веществ из окружающей среды (рис. 1.1).
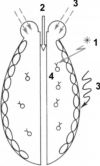
Рис. 1.1. Многоклеточный организм: защита внутренней среды от факторов внешней среды. Многоклеточному организму необходимо защищать свою внутреннюю среду от деструктивного проникновения следующих веществ и объектов из внешней среды: 1 — инфекции; 2 — нерасщеплённые пищевые вещества; 3 — ингаляторные и аппликаторные вещества; 4 — лимфоциты, специализированные клетки, «антимикробы» внутри организма с самым большим популяционным разнообразием поверхностных «распознающих» Рц.
Распознавание и элиминация из организма собственных, но ненужных клеток (в первую очередь повреждённых инфекцией, травмированных), т.е. некое уникальное самораспознавание и явилось тем новым эволюционным приобретением многоклеточных, которое стало и продолжает быть базисной функцией новой системы клеток многоклеточных — иммунной системы. Возник и прочно закрепился в эволюции некий определённый механизм молекулярного распознавания. В основе этого механизма — уникально устроенные гены и синтезированные по их программе уникальные белки. Работают эти уникальные гены только и исключительно в единственном типе дифференцированных клеток многоклеточных — в лимфоцитах. Более того, поиск сходным образом устроенных и работающих генов (процесс соматической рекомбинации ДНК) в самых разных эукариотических клетках, начиная с грибов и простейших, пока не выявил ни одного аналога.
Реакция иммунной системы на трансплантат — в отличие от реакций на микроорганизмы неестественная, неприродная, но «предложенная» иммунной системе антропогенными действиями по трансплантациям, переливаниям крови и введениям кровепродуктов, т.е. артефакт. В естественной природе нет процессов, при которых рожденные дефинитивные особи обмениваются между собой органами, кровью (парентерально). Это существенно, а не просто констатация ситуации. Отсутствие природных процессов в эволюционном «анамнезе» обязывает иметь в виду, что в эволюции многоклеточных в их иммунной системе не мог идти отбор приспособительных защитных механизмов в отношении факторов, связанных с трансплантацией тканей других организмов во внутреннюю среду данной особи. Принципиальная неспособность иммунной системы млекопитающих контролировать ретровирусные инфекции (а это кровяные инфекции) связана, весьма вероятно, в значительной мере как раз с тем, что широкое распространение среди людей этих инфекций пошло неприродными путями, но ятрогенно и фармакогенно (с переливаниями крови и введением кровепрепаратов).
1.3.1. Резистентность к инфекциям и продуктам повреждения тканей. Физиологические защитные системы организма. Место иммунитета
Биологической основой освобождения многоклеточного организма от продуктов повреждения собственных клеток и от инфекций стали биохимические механизмы пищеварительной функции одноклеточных, т.е. ферментативные системы расщепления (протеазы, гидролазы), перекисного окисления, нитрования природных макромолекул до низкомолекулярных продуктов распада, которые клетка способна выбросить через мембрану во внешнюю среду. У многоклеточных во внутренней среде появились специализированные для расщепительно-литических процессов клетки (в первую очередь фагоциты, затем и все остальные лейкоциты общевоспалительного назначения), а также особые гуморальные ферментативные системы литического назначения в сыворотке крови и тканевых жидкостях (комплемент, лизоцим и др.). Это доиммунные механизмы физиологической резистентности к инфекциям и продуктам повреждения собственных клеток. Литические биохимические механизмы агрессивны по сути. Поэтому в норме они не могут постоянно пребывать в активном состоянии или даже в близкой готовности к активизации, иначе будут лизировать «все подряд». Вот для того чтобы распознать, в каком месте в организме и в какой момент времени надо «включить» санирующие литические механизмы, природа и создала новые клетки — лимфоциты с новой функцией — молекулярного распознавания. С лимфоцитами появился новый механизм биологической защиты от повреждённых клеток и от инфекций — иммунитет.
Одна из причин, по которым в иммунологии как научной дисциплине распространены разное толкование терминов и не всегда точное их употребление даже специалистами, лингвистическая. Основной поток научной информации в этой области знаний в XX–XXI в. идёт на английском языке, который по сравнению с латинским и русским языками меньше «заботится» о взаимно однозначном соответствии термина и явления природы или объекта. Поэтому то, что привычно устраивает англоязычное мышление, не всегда удовлетворяет русскоязычной логике. Например, в английском языке используют термин «врождённый иммунитет» (innate [natural] immunity). Под этим понимают то, что мы назвали доиммунными механизмами резистентности, а именно это вполне определённый перечень клеток, молекул и физиологических механизмов (бактерицидные ферменты биологических жидкостей, фагоцитоз, система комплемента и т.п.). Однако не эта материя лежит в основе практики античных китайцев, греков, оспоинокуляторов, работ современных иммунологов. То, что лежит в основе практики античных китайцев и остальных перечисленных выше исследователей, в современном английском называют приобрётенным иммунитетом (acquired immunity).
Для удовлетворения потребностей русскоязычной логики, а также следуя представлениям древних, мы предлагаем называть материю, которая в английском названа innate immunity, не иммунитетом, а резистентностъю с указанием конкретного определения (прилагательного) — системы комплемента, лизоцима, фагоцитоза, эозинофильной цитотоксичности и т.д. А иммунитетом называть то биологическое свойство, которому соответствуют глагол — иммунизировать, существительное — иммунизация, прилагательное — иммунный. За этим свойством «стоит» особая система особых клеток—лимфоцитов, развившихся в эволюции позже тех клеток и их продуктов, которые обеспечивают врождённую резистентность (к инфекциям и инвазиям).
Эта система и есть иммунная система. Анатомический синоним иммунной системы — лимфоидная система. И эти особые, эволюционно новые клетки с новым уникальным свойством — молекулярного распознавания — лимфоциты и только они. Кстати, лимфоциты и их свойства, включая генерацию разнообразия Рц, также врождённые, т.е. генетически предопределённые. То, что попадание патогена в организм индуцирует размножение лимфоцитов и усиленный (вторичный) ответ при повторном попадании того же патогена, есть биологический механизм функционирования системы лимфоцитарного иммунитета, а не свойство генетической врождённости/приобрётенности.
Лимфоциты взаимодействуют со всеми клетками системы крови, сосудов, по которым и через стенку которых лимфоциты попадают в ткани. Лимфоциты способны вступать в контакты со всеми клетками организма. Лимфоциты через специальные Рц воспринимают информацию от нервной системы, эндокринной системы, об уровне глюкозы в крови и т.д.
Но это не значит, что иммунная (лимфоцитарная) система сливается до неразличимости со всем организмом и в список иммуноцитов надо включать клетки эндотелия венул, фибробласты рыхлой соединительной ткани и т.д. У лимфоцитарного иммунитета есть вполне конкретные и ясные свойства, по которым он может быть идентифицирован как особое биологическое свойство многоклеточных организмов. Лимфоциты функционируют не сами по себе, где-то вне организма, следовательно, их взаимосвязи с другими клетками, тканями и органами в целостном организме — единственно возможная реальность. Более того, лимфоцит, специально дифференцированный для уникальной функции распознавания, все свои клеточные «силы» отдает именно этой функции, а доведение дела защиты организма от того, что распознал лимфоцит, он «передает» другим клеткам [за исключением только цитотоксических лимфоцитов — T и NK (нормальных киллеров)].
Дата добавления: 2016-07-18; просмотров: 2284;











