Краткое теоретическое обоснование
Порогом коагуляции называется минимальное количество электролита, которое надо прибавить к золю, чтобы вызвать явную коагуляцию(т.е. различимой глазом)– помутнение раствора или изменение его окраски.
Порог коагуляции / 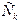 / можно рассчитать по формуле:
/ можно рассчитать по формуле: 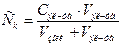 , где
, где 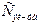 – исходная концентрация электролита;
– исходная концентрация электролита; 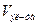 – объем раствора электролита, добавленного к золю;
– объем раствора электролита, добавленного к золю; 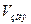 – объем исходного золя. Величину, обратную порогу коагуляции, называют коагулирующим действием и определяют по формуле:
– объем исходного золя. Величину, обратную порогу коагуляции, называют коагулирующим действием и определяют по формуле: 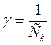
Отношение порогов концентрационной коагуляции для ионов разных зарядов найдено теоретически Б.В. Дерягиным и Л.Д. Ландау и названо законом 6-й степени. Они показали, что энергетический барьер между коллоидными частицами исчезает ( 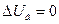 ) при достижении критической концентрации /
) при достижении критической концентрации / 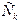 /, которая обратно пропорциональна шестой степени заряда иона- коагулянта:
/, которая обратно пропорциональна шестой степени заряда иона- коагулянта: 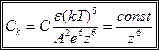 , где С — константа, зависящая от числа зарядов катиона и аниона;
, где С — константа, зависящая от числа зарядов катиона и аниона; 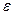 (
( 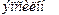 ) — диэлектрическая проницаемость раствора; А — константа сил притяжения; е — заряд электрона (т.е. валентность иона– коагулятора).
) — диэлектрическая проницаемость раствора; А — константа сил притяжения; е — заряд электрона (т.е. валентность иона– коагулятора).
Согласно 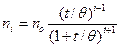 , соотношение порогов коагуляции одно-, двух- и трехзарядных ионов имеет вид.
, соотношение порогов коагуляции одно-, двух- и трехзарядных ионов имеет вид. 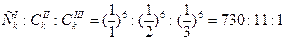 .
.
/где 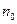 – первоначальное число частиц; i – порядок (одиночные, двойные, тройные и т.д.), t- время от начала коагуляции;
– первоначальное число частиц; i – порядок (одиночные, двойные, тройные и т.д.), t- время от начала коагуляции; 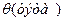 – время половинной коагуляции, в течение которого число частиц уменьшается вдвое против начального/,
– время половинной коагуляции, в течение которого число частиц уменьшается вдвое против начального/,
Правило Щульце –Гардии на основании опытных данных дает для тех же ионов соотношение: 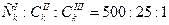 .
.
Как видно, в первом приближении эти ряды согласуются между собой. Некоторое расхождение результатов можно объяснить увеличением роли специфической адсорбции у многозарядных ионов, что не учитывается «Теорией устойчивости гидрофобных дисперсных систем ДЛФО» (ДЛФО– это в соответствии с первыми буквами фамилий авторов Дерягина, Ландау, Фервейа, Овербега).
Таким образом, эмпирическое правило Шульце—Гарди получило теоретическое обоснование. В то же время следует отметить, что сложные органические катионы (алкалоиды, красители) проявляют высокую коагулирующую способность вне связи с валентностью, т. е. такие ионы не укладываются в рамки правила Шульце—Гарди.
Необходимо иметь в виду, что величина порога коагуляции зависит от ряда условий:
Þ от момента его фиксирования после внесения электролита;
Þ от метода наблюдения;
Þ от концентрации исследуемого золя и др.
Наиболее распространенные методы определения порога коагуляция состоят в наблюдениях за изменением светорассеяния (через определенное время после смешивания золя с электролитом).
Задача №3.Как изменится порог коагуляции золя 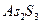 , если для коагуляции
, если для коагуляции 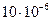
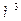 золя потребуется
золя потребуется 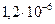
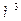 раствора
раствора 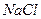 с концентрацией 0,5
с концентрацией 0,5 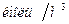 ? Определите порог коагуляции под действием раствора
? Определите порог коагуляции под действием раствора 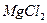 концентрацией 0,036
концентрацией 0,036 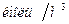 , которого потребуется
, которого потребуется 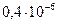
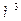 на
на 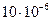
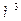 золя и раствора
золя и раствора 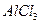 концентрацией 0,01
концентрацией 0,01 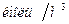 , которого потребуется
, которого потребуется 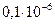
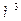 на
на 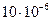
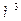 золя. Проверьте выполнение условия:
золя. Проверьте выполнение условия:
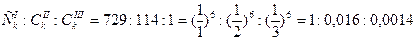 .
.
Решение.
1. 
 Из формулы расчета порога коагуляции
Из формулы расчета порога коагуляции 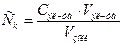 /формула справедлива при
/формула справедлива при 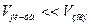 /, следует:
/, следует:
а) 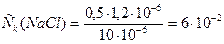
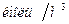 .
.
б) 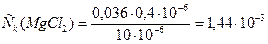
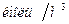 .
.
в) 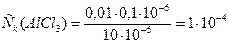
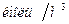 .
.
Как видно, согласно правилу Шульце – Гарди, с увеличением заряда иона –коагулятора порог коагуляции уменьшается, а коагулирующая способность при этом возрастает.
2. Из полученных результатов следует:
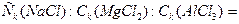
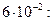
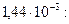
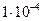
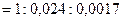 , что условие коагуляции разноименно заряженными ионами удовлетворительно выполняется.
, что условие коагуляции разноименно заряженными ионами удовлетворительно выполняется.
Ответ. Согласно правилу Шульце – Гарди, с увеличением заряда иона –коагулятора порог коагуляции уменьшается и условие коагуляции разноименно заряженными ионами выполняется.
Дата добавления: 2020-07-18; просмотров: 926;











