Методы химической конденсации
В этих методах новая фаза образуется при протекании гомогенных химических реакций, приводящих к образованию нерастворимых в данной среде веществ. Это могут быть реакции восстановления, окисления, обмена, гидролиза и т.д.
Как правило, высокодисперсные частицы получают добавлением в разбавленный раствор одного из реактивов при интенсивном перемешивании небольшого количества раствора второго реактива.
Таким образом, один из исходных реагентов должен быть взят в избытке, чтобы служить стабилизатором получаемого лиозоля. Если вещества будут взяты в эквивалентных количествах, то золь не образуется.
Примером образования дисперсных систем с помощью метода химической конденсации могут служить следующие процессы:
1) получение гидрозоля серы окислением сероводорода сернистой кислотой:
2H2S + H2SO3 = 3S↓ + 3H2O;
2) получение золя хлорида серебра с помощью реакции ионного обмена, протекающей при смешивании разбавленных растворов хлорида натрия и нитрата серебра:
NaCl + AgNO3 = AgCl↓ + NaNO3;
3) получение золя гидроксида железа (III) реакцией гидролиза при повышенной температуре:
FeCl3 + 3H2O 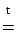 Fe(OH)3↓ + 3HCl
Fe(OH)3↓ + 3HCl
Методы химической конденсации лежат в основе образования коллоидных частичек растворенных веществ в биологических жидкостях. Поэтому изучение механизма данного процесса, возможностей его регулирования имеет большое значение для биологии и медицины.
Очистка золей
Полученные тем или иным способом коллоидные растворы (особенно с помощью метода химической конденсации) практически всегда содержат определенное количество низкомолекулярных соединений в виде примесей. В их роли могут выступать: избыток одного из исходных реагентов, образующийся в ходе реакции побочный продукт, добавляемый для повышения устойчивости системы стабилизатор и т.п.
Так, например, при получении золя хлорида серебра обменной реакцией между NaCl и AgNO3 в качестве побочного продукта образуется электролит NaNO3, остается неизрасходованный избыток одного из исходных веществ.
Примеси оказывают определенное влияние на свойства золей, снижают их устойчивость, поэтому коллоидные растворы необходимо от них очищать.
Для очистки золей от примесей нежелательных низкомолекулярных соединений применяют диализ или ультрафильтрацию.
Диализ основан на способности молекул или ионов малых размеров проходить через полупроницаемые пленки или мембраны, тогда как крупные частицы дисперсной фазы такой способностью не обладают.
Полупроницаемыми являются различные растительные, животные и искусственные мембраны. Их можно приготовить из пергамента, бычьего, свиного, рыбьего пузыря, коллодия, целлофана и т.д.
Приборы, в которых осуществляется диализ, называются диализаторами. Простейший из них, предложенный еще в 19 веке английским химиком Т. Грэмом, состоит из вставленных друг в друга стеклянных сосудов (рис. 51). Дно либо боковая стенка одного из них (внутреннего) затянуты полупроницаемой мембраной. В этот сосуд помещают очищаемый гидрозоль. В другой сосуд (внешний) наливают дистиллированную воду, которую периодически или непрерывно заменяют.
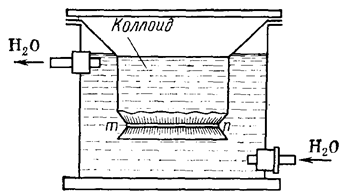
Рис. 51. Схема простейшего диализатора: тп – полупроницаемая перепонка (мембрана)
За счет диффузии низкомолекулярные примеси постепенно переходят через мембрану из золя во внешний сосуд с растворителем.
Недостатком данного метода является большая длительность процесса очистки (в течение нескольких суток).
Если в качестве низкомолекулярных примесей выступают электролиты, то скорость очистки можно существенно увеличить используя для этого постоянный электрический ток. Такой процесс называется электродиализом. Он проводится в диализаторе другой конструкции, представляющем собой сосуд, разделенный двумя полупроницаемыми мембранами (М) на 3 камеры (рис. 52).
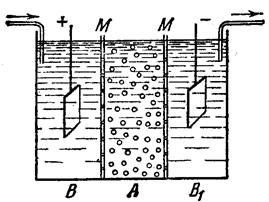
Рис. 52. Схема электродиализатора
В среднюю камеру (А) наливают коллоидный раствор, а в боковые (В и В1) – дистиллированную воду и помещают в них электроды, подключенные к соответствующим полюсам источника постоянного тока. Под действием электрического поля ионы, содержащегося в золе электролита, проходят через полупроницаемые мембраны в боковые камеры к соответствующим электродам и уносятся из сосуда потоком воды. Чем больше разность потенциалов между электродами, тем выше скорость диализа и меньше время очистки (от нескольких часов до нескольких минут).
Недостатком электродиализа является то, что с его помощью нельзя очистить золь от примесей неэлектролитов.
Более универсальным методом очистки золей является ультрафильтрация. В нем удаление примесей осуществляется через специально приготовленные плотные фильтры или мембраны, непроницаемые для коллоидных частиц.
Дата добавления: 2020-07-18; просмотров: 951;











