Гормоны щитовидной железы. Тироидные гормоны
Щитовидная железа построена из 2-х типов клеток: фолликулярных и
парафолликулярных. В соответствии с этим она вырабатывает 2 вида гормонов: тироидные и тирокальцитонин. Первые включают в свой состав йод, что зависит от количественного поступления йодидов с пищей и водой. Суточная потребность галогена составляет 100-200 мкг. В мембранах фолликулов активно функционируют йодидные насосы. Поступая в цитозоль, йодиды под влиянием йодпероксидазы окисляются до молекулярного йода:
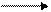 Н2О2
Н2О2
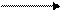
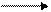
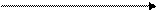 2 I- I2
2 I- I2
НАДФН+Н+ 2Н2О
В это время на рибосомах идёт синтез специфического белка – гликопротеида – тироглобулина, включающего большое количество остатков тирозина. Его посттрансляционная модификация заключается в йодировании тирозинов. С помощью йодпероксидазы йод включается в остатки аминокислоты по 3-ему и по 5-ому положениям с образованием монойод- и дийодтирозинов. Затем идёт реакция конденсации с участием конденсирующего фермента, приводящая к синтезу трийод- (Т3) и тетрайодтиронинов (тироксина, Т4) в тироглобулине. Весь процесс регулируется ТТГ гипофиза, который активирует ДНК-полимеразу, запускающую репликацию и митозы фолликулов щитовидной железы; стимулирует йодидные насосы, работу ферментов синтеза тироидных гормонов, специфических протеаз, высвобождающих их в кровь, где они связываются с α1-, α2-глобулинами плазмы. В свободном виде Т3 и Т4 транспортируются не более 1%.
Практически все клетки для тироидных гормонов эффекторные (печень, почки, миокард, головной мозг, мышцы, лимфоидная ткань). Тироксин является прогормоном, так как его активность в несколько раз слабее, чем у Т3. В печени, почках, головном мозге, миокарде и щитовидной железе локализуется дейодиназа, которая катализирует конверсию (преобразование) Т4 в трийодтиронин. Одним из основных компонентов активного центра данного энзима является селен-цистеин, что следует учитывать в местностях с дефицитом этого микроэлемента.
Механизм действия
Щитовидная железа начинает функционировать у плода на 13-14-ой неделе. Тироидные гормоны слабополярны, поэтому обладают внутриклеточной рецепцией. Легко преодолевают ядерную и митохондриальную мембраны, взаимодействуют с ГЧЭ определённых генов, обеспечивая их экспрессию или, наоборот, репрессию. Стимулируют не только транскрипцию и трансляцию, но и деление клеток, дифференцировку тканей, в том числе и нервной системы.
Тироидные гормоны регулируют, в первую очередь, энергетический обмен. Стимулируют работу ионных каналов, изменяя потенциал мембраны: увеличивают её проницаемость, особенно у митохондрий, для окисляемых субстратов и кислорода. Ускоряют синтез ферментов ЦТК, ЭТЦ, но не влияют на скорость окислительного фосфорилирования. Поэтому при повышенных концентрациях тироидные гормоны усиливают высвобождение энергии, в том числе и тепловой, но захват её в окислительном фосфорилировании непропорционально низок; возникает чувство жара (калорический эффект).
Повышают интенсивность гидролитической фазы катаболизма: распад гомополисахаридов (гликогена), гликозаминогликанов и гетерополисахаридов. При активации гликогенолиза может развиться гипергликемия (тироидный диабет). При недостатке тироидных гормонов гликозаминогликаны накапливаются в основном в соединительной ткани. За счёт многочисленных ОН-групп они легко образуют водородные связи, в том числе с молекулами воды, поэтому удерживают её в тканях, что провоцирует возникновение отёка слизистых (микседемы). Т3 усиливает скорость начальной стадии распада липидов: стимулирует ТАГ-липазу; в митохондриях активирует ферменты β-окисления ВЖК, повышает активность глицеролфосфатДГ, окисляющей глицерол-1-фосфат.
В физиологических концентрациях тироидные гормоны обладают анаболическим эффектом, то есть способствуют синтезу тканевых протеинов. Но при высоких величинах Т3 и Т4 начинают активировать клеточные протеазы (катепсины), ответственные за распад белков.
Патология
Среди приобретённых, врождённых и наследственных заболеваний щитовидной железы по количественному направлению эффектов выделяют: гипертироз (тиротоксикоз), гипотироз, эутироидные состояния.
Гипертироз –болезнь Грейвса, в основе которой лежат аутоиммунные процессы: у пациентов синтезируются иммуноглобулины к рецепторам ТТГ в мембранах фолликулов щитовидной железы. Образовавщийся комплекс (антиген + антитело) обладает повышенной аффинностью к ТТГ, что при его физиологических величинах приводит к развитию зоба. Усиленная секреция тироидных гормонов провоцирует различные симптомы: повышенную эмоциональность, плаксивость, раздражительность, быструю смену настроения; чувство жара (калорический эффект), похудание (усилены катаболические фазы всех обменов), пучеглазие (экзофтальм), тахикардию. В плазме крови регистрируются гипергликемия, гипераминоацидемия, гиполипемия.
Примергипотироза –зоб Хашимото–также аутоиммунное заболевание. Образуются антитела к ферментам синтеза тироидных гормонов, в результате снижается их секреция. По принципу «+» - «-» взаимодействия стимулируется выброс ТТГ, который активирует деление фолликулов щитовидной железы (зоб). Но избыточного генеза тироидных гормонов не происходит. Поэтому клиника прямо противоположна болезни Грейвса: поражение ЦНС (апатия, равнодушие, сонливость, бедная эмоциональная окраска), зябкость (угнетение энергетического обмена), ожирение, вследствие подавления липолиза; из-за замедления распада ГАГ, входящих в состав различных видов соединительной ткани, они накапливаются и удерживают воду, возникает – микседема. Основные биохимические сдвиги в крови: гипогликемия, гиперлипемия, гиперхолестеролемия, повышенное содержание ВЖК.
Эутироидные состояния:среди эндокринной патологии у людей, живущих в биогеохимических провинциях с дефицитом йода, (иногда в сочетании с недостатком селена, - Забайкалье), развивается эндемический зоб. Синтез тироидных гормонов определяется поступлением этих биотиков с пищей и водой. Из-за их недостатка в крови, которая омывает гипоталамус, по типу обратной связи стимулируется секреция тиролиберина, активирующая выделение ТТГ гипофиза. Последний ускоряет митозы фолликулов щитовидной железы (зоб). При этом её функция не нарушается, так как за единицу времени через увеличенную массу железы протекает большее количество крови, которая доставляет достаточные величины йода. Возникает эутироидное состояние, но это равновесие хрупкое. В любой момент может развиться или гипо-, или гиперсекреция тироидных гормонов.
Практически везде на планете в почвах и воде - неблагоприятная экологическая обстановка, характеризующаяся сниженными величинами йода и избытком микроэлементов, которые являются его антагонистами (молибден, мышьяк и другие). Некоторые растения (редька, капуста – крестоцветные) захватывают йод и нарушают его всасывание (биодоступность).
Около 1 млрд. человек на Земном шаре страдают йоддефицитными заболеваниями. Выделяют различные формы этих недугов: эндемический зоб, врождённые глухота, немота, гипотироидизм новорождённых, эндемический кретинизм. У беременной, проживающей в биогеохимической провинции с недостатком йода и селена, страдающей эндемическим зобом, высока вероятность рождения ребёнка с врождённой патологией щитовидной железы.
Наследственная патология –болезнь Pendrеd; в её основе лежит мутация в гене, ответственном за синтез белка пендрина, который регулирует образование тироидной пероксидазы. У пациентов снижается концентрация тироидных гормонов в крови. Основные симптомы – глухота, зоб с признаками гипотироза.
Тирокальцитонин
Это второй гормон щитовидной железы, который вырабатывается парафолликулярными клетками, расположенными между фолликулами. Его основное предназначение – регуляция обмена ионов кальция. (Отсюда необходимо кратко остановиться на судьбе их в организме).
Метаболизм и роль кальция. Поступает с водой и пищей (в основном, с молоком и молочными продуктами: сыром, творогом). После всасывания в кишечнике 99% Ca2+ связывается с фосфатами, образуют кристаллическую решётку гидроксиапатита в хрящевой и костной тканях, что составляет депо кальция; 1% Ca2+ содержится во внеклеточной жидкости, в том числе и плазме крови, где существует в трёх видах: связанным с белками, анионами минеральных и органических кислот. Свободный, или ионизированный кальций – это самая важная форма, так как она наиболее активна. В норме её уровень в крови составляет 1,1 – 1,3 ммоль/л. Соли кальция выводятся через почки и в составе желчи через ЖКТ.
Это внеклеточный катион. Попадая в клетки, Ca2+ выполняет следующие функции. Является компонентом гидроксиапатита костной ткани, которая образует скелет. Регулирует работу актин-миозинового комплекса, осуществляющего мышечное сокращение. Служит IV фактором свёртывания крови. Участвует в проведении нервного импульса. Воздействует на скорость диффузии различных веществ через мембраны (секрецию пищеварительных соков, гормонов, работу ионных каналов). Является second-messender. Стабильность уровня кальция обеспечивается балансом тирокальцитонина, паратгормона, кальцитриола. Основные органы-мишени, через которые регулируется обмен макроэлемента: кишечник, костная ткань, почки.
Тирокальцитонин - гормон пептидной природы, вырабатывается в неактивной форме. Его созревание и посттрансляционная модификация происходят постадийно путём частичного протеолиза:
 препротирокальцитонин (139 а/к) протирокальцитонин ти-
препротирокальцитонин (139 а/к) протирокальцитонин ти-
пептид пептид
рокальцитонин (32 а/к).
Механизм действия
Основные органы-мишени: кишечник, костная ткань, почки. Обладает трансмембранной рецепцией, активируя аденилатциклазу. Секреция тирокальцитонина усиливается при гиперкальциемии (при содержании свободного Ca2+ в крови выше, чем 1,3 ммоль/л). В кишечнике он подавляет скорость всасывания кальция. В костной ткани активирует работу остеобластов; усиливает минерализацию костей за счёт накопления кальция и фосфатов и формирования кристаллической решётки; ингибирует остеокласты. В почках угнетает реабсорбцию кальция, но стимулирует выведение магния.
Патологические состояния, связанные с обменом тирокальцитонина, не описаны.
Дата добавления: 2020-05-20; просмотров: 755;











