Общее давление и состав пара и жидкости. Законы Коновалова
Как уже рассматривалось, общее давление над идеальным раствором изменяется линейно (рис.2) с изменением состава жидкости. Состав пара отличается от состава равновесной с ним жидкости. Из закона Дальтона следует, что парциальные давления компонентов газовой смеси
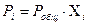 , следовательно:
, следовательно: 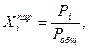 в то время как
в то время как 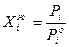

Рисунок - Зависимость общего давления от состава жидкости и пара.
Эти две зависимости обычно изображают на одной диаграмме жидкость - пар (рис.7). Линии жидкости и линия пара делят плоскость диаграммы на три фазовых поля. Верхнее поле - жидкая фаза, нижнее - пар, между этими полями - гетерогенная область находящихся в равновесии жидкости и пара. Например, точка 0 изображает равновесие при общем давления Р, жидкости состава X и пара состава У.
Из рис.7 видно, что в идеальных системах пар по сравнению с равновесной жидкостью всегда обогащен более летучим компонентом, в данном, случае компонентом В. В реальных же растворах не всегда паровая фаза обогащена более летучим компонентом.
Более общая зависимость состава пара от состава жидкости дается первым законом Д.П. Коновалова.
В равновесной системе пар по сравнению с жидкостью обогащен тем компонентом, добавление которого повышает общее давление пара (или понижает температуру кипения раствора при постоянном давлении).
Так в системе, изображенной на рис. 4 и 7, добавление к раствору, например, компонента В приводит к росту общего давления, следовательно, в паре будет содержаться компонента В больше, чем в жидкости. В системе же на рисунке 8 добавление В приводит к росту общего давления лишь до точки С и Сl, а дальнейшее добавление В снижает общее давление, следовательно, до точек С и Сl пар обогащен компонентом В, а после этих точек — компонентом А.
Для систем с экстремумами на кривых Р =f(Х!ж) установлен второй закон Д.П. Коновалова.
Экстремумы на кривых общего давления пара или температуры отвечают такому равновесию раствора и насыщенного пара, при котором состав обеих фаз одинаковы.
По второму закону Коновалова кривая пара и кривая жидкости, имеющие экстремумы, должны касаться в точке экстремума (рис.8).
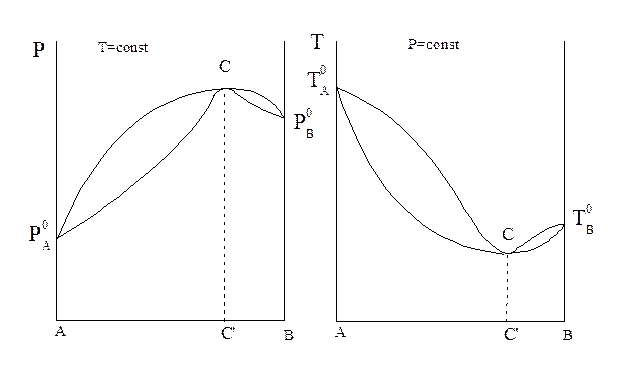
Рисунок 8- Диаграммы общее давление — состав и температура кипения -состав для систем смаксимумом давления пара.
Смеси, у которых составы жидкости и равновесного с ней пара совпадают, называются азеотропными. Они кипят при постоянной температуре. Соотношение между составом пара и составом жидкости часто изображается в координатах 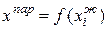 . Диагональ квадрата отвечает равному составу жидкости и пара. Но даже для идеальных систем составы жидкости и пара различны. Если добавление В к раствору повышает общее давление, то В паре будет больше, кривая 1 (рисунок 9) пойдет выше диагонали. Если же пар содержит меньше В, чем жидкость, то кривая 2 пойдет ниже. Системы с азеотропом изображаются S-образной кривой, пересекающей диагональ в точке, отвечающей азеотропу (кривая 3).
. Диагональ квадрата отвечает равному составу жидкости и пара. Но даже для идеальных систем составы жидкости и пара различны. Если добавление В к раствору повышает общее давление, то В паре будет больше, кривая 1 (рисунок 9) пойдет выше диагонали. Если же пар содержит меньше В, чем жидкость, то кривая 2 пойдет ниже. Системы с азеотропом изображаются S-образной кривой, пересекающей диагональ в точке, отвечающей азеотропу (кривая 3).

Рисунок 9 – Соотношение между составом жидкости и пара
Дата добавления: 2016-06-22; просмотров: 2846;











