Химические свойства.
Легко восстанавливается; при нагревании разлагается на ртуть и кислород. Реагирует с кислотами с кислотами с образованием солей и воды.
Сульфид ртути (II) HgS (киноварь) – ярко-красный нерастворимый в воде порошок.
Hg + S  HgS
HgS
Hg2+ + S2-  HgS
HgS
Галогениды.
Получение
Hg + Br2  HgBr2
HgBr2
HgO + 2HCl(сулема)  HgCl2 + H2O
HgCl2 + H2O
Сулему также получают растворением ртути в царской водке.
Химические свойства:
HgI2 + 2KI  K2[HgI4](реактив Несслера)
K2[HgI4](реактив Несслера)
Реактив Несслера используется в качестве очень чувствительного аналитического реагента для обнаружения иона NH4+:
Сульфат ртути (II) и нитрат ртути (II). Получают растворением ртути или оксида ртути (II) в концентрированных серной или азотной кислотах соответственно.
Hg + 2H2SO4(горячая,конц.)  HgSO4 + SO2
HgSO4 + SO2 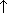 + 2H2O
+ 2H2O
HgO + H2SO4  HgSO4 + H2O
HgSO4 + H2O
3Hg + 8HNO3(конц.)  3Hg(NO3)2 + 2NO
3Hg(NO3)2 + 2NO 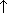 + 4H2O
+ 4H2O
HgO + 2HNO3  Hg(NO3)2 + H2O
Hg(NO3)2 + H2O
Более активные металлы легко вытесняют ртуть из ее солей:
Cu + Hg(NO3)2  Cu(NO3)2 + Hg
Cu(NO3)2 + Hg
Цинк. Физиологическая роль цинка осуществляется благодаря связи его с ферментами. Цинк входит в состав эритроцитов, участвуя в газообмене и тканевом дыхании (ионы цинка входят в состав ферментов карбоангидразы).
Многие соединения цинка используются как вяжущие, антисептические средства для наружного применения.
ZnSO4*7H2O – глазные капли.
ZnO – присыпка, мази, пасты для кожных заболеваний.
Дата добавления: 2016-06-22; просмотров: 2248;











