Химические свойства
Возможные степени окисления
В соединениях медь проявляет две степени окисления: +1 и +2. Первая из них склонна к диспропорционированию и устойчива только в нерастворимых соединениях (Cu2O, CuCl, CuI и т. п.) или комплексах (например [Cu(NH3)2]+. Её соединения бесцветны. Более устойчива степень окисления +2, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5. Последняя встречается в солях купраборанового аниона Cu(B11H11)23−, полученных в 1994 году.
Простое вещество
Не изменяется на воздухе в отсутствие влаги и диоксида углерода. Является слабым восстановителем, не реагирует с водой, разбавленнойсоляной кислотой. Переводится в раствор кислотами-неокислителями или гидратом аммиака в присутствии кислорода, цианидом калия. Окисляется концентрированными серной и азотной кислотами, «царской водкой», кислородом, галогенами, халькогенами, оксидаминеметаллов. Реагирует при нагревании с галогеноводородами.
На влажном воздухе медь окисляется, образуя основный карбонат меди(II):
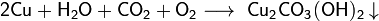
Реагирует с концентрированной холодной серной кислотой:
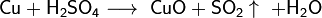
С концентрированной горячей серной кислотой:
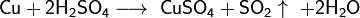
С безводной серной кислотой при 200 °C:
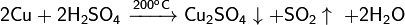
C разбавленной серной кислотой при нагревании в присутствии кислорода воздуха:
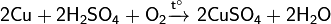
Реагирует с концентрированной азотной кислотой:
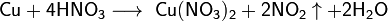
С разбавленной азотной кислотой:
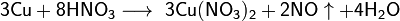
С царской водкой:
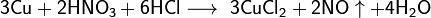
С концентрированной горячей соляной кислотой:
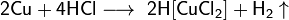
C разбавленной хлороводородной кислотой в присутствии кислорода:
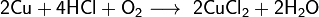
С газообразным хлороводородом при 500—600 °C:
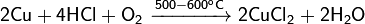
С бромоводородом:
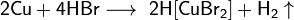
Также медь реагирует с концентрированной уксусной кислотой в присутствии кислорода:

Медь растворяется в концентрированном гидроксиде аммония, с образованием аммиакатов:

Окисляется до оксида меди(I) при недостатке кислорода и 200 °C и до оксида меди(II), при избытке кислорода и температурах порядка 400—500 °C:
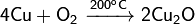
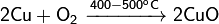
Медный порошок реагирует с хлором, серой (в жидком сероуглероде) и бромом (в эфире), при комнатной температуре:
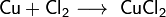
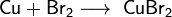
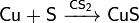
При 300—400 °C реагирует с серой и селеном:
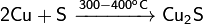
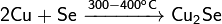
C оксидами неметаллов:
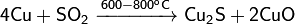
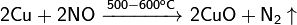
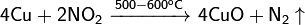
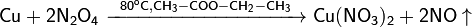
Медь реагирует с цианидом калия с образованием дицианокупрата(I) калия, щелочи и водорода:
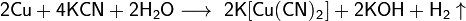
С концентрированной соляной кислотой и хлоратом калия:
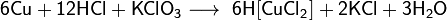
Соединения меди(I)
Степени окисления +1 соответствует оксид Cu2O красно-оранжевого цвета. Соответствующий гидроксид CuOH (жёлтого цвета) быстро разлагается с образованием оксида. Гидроксид CuOH проявляет основные свойства.
Многие соединения меди +1 имеют белую окраску либо бесцветны. Это объясняется тем, что в ионе Сu+ все пять Зd-оны меди(I) в водном растворе неустойчивы и легко диспропорционируют:
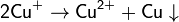
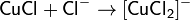
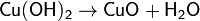
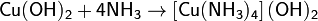
Серебро́ — элемент 11 группы (по устаревшей классификации — побочной подгруппы первой группы), пятого периодапериодической системы химических элементов Д. И. Менделеева, с атомным номером 47. Обозначается символом Ag(лат. Argentum).
Простое вещество серебро (CAS-номер: 7440-22-4) — ковкий, пластичный благородный металл серебристо-белого цвета.Кристаллическая решётка — гранецентрированная кубическая. Температура плавления — 962 °C, плотность — 10,5 г/см³.
Дата добавления: 2016-06-22; просмотров: 2604;











