Графики изотермического процесса
Вообще, графики термодинамических процессов принято изображать в следующих системах координат:
pV-диаграмма: ось абсцисс V , ось ординат p;
V T-диаграмма: ось абсцисс T, ось ординат V ;
pT-диаграмма: ось абсцисс T, ось ординат p.
График изотермического процесса называется изотермой.
Изотерма на pV-диаграмме — это график обратно пропорциональной зависимости p = constV. Такой график является гиперболой (вспомните алгебру — график функции 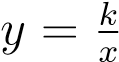 ). Изотермагипербола изображена на рис. 7.
). Изотермагипербола изображена на рис. 7.
| V |
| p |
| изотерма |
Рис. 7. Изотерма на pV-диаграмме
Изобарный процесс
Напомним ещё раз, что изобарный процесс — это процесс, проходящий при постоянном давлении. В ходе изобарного процесса меняются лишь объём газа и его температура.
Типичный пример изобарного процесса: газ находится под массивным поршнем, который может свободно перемещаться. Если масса поршня M и поперечное сечение поршня S, то давление газа всё время постоянно и равно
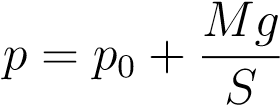 ,
,
где p0 — атмосферное давление.
Пусть идеальный газ совершает изобарный процесс при давлении p. Снова рассмотрим два произвольных состояния газа; на этот раз значения макроскопических параметров будут равны p,V1,T1 и p,V2,T2.
Выпишем уравнения состояния:
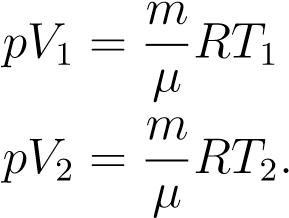 ,
,
Поделив их друг на друга, получим:
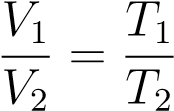 .
.
В принципе, уже и этого могло бы быть достаточно, но мы пойдём немного дальше. Перепишем полученное соотношение так, чтобы в одной части фигурировали только параметры первого состояния, а в другой части — только параметры второго состояния (иными словами, «разнесём индексы» по разным частям):
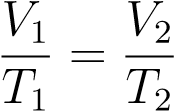 .
.
А отсюда теперь — ввиду произвольности выбора состояний! — получаем закон Гей-Люссака:
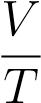 = const.
= const.
Иными словами, при постоянном давлении газа его объём прямо пропорционален температуре: V = const · T.
Почему объём растёт с ростом температуры? При повышении температуры молекулы начинают бить сильнее и приподнимают поршень. При этом концентрация молекул падает, удары становятся реже, так что в итоге давление сохраняет прежнее значение.
Дата добавления: 2020-04-12; просмотров: 891;











