Между двумя несмешивающимися жидкостями
| Бензол |
| Вода |
| I2 |
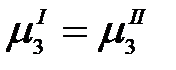 .
.
Выразим химический потенциал третьего компонента в обеих жидких фазах через его термодинамическую активность:
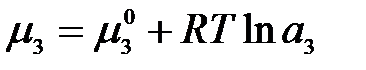 .
.
Подставим значение химического потенциала:
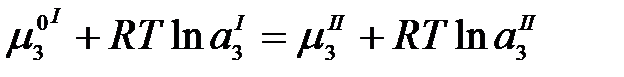 ,
,
где 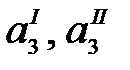 – термодинамические активности распределяющегося компонента (йода) в обеих фазах.
– термодинамические активности распределяющегося компонента (йода) в обеих фазах.
Преобразуем:
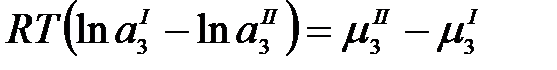 ;
;
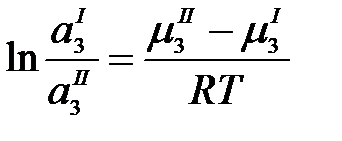 ;
;
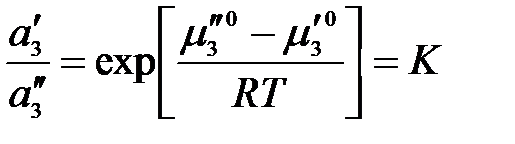 .
.
Так как стандартный химический потенциал зависит только от температуры, в правой части имеем величину, постоянную при Т = const, тогда
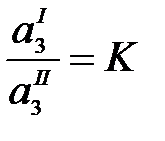
где К – коэффициент распределения вещества между несмешивающимися жидкостями.
Если количество добавленного третьего компонента мало по сравнению с массами фаз, то термодинамические активности можно заменить концентрациями:
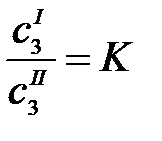 . (2.10)
. (2.10)
где 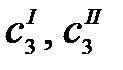 – равновесные концентрации распределяющегося вещества в соприкасающихся фазах.
– равновесные концентрации распределяющегося вещества в соприкасающихся фазах.
Уравнение (2.10) выражает известный закон распределения Нернста: отношение равновесных концентраций распределяющегося вещества в двух соприкасающихся, но не смешивающихся растворителях есть величина постоянная при Т = const.
Значения К для различных систем приведены в справочной литературе.
Если распределяющийся между фазами компонент в какой-либо из фаз подвержен диссоциации или ассоциации, то закон распределения принимает вид:
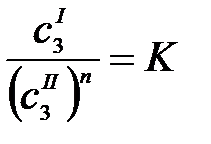 ,
,
где n = const – показатель ассоциации.
| lnc3I |
| lnc3II |
| lnK |
| α |
| n = tgα |
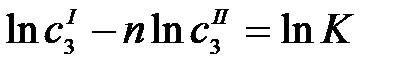 ;
;
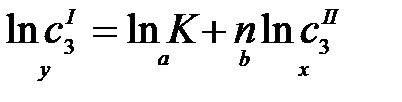 ;
;
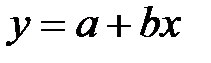 .
.
| Рис. 2.9. Графическое определение констант К и n уравнения Нернста |
Закон распределения Нернста является основой для расчета процесса разделения жидких смесей методами жидкостной экстракции.
Экстракция – процесс извлечения растворенного вещества (целевого компонента) из раствора с помощью другого растворителя (экстрагента), практически не смешивающегося с первым.
Основные цели экстракции:
1. получение чистого растворителя (очистка)
2. концентрирование целевого компонента в аналитических и технологических целях.
Движущая сила экстракции – разность химических потенциалов извлекаемого вещества в растворе и экстрагенте.
При выборе экстрагента сравнивают значения коэффициента распределения, который определяют экспериментально или берут из справочника. Чем больше К, тем эффективнее экстракция при условии, что в законе распределения фазой (I) является экстрагент.
Экспериментально установлено, что лучшее извлечение компонента достигается, если экстракция осуществляется в несколько приемов небольшими порциями экстрагента, чем один раз таким же общим количеством экстрагента. Таким образом, чем больше кратность экстракции, тем эффективнее извлечение целевого компонента.
Раздел III. химическое равновесие
Дата добавления: 2016-06-22; просмотров: 3067;











