Люминесценция вещества
Атомы вещества могут быть приведены в возбужденное состояние (в состояние с потенциальной энергией, превышающей равновесную энергию) без увеличения их средней кинетической энергии неупорядоченного движения, т.е. без нагревания вещества. Но находиться в возбужденном состоянии они могут в течение малого промежутка времени (»10-15 с) и всегда стремятся перейти в невозбужденное состояние. Процесс перехода атомов вещества из возбужденного в невозбужденное (равновесное) состояние чаще всего сопровождается каким-либо электромагнитным излучением.
Люминесценцией называют собственное свечение вещества. Люминесценция – это неравновесное излучение в данной области спектра, превосходящее тепловое излучение этого же вещества при данной температуре. Длительность люминесценции всегда больше периода световых колебаний, что является её отличительной особенностью по сравнению с другими вида излучений (свечении веществ) теплового излучения, отражения, рассеяния света и т.д.
Возбужденное состояние атомов вещества может быть достигнуто различными видами внешних воздействий: световым, рентгеновским, потоком электронов, электрического поля, ядерным излучением (g-квантов, нейтронов, протонов), химическими превращениями, механическими воздействиями. Поэтому различают следующие виды люминесценции: фотолюминесценцию, рентгенолюминесценцию, катодолюминесценцию, электролюминесценцию, радиолюминесценцию, хемилюминесценцию, триболюминесценцию.
По длительности свечения условно различают: флуоресценцию (t£10-8 с) и фосфоресценцию – свечение, продолжающиеся заметный промежуток времени после прекращения возбуждения.
Люминесцирующее вещество (люминофор) задерживает часть поглощаемой энергии в форме энергии возбужденного состояния атомов (молекул) вещества и, не преобразуя ее в тепло, испускает эту энергию в виде собственного излучения. При любом виде люминесценции справедливы два положения. Во-первых, возбудителем люминесценции может служить только тот физический агент, энергия которого в той или иной степени поглощается люминофором. Во-вторых, излучение люминесценции - собственное излучение, которое не зависит от способа его возбуждения. Спектр люминесценции вещества может быть расположен как в оптической, так и в рентгеновской области спектра электромагнитных излучений (включая и гамма-излучения атомных ядер).
При флюоресценции свечение возникает как результат перехода атомов с уровня возбужденного состояния на энергетический уровень основного состояния. Процесс лучеиспускания протекает в энергетически изолированных атомах и молекулах, и для него характерно относительно быстрое затухание послесвечения, подчиняющегося экспоненциальному закону мономолекулярных процессов:
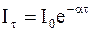 , (8.33)
, (8.33)
где Io – начальная интенсивность послесвечения;
a = 1/t – вероятность соответствующих энергетических переходов;
t – длительность возбужденного состояния молекул люминесцирующего вещества.
Фосфоресценция отличается от флюоресценции тем, что возбужденная молекула (атом) не сразу переходит в свое основное состояние, а некоторое время удерживается в метастабильном состоянии с энергией, несколько меньшей энергии возбужденного состояния.
Величину ea = WF - WM называют энергией активации. В возбужденном (метастабильном) состоянии атомы и молекулы находятся до тех пор, пока им не будет сообщена энергия активации, необходимая для высвечивания в результате беспорядочного движения молекул вещества или в результате поглощения ими энергии. В отличие от флюорофора атомы фосфорофора запасают энергию до некоторого предела, определяемого содержанием в нем активированных молекул (фосфорогенов). Насыщение может быть достигнуто как малой интенсивностью возбуждения в течение длительного промежутка времени, так и большой интенсивностью за короткое время. Высвечивание световой суммы, запасенной в метастабильных состояниях возбужденных молекул, например фосфора, при комнатной температуре и больших значениях энергии активации может происходить в течение нескольких месяцев, что связывают с медленными тепловыми колебаниями узлов кристаллической решетки. Этот процесс может быть ускорен под влиянием иных нетемпературных факторов, например электромагнитного поля, что характерно для так называемых лазеров.
Фосфоресценция в чистом виде представляет собой мономолекулярный процесс и, следовательно, затухание послесвечения также происходит по экспоненциальному закону, однако коэффициент затухания резко возрастает с повышением температуры.
Разновидностью люминесценции является рекомбинационное свечение люминофора. Оно возникает в том случае, когда в результате поглощения энергии активирующего процесса электроны молекул (атомов) или узлов кристаллической решетки оказываются переведенными в зону проводимости. Оно возникает при соединении электронов с возбужденными молекулами (атомами). Этот процесс является типично бимолекулярным, поэтому его интенсивность пропорциональна квадрату числа возбужденных центров nв единице объёма вещества, а послесвечение подчиняется закону:
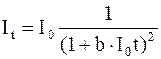 , (8.34)
, (8.34)
где Io – начальная интенсивность послесвечения;
b – характеристический множитель, зависящий от температуры.
При достаточно больших значениях начальной интенсивности высвечивания Io закон затухания рекомбинационного свечения может быть представлен в виде
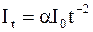 . (8.35)
. (8.35)
Такой закон послесвечения характерен для кристаллофоров, у которых поглощение энергии возбудителя происходит во всей решетке, а высвечивание – в локализованных центрах, т.е. место актов поглощения удалено от места актов высвечивания (наблюдается миграция, или блуждание энергии). При этом в процессе люминесценции участвуют не изолированные атомы или молекулы, а их множество и даже в отдельных случаях – вся решетка (Ленардовы фосфоры).
Все три вида люминесценции (флюоресценция, фосфоресценция и рекомбинационное свечение) могут протекать одновременно.
На процесс люминесценции могут также накладываться дополнительные явления, такие, как химические реакции в веществе люминофора (старение люминофора), гашение примесями или инфракрасным излучением и воздействие переменными электрическими полями (для усиления высвечивания).
Первое количественное исследование люминесценции было проведено в 1852 г. Дж. Стоксом, который сформулировал закон: длина волны люминесцентного излучения всегда больше длины волны света, возбудившего его.
С квантовой точки зрения, закон Стокса можно записать так:
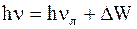 , (8.36)
, (8.36)
где n – частота падающего света;
nл – частота электромагнитного излучения люминофора;
DW – энергия, израсходованная на какие-то неоптические явления.
Вавилов С.И. в 1924 г. ввел в рассмотрение основную энергетическую характеристику люминесценции – энергетический выход.
Энергетический выход – это отношение энергии, излученной люминофором при полном высвечивании, к энергии, поглощенной им.
Вначале энергетический выход растет пропорционально длине волны, а затем, достигая максимума, спадает до нуля при дальнейшем увеличении длины волны (закон Вавилова).
Величина энергетического выхода для различных люминофоров колеблется в широких пределах. Максимальное его значение может достигать 80 %.
Механизм возникновения люминесценции, с точки зрения зонной теории, можно проследить на примере люминесцирующих кристаллофоров, искусственно приготовленных кристаллов с посторонними примесями. В кристаллофорах между валентной зоной и зоной проводимости располагаются примесные уровни активатора. При поглощении атомом активатора падающего фотона с энергией hn электрон с примесного уровня переходит в зону проводимости, свободно перемещается по кристаллу до тех пор, пока не рекомбинирует с ионом активатора, перейдя вновь на примесный энергетический уровень. Процесс рекомбинации сопровождается излучением кванта люминесцентного излучения. Время высвечивания люминофора определяется временем жизни возбужденного состояния атома – активатора, которое обычно мало. Поэтому свечение является кратковременным и исчезает почти вслед за прекращением облучения.
Для увеличения длительности свечения кристаллофор должен содержать центры захвата или ловушки для электронов, представляющие собой локальные незаполненные энергетические уровни, расположенные вблизи зоны проводимости. Центры захвата могут быть образованы различными факторами (и в частности, атомами примеси активатора). Под действием света атомы активатора возбуждаются, электроны с примесного уровня переходят в зону проводимости, становятся свободными. Захватываясь ловушками (центрами захвата), они теряют свою подвижность, а следовательно, и способность рекомбинировать с ионом активатора. Освобождение электрона из ловушки требует дополнительной энергии, которую они могут получить, например, за счет тепловых колебаний решетки. Получив дополнительную энергию, электрон может попасть в зону проводимости, будет двигаться по кристаллу до тех пор, пока не будет вновь захвачен ловушкой или не рекомбинирует с ионом активатора. Процесс рекомбинации сопровождается излучением кванта люминесцентного излучения. Длительность возможного процесса зависит от времени пребывания электрона в ловушке.
Явление люминесценции широко используется в различных областях науки и техники. Фотолюминесценция используется в оптических квантовых генераторах (лазерах) и при анализе состава неорганических и органических веществ. Что касается люминесцентного анализа, то относительно немногочисленные люминесценции жидких и твердых тел настолько характерны, что при анализе на чистоту вещества их можно с уверенностью отнести только к определенному веществу. Флуоресцентный анализ обладает рядом преимуществ: возможностью анализа относительно нестойких соединений, которые разрушаются при электрическом разряде или при нагревании; возможностью применения незначительных количеств анализируемого вещества, чем при других видах анализа (например, абсорбционном). Надо отметить, что при количественном флуоресцентном анализе интенсивность свечения не всегда прямопропорциональна концентрации активного вещества. Поэтому, как правило, вначале строят температурные градуировочные кривые, а затем по ним и по интенсивности свечения определяют концентрацию активного вещества.
Широкое применение имеет технический фотолюминесцентный анализ самых разнообразных материалов в микробиологии для обнаружения изменений вещества (окисление, старение), различных изъянов, пятен и фальсификации в документах и денежных знаках, распознавания различных маркировок, для обнаружения и исследования различных гидросвязей (в реках, озерах, кровотоках и в растениях).
Большое применение фотолюминесценция нашла в устройстве различных экранов, на которые наносятся различные флюоресцирующие под действием различных факторов (рентгеновского излучения, гамма – излучения, потоков электронов) составы.
Для электролюминесценции основной зависимостью является соотношение между интенсивностью свечения экрана и плотностью потока электронов заданной энергии, которые соответственно зависят от плотности электрического тока и ускоряющей разности потенциалов:
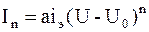 , (8.37)
, (8.37)
где U – ускоряющее напряжение;
Uo – пороговое значение ускоряющего напряжения для данного люминофора (равное 10¸100 В);
а – коэффициент, зависящий от выбора единиц измерения;
n – показатель, зависящий от энергии электронов (n = 1 ¸ 3).
Энергетический выход электролюминесценции экранов не превышает 10 %.
В зависимости от назначения кристаллофосфоры представляют собой сульфиды цинка (ZnS, ZnSAg, ZnSCu) и кадмия (ZnCdSAg), применяемые для люминесцентных красок, рентгеновских, осциллографических и телевизионных экранов визуального наблюдения (4600¸5200 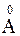 ); вольфраматы кальция (шеслит CaWO4) и кадмия (CdWO4) – для усиливающих экранов (4200¸4800
); вольфраматы кальция (шеслит CaWO4) и кадмия (CdWO4) – для усиливающих экранов (4200¸4800 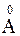 ); силикаты цинка (ZnSiO4Mn) и кадмия (CdSiO4Mn), активизированные марганцем, – для люминесцентных ламп (5300¸6000
); силикаты цинка (ZnSiO4Mn) и кадмия (CdSiO4Mn), активизированные марганцем, – для люминесцентных ламп (5300¸6000 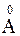 ); рубины (Al2O3Cr), обладающие большим запасом световой суммы,– для сцинтиллирующих кристаллофосфоров; урановые стекла – для индикаторов ультрафиолетового излучения и оболочек газоразрядных трубок. Кроме того, применяются органические фосфоры (сцинтилляторы), борные фосфоры (обеспечивающие длительное послесвечение), молекулярные двойные соли MePt(CN)474H2O, например платиносинеродистый барий, и минералы.
); рубины (Al2O3Cr), обладающие большим запасом световой суммы,– для сцинтиллирующих кристаллофосфоров; урановые стекла – для индикаторов ультрафиолетового излучения и оболочек газоразрядных трубок. Кроме того, применяются органические фосфоры (сцинтилляторы), борные фосфоры (обеспечивающие длительное послесвечение), молекулярные двойные соли MePt(CN)474H2O, например платиносинеродистый барий, и минералы.
Дата добавления: 2016-06-22; просмотров: 2793;











