Нарушения конечных этапов обмена белка
Конечные этапы белкового обмена — это вся совокупность превращений, приводящих к формированию экскретируемых из организма терминальных азотсодержащих продуктов — аммиака, мочевины, мочевой кислоты, креатинина, индикана, а также и сам процесс их экскреции.
Равновесным показателем выведения и образования всех этих продуктов служит уровень остаточного (небелкового) азота сыворотки крови. По И. Тодорову, эта величина находится в пределах 15-40 мг/дл. Остаточный азот по фракциям распределяется в норме, как показано в табл. 6.

Таблица 6. Остаточный азот сыворотки крови и его составляющие
Таким образом, главная составная часть остаточного азота — мочевина. Собственно аммиак представлен в крови в связанном состоянии. Его молярная концентрация ничтожна и у здорового индивида составляет менее 517 мкмоль/л. В тканях равновесные концентрации аммиака также крайне малы, но скорости его образования и превращения велики, что делает аммиак важнейшим метаболитом белка.
Большие количества аммиака формируются при окислительном и неокислительном дезаминировании (рис. 17). Аммиак — высокотоксичный продукт азотистого метаболизма, к тому же он легко проникает через липидные мембраны. Больше всего аммиака формируют органы с наиболее интенсивным обменом аминокислот и биогенных аминов — лидером является мозг, затем идут печень и ЖКТ (где этот процесс сильно зависит от деятельности микрофлоры и степени нарушения переваривания белков, а также регулярности опорожнения кишечника).
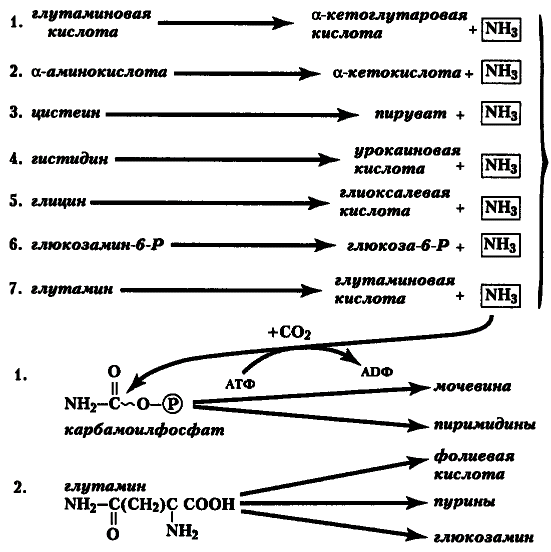
Рис. 17. Пути образования аммиака
Почки — также активные продуценты аммиака, поскольку такой способ регуляции кислотно-щелочного равновесия, как аммониогенез, предусматривает экскрецию иона аммония в мочу в обмен на натрий, с целью компенсации ацидоза, особенно хронического (см. ниже). До 6 % от мочевого азота составляет именно продукт аммониогенеза — ион аммония.
На месте своего образования, в тканях и органах, аммиак подлежит немедленной нейтрализации. Это достигается путём аминирования α-кетокислот, прежде всего α -кетоглутаровой, с образованием глутаминовой кислоты (рис. 18, с. 108, вверху) и, в особенности, путем превращения глутаминсинтетазой глутаминовой кислоты в ее амид — глутамин. Он-то и служит, в основном, эквивалентом непротонированного NH3 при синтетических процессах и временным хранилищем (транспортёром) нетоксичной формы аммиака.
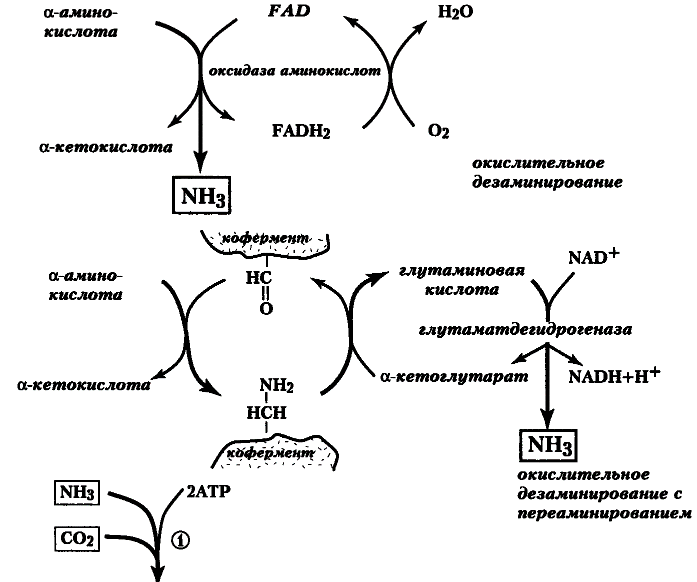
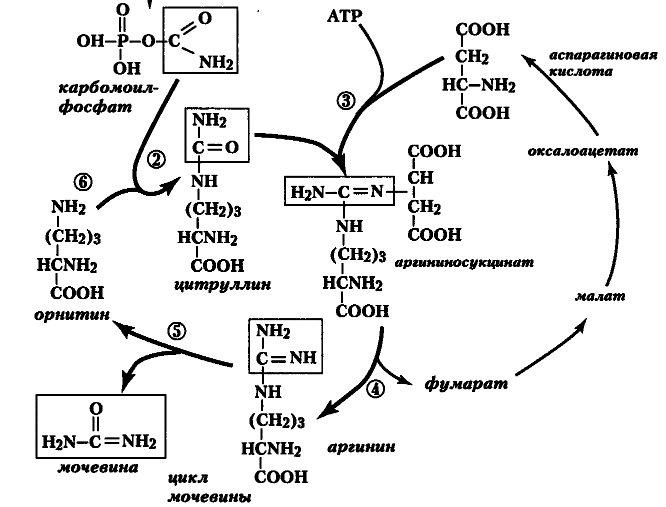
Рис. 18. Первичная нейтрализация аммиака (вверху) и цикл мочевины (внизу). Наследственные дефекты образования мочевины обозначены цифрами 1-6, расшифровку см. в таблице 7
Глутамин образуется в самой печени и испытывает постоянный кругооборот между нею и другими органами. Избыток аммиака из мозга достигает печени в этой же транспортной форме. Почки получают глутамин для процесса аммониогенеза также из печени. Глутаминзависимая аспарагинсинтетаза может переводить аммиак в состав аспарагина и освобождать глутамат. Карба-моилфосфат-синтетазы I и II (рис. 17), из которых первая уникальна для печени, а вторая имеется и в других тканях с напряжённым аминокислотным обменом, превращают, соответственно, глутаминовую кислоту и глутамин в карбамоилфосфат — активную форму, переносящую аммиак в системы, синтезирующие аргинин или пиримидины.
Через синтез и превращения аргинина лежит путь аммиачного азота к мочевине (карбамиду) — конечному выводимому продукту его метаболизма у млекопитающих (рис. 18 внизу). Печень синтезирует подавляющую часть мочевины, что было обнаружено в результате опытов отечественных учёных М.В. Ненцкого, С.С. Салазкина и И. Залесского в лаборатории И.П. Павлова. Справедливости ради, надо отметить, что незначительное количество мочевины способен образовывать сам головной мозг.
Процесс образования карбамида представляет цикл реакций (орнитиновый, он же цитруллиновый цикл, в зарубежной литературе — цикл Кребса-Гензелейта, или цикл мочевины). Многие этапы этих реакций требуют гидролиза макроэргических фосфатных связей. Считается, что весь процесс объединения аммиака с С02 в мочевину обходится печени в значительное количество энергии — 4 макроэргических связи на моль карбамида (рис. 17-18).
Эти расходы оправдываются тем, что в результате ядовитейший аммиак становится частью практически малотоксичной мочевины, которая водорастворима и ведет себя, как беспороговое вещество — то есть выводится почкой пропорционально её образованию, а не после преодоления какого-то минимального уровня её плазменного содержания.
Если бы этот процесс не происходил, все большее количество кетокислот (прежде всего, α-кетоглутаровой и щавелевоуксусной) связывалось бы с аммиаком и расходовалось на его временную нейтрализацию, без регенерации обратно в кетоформу. Рано или поздно это привело бы к торможению цикла Кребса и развитию тканевой гипоксии, прежде всего, в органах, производящих больше всего аммиака — в частности, в ЦНС.
Именно это и наблюдается при срыве мочевинообразования в печени и проявляется нарастающей тканевой гипоксией мозга, дающей прекому и кому.
С другой стороны, большое значение имеет постоянное выведение мочевины почками. Опять-таки, ради точности отметим, что около 1 % экскреции мочевины в норме идёт через потовые железы, а при обильном потении этот процент может стать больше. Примерно 25 % суточной продукции мочевины диффундирует в кишечник, где разлагается бактериями с образованием аммиака и снова утилизируется.
При почечной недостаточности растет экстраренальное выделение мочевины через кожу и слизистые кишечника и желудка. У здорового взрослого на обычной диете каждый день почками выделяется 25-35 г этого метаболита. Подчеркнем еще раз принципиальное положение о малой токсичности карбамида. Воспринимаемая обыденным сознанием как яд (шлак), мочевина нужна организму, который толерантен к достаточно большим её концентрациям.
Уремия, как терминальная стадия хронической почечной недостаточности, когда конечные продукты азотистого обмена не выводятся из организма, также, по современным данным, не является чисто мочевинным отравлением, а представляет результат совокупного действия на организм более чем 200 других накапливаемых продуктов, которые куда более вредоносны, даже в малых, по сравнению с карбамидом, концентрациях.
Мочевина используется почкой для осмотического диуреза, а лейкоцитами как бактерицидный агент. Не случайно, она реабсорбируется здоровыми почками (при условии высокой скорости мочетока и, особенно, при бедной белком диете) примерно на 1/3 от всей ее фильтрации и имеет клиренс порядка 75 мл/мин, в отличие, например, от нереабсорбируемого инулина (90-130 мл/мин).
Любопытно отметить, что мочевина даже может служить источником пищевого азота (в ветеринарии). П.Е. Калмыков и М.Н. Логаткин отмечают, что мочевина при пероральном введении и действии уреазы кишечных бактерий (а по некоторым данным — и эндогенная мочевина) могут использоваться организмом в особых условиях, как источник азота для заменимых аминокислот (1974). Хвалебную песнь мочевине мы можем закончить упоминанием о ней, как компоненте высокоэффективной зубной пасты и жевательной резинки, о чём с энтузиазмом сообщает реклама.
И всё же, избыточное накопление карбамида не остаётся для организма без последствий, как в силу его осмотического эффекта, так и в связи с тем, что при уремии будет снижаться активность аммиак-нейтрализующих реакций, приводящих к его синтезу: ведь продукт из сферы действия реакции не выводится.
В конечном итоге, и нарушение выведения продуктов азотистого метаболизма, так же как нарушение нейтрализации аммиака в мочевину, приводит к дефициту метаболитов цикла Кребса, тканевой гипоксии и коме.
Дата добавления: 2022-12-02; просмотров: 2528;











