Пути обмена пуринов
Нуклеиновые кислоты организма наполовину состоят из пуриновых нуклеотидов, каждый из которых, помимо пентозы и фосфорной кислоты, содержит пуриновое азотистое основание. Пуриновые основания — производные пурина.
Пурин — ароматическое гетероциклическое соединение, образуемое из двух колец — имидазола и пиримидина. Последний также представляет собой ароматический гетероцикл в виде шестичленного азот-углеродного кольца с тремя двойными связями. Имидазол, в свою очередь, пятичленное азот-углеродное кольцо (рис. 21).
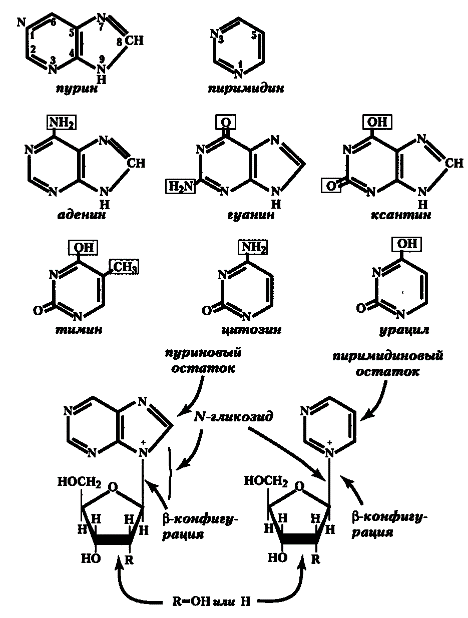
Рис. 21. Структура нуклеотидов
В составе нуклеотидов встречается два главных пуриновых основания — аденин (А) и гуанин (Г). Изредка в нуклеиновых кислотах обнаруживаются минорные метилированные пурины — 2-метиладенин и 1-метилгуанин. По некоторым данным, усиленное метилирование генов препятствует их активной экспрессии.
N-гликозиды пуриновых оснований, лишенные фосфорной кислоты, называются нуклеозидами (аденозин, гуанозин). Таким образом, нуклеотиды — их фосфорнокислые эфиры. Дифосфатные эфиры аденозина и гуанозина известны как нуклеозид- пирофосфаты (АДФ и ГДФ). Наконец, трифосфат аденозина — это знакомая каждому студенту-медику со школьной скамьи адено- зинтрифосфорная кислота (АТФ).
Трифосфатом гуанозина является гуанозинтрифосфорная кислота (ГТФ). Таким образом, роль пуринов не исчерпывается их пластическими функциями в составе РНК и ДНК. Главные участники энергетических процессов в клетке, связующее звено между реакциями, протекающими с выделением и с потреблением энергии — это именно три- фосфорибонуклеозиды (см. выше).
Механизм биосинтеза пуриновых нуклеотидов таков, что азотные атомы для их колец происходят из амидных групп глутамина (N-3, N-9) и аспарагина (N-1), а также из глицина (N-9). Углеродные компоненты колец берутся из глицина (С-4, С-5), из формиата (С-2, С-8), а также из углекислого газа (С-6). Вначале образуется на основе фосфорибозил-пирофосфата ациклическая форма нуклеотида с открытой цепью.
Только затем кольцо замыкается в пуриновый цикл. Скорость биосинтеза пуринов регулируется по типу обратной связи количеством конечных продуктов. Кроме того, избыток АТФ способствует синтезу гуаниловой, а избыток ГТФ — адениловой кислоты. Накопление ГМФ подавляет продукцию АМФ (рис. 22).
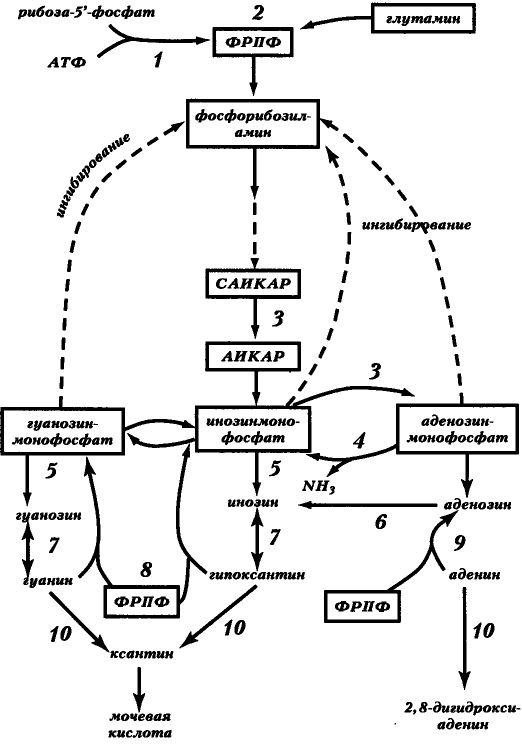
Рис. 22. Пути пуринового обмена. Сокращения: ФРПФ — фосфорибозилпирофосфат; САИКАР — сукцинил-аминоимидазолкарбоксиамид-риботид; АИКАР — аминоимидазолкарбоксиамид-ри ботид; ФЕРМЕНТЫ: 1 — ФРПФ-синтетаза; 2 — амидофосфорибозилтрансфераза; 3 — аденилосукцинат-лиаза; 4—АМФ-дезаминаза; 5 - нуклеотидаза; 6 — аденозиндезаминаза, 7 — пуриннуклеозидфосфорилаза; 8 — гипоксантин-фосфорибозилтрансфераза (ГФРТ); 9 — аденин-фосфорибозилтрансфераза; 10 – ксантиноксидаза
При распаде ДНК и РНК образуются мононуклеотиды, которые могут реутилизироваться для их нового синтеза. Дальнейший ферментативный гидролиз мононуклеотидов даёт свободные азотистые основания. Затем они распадаются в соответствии с общей последовательностью, показанной на рис. 23. Разные животные доводят распад пуринов до различных конечных стадий.
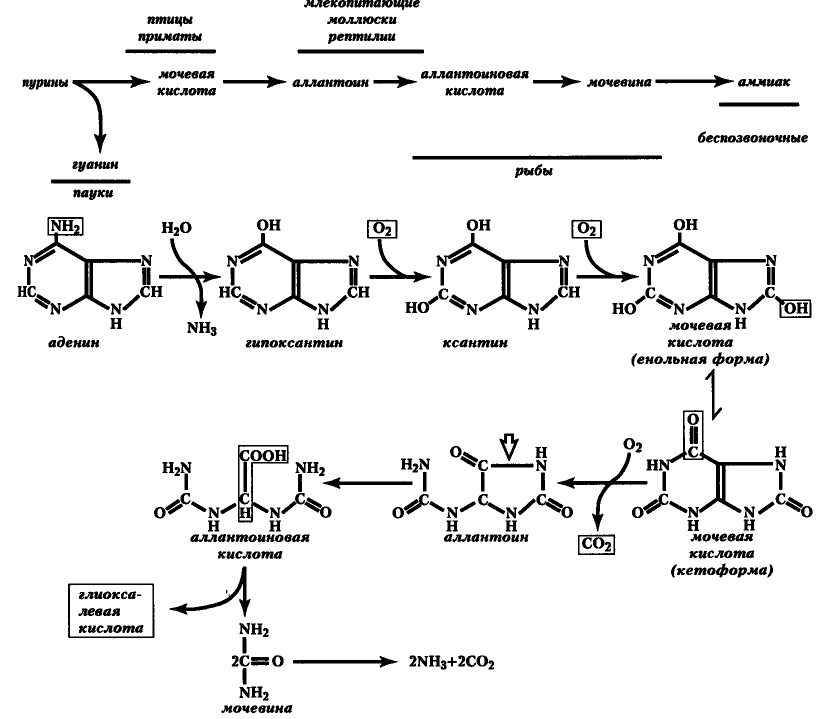
Рис. 23. Пути деградации пуринов и конечные продукты их обмена у животных
У беспозвоночных — это аммиак, у пластинчатожаберных моллюсков и рыб — мочевина и, реже, аллантоиновая кислота, у бронхоногих моллюсков, черепах и млекопитающих — аллантоин, наконец, у человека, приматов, птиц, ящериц и змей, а также у... героя знаменитого мультфильма — дога-далматинца — конечным продуктом пуринового обмена служит мочевая кислота. Интересно, что такие разные живые существа, как пауки и свиньи, имея недостаточно гуаниндезаминазы, экскретируют пурины в виде гуанина.
С банально-энергетической, утилитарной точки зрения непонятно, почему эволюционно более сложные животные все более и более недоокисляют пурины, теряя их во все более сложной форме?
Вероятно, за этим кроются какие-то этапные эволюционные изменения в метаболизме этих живых существ, и, по крайней мере, мочевая кислота нужна им для каких-то неэнергетических целей.
Человек выводит около 1,5 г мочевой кислоты в день, причем не менее 60 % происходит из эндогенных пуринов, остальное — из пуринов пищи. У 95 % мужского населения концентрация мочевой кислоты в плазме лежит между 2,2 и 7,5 мг/дл, у женщин до менопаузы эстрогены обеспечивают более эффективную экскрецию уратов, поэтому статистическая норма содержания мочевой кислоты у них ниже и находится между 2,1 и 6,6 мг/дл. У детей обоего пола уровень мочевой кислоты существенно ниже (около 3-4 мг/дл), кроме первой недели жизни, когда он подвержен действию транзиторной физиологической гиперурикемии новорожденных (см. т.1, с. 108). У подростков среднее содержание уратов растет (до 5,1 мг/дл у юношей и 4,1 — у девушек).
Нормальная судьба мочевой кислоты в организме характеризуется следующими данными. Хотя пурины синтезируются и деградируют в каждой клетке, мочевая кислота может быть образована только под действием фермента ксантиноксидазы. У человека этот энзим имеется лишь в печени и энтероцитах, где и идет переработка ксантина в мочевую кислоту.
Мочевая кислота — слабокислый продукт, поэтому она, секретируясь в кровь, образует соли-ураты — со щелочными катионами (на 98 % — с натрием), которые связываются α1α2 -глобулинами плазмы только на 5% и выводятся на 2/3 почками, а на 1/3 — через тонкий кишечник. В кишечнике бактерии разрушают кислоту, последовательно, с помощью ферментов уриказы, аллантоиназы,аллантоиказы и, наконец, уреазы — до аммиака и глиоксалевой кислоты.
При гиперурикемии и нарушениях почечной экскреции уратов этот путь выведения конечных продуктов пуринового и азотистого метаболизма усиливается. Считается, что усиленное кишечное выведение и бактериальное превращение мочевой кислоты и мочевины имеет отношение к возникновению язвенных поражений ЖКТ при уремии.
Плазма крови при 37 °С насыщается уратом натрия уже при концентрации 6,8 мг/дл, то есть верхняя граница нормального содержания уратов в плазме у мужчин находится, примерно, на уровне насыщения. Однако, ураты в крови не кристаллизуются даже при превышении этого порога в 8-10 раз, оставаясь в состоянии супернасыщенного раствора, благодаря действию каких-то неидентифицированных солюбилизаторов.
Подобные растворы, при действии каких-то факторов, меняющих их свойства, могут легко давать кристаллизацию. Вместе с тем, в тканях и моче ураты кристаллизуются и при меньших концентрациях. Г. Шаде считал, что большое значение имеет изомерная форма урата натрия, так как его лактимы растворяются труднее лактамов. По всеобщему признанию, наибольшее сродство к уратам испытывают хрящевая ткань и интерстиций почек.
В экскреции уратов почками участвуют все три основные парциальные функции. После фильтрации 98 % уратов реабсор- бируется, половина этого количества повторно секретируется в первичную мочу и 40-44 % секретированных уратов реабсорбируется вновь. Таким образом, 8-12% первоначально отфильтрованного количества уратов выводится с дефинитивной мочой. В моче кристаллизации уратов способствует кислый pH.
При рН=5 в моче можно растворить от 6 до 15 мг/дл уратов без кристаллизации, подщелачивание мочи с кристаллами уратов вызывает их исчезновение, что используется как экспресс-тест, но уже при рН=7 насыщение мочи требует более чем 158 мг/дл уратов. Именно поэтому все виды ацидоза, в том числе — кетоацидоз и лактатацидоз (например, наступающий при алкоголизации, осложняющий сахарный диабет, а также сопровождающий физическое утомление), способствуют обострениям подагры.
Ураты легче выпадают в осадок при температурах ниже 37 °С. При 32 °С (температура коленного сустава) растворимость уратов уменьшается на треть, при 29 °С (температура голеностопа) — наполовину. Наиболее «холодным» суставом организма является первый предплюснофаланговый сустав стопы. Не случайно, именно он поражается у 80 % больных подагрой, обострениям которой способствует, в частности, и переохлаждение. Описаны также подагрические шишки в хрящах других подверженных переохлаждению органов — ушных раковин.
Дата добавления: 2022-12-02; просмотров: 2719;











