Стеклообразное и кристаллическое состояние
Вещества
Вещества в твёрдом состоянии могут иметь кристаллическое или аморфное строение. Для кристаллических тел характерны следующие особенности:
1. Строгий порядок расположения частиц (атомов и молекул) в пространстве.
2. Как следствие, кристаллические тела имеют чёткие геометрические формы, определённую температуру плавления, анизотропию свойств (физические свойства различны в разных направлениях).
3. Кристаллическое состояние стабильно при обычных условиях, имеет наиболее низкую внутреннюю энергию.
Стеклообразное состояние – это аморфная разновидность твердого состояния. Атомы в стекле расположены беспорядочно. Стеклообразное состояние метастабильно, так как внутренняя энергия такого состояния выше, чем кристаллической упорядоченной структуры (рис 1.1).
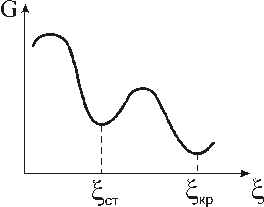
Рис. 1.1. Влияние степени упорядоченности системы на энергию Гиббса
Мерой устойчивости термодинамической системы является энергия Гиббса G = H – TS. Если при переходе в новое состояние изменение энергии Гиббса системы DG < 0, процесс протекает самопроизвольно.
x – обобщённый структурный фактор, характеризующий упорядоченность расположения структурных элементов системы.
Термодинамически переход стеклообразного состояния в кристаллическое оправдан, так как такое структурное превращение сопровождается снижением энергии Гиббса: DG = Gкр – Gст < 0. Однако из-за большой вязкости твёрдого стекла самопроизвольная кристаллизация при невысоких температурах практически невозможна. Для перестройки структуры вещества необходимо поступательное движение атомов или молекул. При обычных температурах частицы в твердых телах совершают преимущественно колебательные движения около центров равновесия. При умеренных температурах один перескок атома в соседнее устойчивое положение приходится примерно на 106 колебаний. Поэтому в обычных условиях стеклообразная структура устойчива. Стабилизация стеклообразного состояния в готовых изделиях является важной задачей во всех стекольных технологиях. Уникальные свойства размягчённого стекла (стекломассы) позволяют получать такие изделия, которые невозможно изготовить из кристаллических материалов.
Стеклом называются все аморфные тела, получаемые путем переохлаждения расплава независимо от состава и температурной области затвердевания и обладающие, в результате постепенного увеличения вязкости, механическими свойствами твердых тел. Процесс перехода из стеклообразного состояния в жидкое должен быть обратимым.
В стеклообразном состоянии могут находиться вещества, относящиеся к разным классам химических соединений. Многовековая история стеклоделия связана в основном с получением силикатных стекол системы SiO2-Na2O-CaO. В последние годы показано, что натрий-кальций-силикатные стёкла составляют лишь небольшую часть безграничного мира неорганических стёкол. Широко используются и другие оксидные стёкла, а также бескислородные и металлические стёкла.
По мнению Аппена, типичные стеклообразные тела:
1) изотропны, т.е. их свойства одинаковы во всех направлениях;
2) при нагревании не плавятся, как кристаллы, а постепенно размягчаются, переходя из хрупкого состояния в тягучее, высоковязкое и, наконец, в капельно-жидкое состояние, причём не только вязкость, но и все другие свойства меняются непрерывно;
3) переходят в жидкое состояние и отвердевают обратимо (если не происходит кристаллизация или ликвация).
Американское общество по испытаниям и материалам (ASTM) предлагает следующее определение стекла: стекло – неорганический продукт плавления, охлаждённый до твёрдого состояния без кристаллизации.
Дата добавления: 2018-11-26; просмотров: 877;











