Диффузия в стёклах и стеклообразующих расплавах
Диффузия – это процесс самопроизвольного выравнивания концентрации компонентов за счёт перемещения отдельных ионов и атомов под действием градиента химического потенциала grad μi.
grad μi – движущая сила диффузии.
Диффузионный поток в общем случае рассчитывается по уравнению:
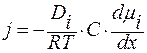 .
.
Для простых случаев это уравнение преобразуется с учётом градиента концентраций диффундирующих компонентов:
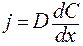 .
.
Возможность перемещения частиц через диффузионные процессы проявляется в связи с их тепловым движением. Колебания атомов или ионов около положений равновесия дают возможность перескока в соседнее положение равновесия, если оно оказывается вакантным. Диффузионный поток реализует стремление системы к минимальной энергии Гиббса.
В том случае, если диффузия частицы протекает в структуре, представленной подобными же частицами, говорят о самодиффузии (например, диффузия катиона натрия в стекле Na2O-SiO2). Если природа частиц различна, то выравнивание концентраций протекает за счёт гетеродиффузии (диффузия катиона калия в стекле Na2O-SiO2).
Особенности диффузии в силикатных стёклах:
1. Кремний и кислород прочно связаны в кремнекислородном каркасе. Поэтому диффузия катионов-стеклообразователей протекает значительно медленнее, чем катионов–модификаторов:
DSi4+<<DNa+
2. Так как анионов кислорода в стекле много и они являются общими для всех катионов, то достаточно незначительного перемещения кислорода чтобы компенсировать изменение заряда при диффузии катионов.
DМеО ≈ DМе2+ , так как ионов О2- много.
3. Механизм диффузии в стёклах во многом аналогичен диффузионному перемещению в кристаллах, так как в обоих случаях перемещаются, в основном, катионы небольших размеров.
Известно, что в кристаллах частицы диффундируют, как правило, по двум вариантам: по вакансиям решетки и по междуузлиям. В стёклах реализуются оба варианта, но обычно ионы–модификаторы диффундируют по межтетраэдрическим полостям, т.к. энергия активации диффузии в этом случае наименьшая.
Энергия активации диффузии для стёкол и кристаллов отличаются незначительно. Так для системы Na2O∙2CaO∙3SiO2 энергия активации диффузии катионов натрия составляет для стеклообразного состояния Едиф= 125 кДж/моль, для кристаллического состояния – Едиф = 125 кДж/моль. Коэффициенты диффузии при температуре 800оС соответственно равны: Dст = 5,3∙10-9 см2/с и Dкр = 6,8 ∙10-10 см2/с.
Так как диффузия протекает по междуузлиям, то энергия активации диффузии в гораздо меньшей степени зависит от природы диффундирующего катиона, чем от структуры стекла.
Температурная зависимость коэффициента диффузии в кристаллах описывается уравнениями:
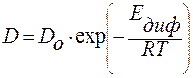 ;
;
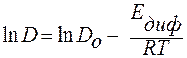 .
.
Для стёкол необходимо учитывать две особенности:
1. Вблизи температуры стеклования меняется структура стекла, поэтому уравнение можно использовать за пределами области размягчения.
|
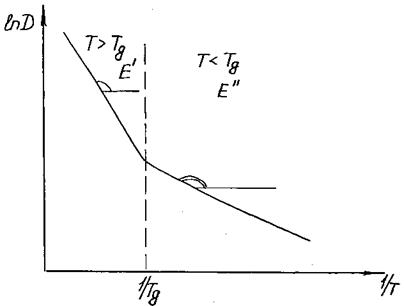
2. При замораживании структуры расплава в стекле образуются межтетраэдрические полости, по которым могут диффундировать катионы-модификаторы. Поэтому энергия активации диффузии при низких температурах будет меньше, чем в расплаве. В расплаве ионы упакованы более плотно, чем в твердом стекле. При высоких температурах Т > Tg структура стеклорасплава ближе к равновесной (рис. 4.3).
Рис. 4.3. Температурная зависимость коэффициентов диффузии компонентов в стекле
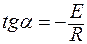 ; E΄ > E΄΄.
; E΄ > E΄΄.
Если предположить, что диффундирующий ион – это сферическая частица, то коэффициент диффузии можно рассчитать по уравнению Стокса–Эйнштейна:
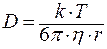 ,
,
где k – постоянная Больцмана;
η – вязкость расплава;
r – радиус диффундирующей частицы.
Коэффициент диффузии связан с электропроводностью уравнением Нернста-Эйнштейна:
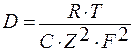 .κ,
.κ,
C – концентрация ионов;
Z – заряд иона;
F – число Фарадея;
Κ – электропроводность.
Экспериментальные методы определения коэффициента диффузии в стёклах такие же, как для кристаллов и высокотемпературных расплавов. В частности, используются метод анализа изменения концентрации диффундирующих изотопов, метод вращающегося диска и другие.
Дата добавления: 2018-11-26; просмотров: 2211;











