Лекция № 22. Элементы IVA-подгруппы
Главную подгруппу IV группы (IVА-подгруппу) составляют: углерод - C, кремний - Si, германий - Ge, олово - Sn и свинец - Pb. Общая электронная формула ns2np2 обуславливает проявление степеней окисления -4 и +4. Кроме этого с увеличением порядкового номера увеличивается устойчивость соединений в степени окисления +2; для свинца эта степень окисления наиболее характерна. В ряду C, Si, Ge, Sn, Pb с увеличением эффективного радиуса атома наблюдается усиление металлических свойств: углерод и кремний - неметаллы, германий - полупроводник, олово и свинец - металлы, соединения которых проявляют амфотерные свойства (для соединений свинца слабоамфотерные).
Отличительная особенность углерода заключается в равенстве числа валентных электронов и валентных орбиталей, что позволяет атомам данного элемента образовывать устойчивые гомоцепи неограниченной длины и циклы. Именно это обстоятельство обуславливает разнообразие органических соединений. Появление у кремния вакантных d-орбиталей делает связь кремний - кремний уязвимой к атаке разнообразными реагентами, поэтому кремниевые аналоги органических соединений неустойчивы и пирофорны (способны к самовоспламенению на воздухе).
Для углерода наиболее характерна ковалентность и координационное число (КЧ) 4, в то время как кремний, германий и олово часто проявляют координационное число 6. Свинец в своих соединениях может проявлять и более высокие КЧ, вплоть до 8.
22.1. Углерод и его соединения
Элемент углерод имеет кларк 0,15 мол.% и представлен в природе двумя стабильными изотопами: 12С (99%) и 13С. Также существует радиоактивный изотоп 14С с периодом полураспада 5570 лет, образование которого происходит при бомбардировке атомов азота нейтронами в верхних слоях атмосферы:
14N + n = 14C + 1H
Вовлечение радиоуглерода в биологический круговорот приводит к тому, что живые организмы имеют постоянную концентрацию данного изотопа. После прекращения жизнедеятельности организма концентрация радиоуглерода постепенно уменьшается за счет распада его ядер. На определении остаточного количества 14C основан один из наиболее точных методов датировки органических остатков в археологии.
Углерод образует группу карбонатных минералов: CaCO3 - кальцит, мел, мрамор, мергель; MgCO3 - магнезит; CaCO3×MgCO3 - доломит; FeCO3 - сидерит; Cu2(OH)2CO3 - малахит. Углерод входит в состав органических соединений, составляющих основу и обеспечивающих жизнедеятельность живых организмов.
В природе встречаются с разной вероятностью все аллотропные модификации углерода, основными из которых являются алмаз, графит и карбин. Алмаз - прозрачные кристаллы, самое твердое из всех природных веществ, плохо проводит тепло, не проводит электрический ток. Свойства алмаза обусловлены строением его кристаллической решетки. Атомы углерода в кристалле алмаза находятся в состоянии sp3-гибридизации и связаны друг с другом прочными ковалентными s-связями, каждый атом окружен четырьмя другими атомами, образующими тетраэдр.
Графит - темно-серое вещество с металлическим блеском, хорошо проводит электрический ток, тугоплавкий, имеет слоистую структуру. Атомы в кристалле графита находятся в состоянии sp2-гибридизации и объединены в плоские слои, состоящие из правильных шестиугольников, в которых каждый атом связан s-связями с соседними атомами. Сопряжение негибридизованных pz-орбиталей атомов углерода, расположенных перпендикулярно плоскости слоев и содержащих неспаренные электроны, приводит к образованию делокализованной p-системы, обеспечивающей высокую электропроводность графита. Расстояние между слоями довольно велико (0,335 нм) и силы взаимодействия слабы, поэтому графит легко расслаивается. При температуре 3000 °С и давлении 7000 - 10000 мПа графит переходит в алмаз.
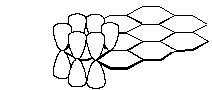 ¾¾®
¾¾® 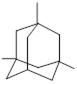
Карбин - мелкокристаллический порошок черного цвета, по твердости занимает промежуточное положение между графитом и алмазом, обладает полупроводниковыми свойствами. При нагревании до 2800 °С без доступа воздуха карбин превращается в графит. Кристаллы карбина состоят из линейных цепочек углеродных атомов, соединенных чередующимися одинарными и тройными связями (полиин) или кумулированными двойными связями (поликумулен).
-CºC-CºC- =C=C=C=
полиин поликумулен
При испарении углерода в пламени электрической дуги образуется группа молекулярных соединений углерода - фуллерены. Наиболее полно изучен букибол - С60, образующий молекулу в форме футбольного мяча (сшитые пяти- и шестичленные циклы).
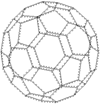
В качестве аллотропной модификации иногда рассматривают стеклоуглерод - аморфное вещество, содержащее фрагменты разных модификаций.
Технические алмазы применяются для изготовления наконечников буров, стеклорезов, для приготовления специальных шлифовальных порошков. Хорошо отшлифованные прозрачные природные алмазы - бриллианты - используют как украшения. Графит используется для изготовления электродов, тиглей для переплавки металлов. Из графита делают термостойкие смазки, стержни карандашей. Сажа, состоящая в основном из мелкодисперсного графита, применяется в качестве наполнителя при вулканизации каучука, для приготовления красок. Каменный и древесный уголь, кокс применяют как восстановители в металлургии. Кроме того, древесный уголь используют как адсорбент (поглотитель) вредных веществ из газов и растворов. Адсорбционную способность угля можно улучшить обработкой перегретым паром, который освобождает поры, увеличивая общую поверхность. Такой уголь называется активированным, он применяется в виде таблеток при отравлениях и желудочных заболеваниях , для очистки спирта от сивушных масел, сахарного сиропа от окрашенных веществ, для очистки воздуха от отравляющих веществ.
Химические свойства. При низких температурах углерод во всех аллотропных модификациях довольно инертен. При нагревании активность углерода увеличивается и он реагирует с водородом, кислородом, серой, кремнием:
t t t
C + 2H2 = CH4 ; C + 2S = CS2; C + Si = SiC
Ni
Взаимодействуя с металлами, углерод образует карбиды:
t t t
Ca + 2C = CaC2; 4Al + 3C = Al4C3; 3Fe + C = Fe3C
При высоких температурах углерод является сильным восстановителем, окисляется водой и другими оксидами, а также кислотами-окислителями:
t t
C + H2O = CO + H2; C + CuO = Cu + CO;
t
C + 4HNO3 = CO2 + 4NO2 + 2H2O
Дата добавления: 2017-10-04; просмотров: 1848;











