Влияние кислотности на степень инактивации при обработке давлением
Давно установлено, что концентрация водородных ионов играет роль фактора, который определяет границы существования живой материи [23]. Большинство экспериментальных работ отмечают, что кислотность пищевой среды существенно влияет на степень инактивации микроорганизмов высоким давлением. В работе [139] приведены результаты исследования баротолерантности Saccharomyces cerevisiae, Escherichia coli и Staphylococcus epidermidis в различных окружениях (агар, бульон, яблочный джем и сок). Показано, что рН окружения играет важную роль в разрушении микробов: S. Epidermidis подавлялась более чем на 90% при 300 МПа за 11,2 мин при рН = 7,2 и по 4,8 мин при рН = 4,0.
Исследования, которые проводились на B. Subtilis, показали, что сопротивление бактерий давления снижалось, когда снижался рН молока, и выживаемость В.subtilis при этом рН может изменяться с давлением и температурой обработки. В работе [58] показано, что кислотное значение рН окружения может быть причиной инактивации поврежденных давлением клеток. Влияние на культуру Escherichia coli 0157Н:7 давления 400 МПа в течение 10 минут и дальнейшей ее выдержки в окружении с рН между 7,0 и 3,5 показало, что наиболее примечательный рост инактивации наблюдается при рН = 4,5 и ниже [158].
В работе [115] величины рН внутри клетки были измерены непосредственно в процессе обработки клеток давлением. Были определены внутренние рН Lactococcus lactis и Lactobacillus plantarum в течение и после обработки давлением 200 и 300 МПа при величинах рН от 4,0 до 6,5. Инактивация давлением происходила быстрее при рН в интервале от 5 до 4. Авторы высказывают предположение, что гидростатическое давление может влиять на рН внутри клетки микроорганизма благодаря усилению диссоциации слабых органических кислот, увеличению проницаемости цитоплазматических мембран и инактивации ферментов, необходимых для гомеостаза рН. Есть основания полагать, что основной причиной изменения кислотности может быть смещение равновесного значения рН водного окружения под воздействием высокого давления.
В работе [6] исследовалось влияние высокого давления на инактивацию мезофильных аэробных и факультативно анаэробных микроорганизмов (МАФАМ) в вишневом соке [4] с рН = 6,1 и в яблочном пюре [2] с рН = 5,3. После обработки высоким давлением (0-600 МПа) изучался количественный и качественный состав микрофлоры образцов. На рис. 9.1 представлены кривые, интерполировать полученные экспериментальные данные (тема 6) для различных температур T и экспозиций t.
Как видим, имеет место важное смещение кривых в сторону меньших давлений (примерно на 150 МПа) при увеличении кислотности образца на 0,7 от рН = 6,1 в вишневом соке до рН = 5,4 в яблочном пюре. Этот результат подтверждает факт роста скорости инактивации микроорганизмов под давлением, когда уменьшается рН. Размер смещение согласуется с данными [41], согласно которым кислотность продуктов питания увеличивается от 0,2 до 0,5 единиц рН на каждые 100 МПа.
В отличие от микроорганизмов, витамин С стабилизируется при повышении кислотности среды. В табл. 4.3 приведены результаты экспериментальных исследований влияния давления на содержание витамина С в средах с различной кислотностью. Результаты измерений, изображены на рис. 4.5, свидетельствуют, что влияние высокого давления на растворы с большим рН вызывает большую деградацию витамина С. Тот же эффект дает увеличение времени обработки давлением.
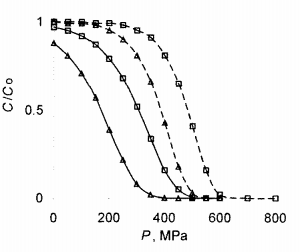
Рис.9.1 – Выживаемость МАФАМ (относительное количество КУЕ) в зависимости от давления Р в вишневом соке [4] (штрихованные) с рН = 6,1 и в яблочном пюре [2] (непрерывные линии) с рН = 5,3 для случаев T = 30°C, T = 20 мин (треугольники) и T = 25°C, t = 10 мин(квадраты)
Рост кислотности пищевых продуктов с повышением давления согласуется с хорошо изученным ростом диссоциации молекул воды при повышении давления и температуры [140, 141]. Данные о диссоциации воды при различных давлениях и температурах можно интерполировать, используя условие термодинамического равновесия нейтральных и ионизированных молекул воды. В результате для водородного показателя воды получаем формулу, применимую при давлении до 1000 МПа и температурах до 100 °С
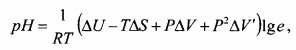 (9.5)
(9.5)
Где изменение свободной энергии ∆U = 6,4 ккал- 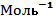 , энтропии ∆S = 0,0106 ккал-
, энтропии ∆S = 0,0106 ккал- 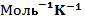 , объема ∆V = –12 мл-
, объема ∆V = –12 мл- 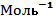 и производная объема по давлению ∆V′ =
и производная объема по давлению ∆V′ =
0,0055 мл- Моль-1 МП.
На рис.9.2 приведен график зависимости равновесного значения рН от давления и температуры, рассчитанной по формуле (9.5).
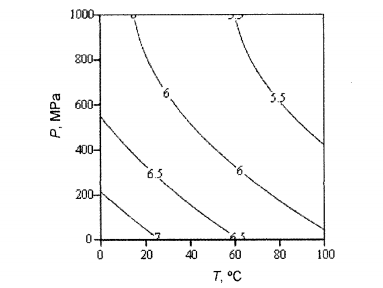
Рис.9.2 –Равновесные значения рН для воды в зависимости от давления и температуры, рассчитанные по формуле (9.5)
Как видно из графика, увеличение давления на 100 МПа уменьшает рН примерно так же, как увеличение температуры на 10°С. Исходя с (9.5), можно получить при нормальных условиях оценки производных 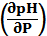
∽0,002 Мп 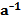 и
и 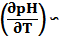 0,02
0,02 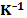 , которые дают возможность сравнить действие давления и температуры на степень ионизации воды. Не случайным представляется совпадение изменений показателя рН в интервалах стерилизующих действия температуры 60-100°С и давление 500-1000 МПа. Можно предположить, что именно изменение рН с ростом как температуры, так и давления, приводит к денатурации белков и, соответственно, к инактивации микроорганизмов. Такое предположение выглядит вполне оправданным, если вспомнить, что вместе с тепловой денатурацией существует и «холодовая» денатурация белка при аномальном понижении температуры [97]. Форма кривой температурного оптимума тесно коррелирует с оптимумом кислотным. Отклонение кислотности ∆рН или температуры ∆T выше или ниже оптимального значения приводят к денатурации. Давление, в отличие от ∆pН и ∆T, трудно сделать отрицательным, однако в области роста Р форма кривых выживаемости (см. Рис. 9.1) также коррелирует с формами температурного и кислотного оптимума.
, которые дают возможность сравнить действие давления и температуры на степень ионизации воды. Не случайным представляется совпадение изменений показателя рН в интервалах стерилизующих действия температуры 60-100°С и давление 500-1000 МПа. Можно предположить, что именно изменение рН с ростом как температуры, так и давления, приводит к денатурации белков и, соответственно, к инактивации микроорганизмов. Такое предположение выглядит вполне оправданным, если вспомнить, что вместе с тепловой денатурацией существует и «холодовая» денатурация белка при аномальном понижении температуры [97]. Форма кривой температурного оптимума тесно коррелирует с оптимумом кислотным. Отклонение кислотности ∆рН или температуры ∆T выше или ниже оптимального значения приводят к денатурации. Давление, в отличие от ∆pН и ∆T, трудно сделать отрицательным, однако в области роста Р форма кривых выживаемости (см. Рис. 9.1) также коррелирует с формами температурного и кислотного оптимума.
Итак, белки и ферменты в живых организмах всегда функционируют в определенном интервале рН. Действие многих денатуратов основано на изменении рН среды. При стерилизации продуктов высоким давлением скорость инактивации микроорганизмов возрастает при повышении кислотности среды, в то же время под давлением замедляется деградация витамина С (аскорбиновой кислоты), что свидетельствует о понижении равновесного рН водной среды под давлением. Поэтому можно предположить, что денатурирующее действие высокого давления обусловлено, в основном, сопутствующим изменением рН среды, а инактивация клетки является вторичным эффектом, вызванным изменением рН клетки при повышении давления.
Дополнительные аргументы за или против этого утверждения можно было бы получить, перечислив полуширину пика кислотного оптимума на соответствующие значения для оптимума по температуре и давлению. К сожалению, для такого сравнения пока не хватает опытных данных с конкретными продуктами. Можно сделать только очень грубые оценки, ориентируясь на примерно одинаковые для многих микроорганизмов критические значения давления ~500 МПа (при 25°С) или температуры стерилизации ~60°С (при Р=0). Эти действия вызывают примерно одинаковое уменьшение равновесного рН воды (см. Рис. 9.2). Считаем инактивацию микроорганизмов, происходящую при этом, следствием изменения рН, получаем соответствующую на полуширину кислотного оптимума около 1-2 единицы рН, согласуемую с данными для большинства микроорганизмов.
Вопросы для самоконтроля
1. Какие факторы приводят к спонтанной диссоциации воды?
2. Как зависит степень диссоциации от температуры среды?
3. Что определяет константа химического равновесия диссоциации?
4. Как определить концентрацию гидроксидов, если известно значение рН?
5. Как влияет кислотность среды на степень инактивации при обработке продуктов питания высоким давлением?
6. Чем обусловлено рост кислотности пищевых продуктов при повышении давления?
7. Как меняются равновесные значения рН для воды с ростом давления или температуры?
Задачи и примеры
1. Найти, как изменяется рН воды при росте температуры от 20 до 80 °С при нормальном давлении. Меняется при этом концентрация гидроксида?
2. Найти, как изменяется рН воды при росте давления от 100 до 600 мпа при температуре 20 °С. Меняется при этом концентрация гидроксида?
3. Пользуясь формулой (9.5), найдите производную 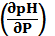 Для давления 200 мпа и температуре 20 °С.
Для давления 200 мпа и температуре 20 °С.
4. Пользуясь формулой (9.5), найдите производную 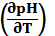 Для давления 200 мпа и температуре 20 °С.
Для давления 200 мпа и температуре 20 °С.
Дата добавления: 2021-09-25; просмотров: 902;











