Электролиз и его применение. Законы Фарадея
При пропускании тока через электролитическую ванну электронные потоки в электродах замыкаются ионными потоками электролита. При этом у анода будет происходить превращение анионов в нейтральные атомы с отдачей электронов аноду; у катода – превращение катионов в нейтральные атомы с получением электронов от катода. У поверхности электродов происходит выделение веществ – это сущность электролиза.
Законы электролиза (Фарадея). Первый закон – масса вещества, выделившегося на электроде, прямо пропорциональна заряду, прошедшему через электролит 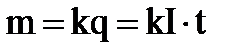 , второй закон – электрохимические эквиваленты прямо пропорциональны их химическим эквивалентам х
, второй закон – электрохимические эквиваленты прямо пропорциональны их химическим эквивалентам х 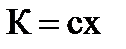 , где : А – атомный вес вещества, Z – его валентность. Число Фарадея – равно электрическому заряду, который нужно пропустить через электролит для выделения на электроде 1 моля вещества.
, где : А – атомный вес вещества, Z – его валентность. Число Фарадея – равно электрическому заряду, который нужно пропустить через электролит для выделения на электроде 1 моля вещества. 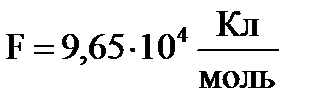 .Третий объединенный закон -
.Третий объединенный закон - 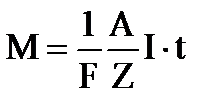 .
.
Вопросы для самоконтроля:
1) Дайте определение электрическому току?
2) Что такое направление тока?
3) Единица измерения, плотность тока?
4) Закон Ома? Что называется работой постоянного тока?
5) Мощность постоянного тока?
6) Механизм проводимости водных растворов электролитов?
7) Какие законы электролиза вы знаете?
8) Что называется электролитической диссоциацией?
Список литературы
Основная
1.Рогачев, Н.М. Курс физики. Учебное пособие/ Н.М. Рогачев. –С.-Петербург: Издательство «Лань», 2010 г. - 448 с.
Дополнительная
2. Грабовский, Р.И. Курс физики. 6-е изд. / Р. И. Грабовский. – СПБ. : Издательство «Лань», 2002. – 608 с
Лекция 11
Дата добавления: 2017-06-13; просмотров: 1215;











