Связь работы обратимого процесса с эксергией.
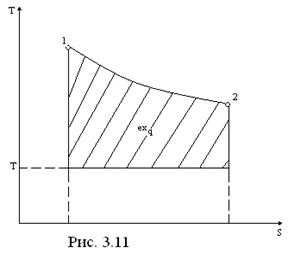 Для обратимого процесса расширения рабочего тела 1-2 (Рис. 3.11) можно записать следующее уравнение:
Для обратимого процесса расширения рабочего тела 1-2 (Рис. 3.11) можно записать следующее уравнение:
l = q - (h2 - h1), (3.20)
exl = (h l- hoc) – Toc (Sl – Soc) (3.21)
ex2 = (h2 – hoc) – Toc (S2 – Soc) (3.22)
Совместное их решение дает формулу
l = ex1 – ex2 + exq, (3.23)
согласно которой работа любого обратимого процесса определяется значениями эксергией начального и конечного состояний и эксергией теплоты процесса.
Реальные процессы необратимы. В процессах расширения получается меньшая работа (l 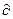 < l). Разность работ обратимого (l) и необратимого (l
< l). Разность работ обратимого (l) и необратимого (l 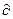 ) процессов представляет собой потерю эксергиии
) процессов представляет собой потерю эксергиии
l- l 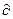 = Δex nom = (ex1 – ex2 + exq) - l
= Δex nom = (ex1 – ex2 + exq) - l 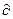 (3.24)
(3.24)
Для процессов расширения и сжатия справедливо выражение
Δexnom = (ex1 – ex2 ±exq)  l
l 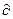 (3.25)
(3.25)
Формулы (3.12), (3.19), (3.25) лежат в основе эксергетического анализа процессов и циклов тепловых двигателей и аппаратов.
3.8. Эксергетический КПД
Эксергетический КПД теплового двигателя или аппарата учитывает все потери данного устройства и рассчитывается по формуле
 (3.26)
(3.26)
где exподв – затраченная энергия, полностью превратимая в другие виды энергии, exотв – полученная (полезная) энергия.
Разность между ними представляет собой потерю эксергии
еxподв – exотв = exпот (3.27)
С учетом выражения (3.27) формулу (3.26) можно представить в следующем виде:
 (3.28)
(3.28)
Эксергетический КПД является характетикой термодинамического совершенства реальных процессов и циклов, протекающих в энергетическом оборудовании.
3.9. Методические указания
1. Теплота и работа представляют собой формы передачи энергии и могут переходить друг в друга. Работа (механическая энергия) полностью превращается в теплоту. Теплоту же полностью превратить в механическую энергию нельзя. На вопрос, «какую часть теплоты можно превратить в работу?», дает ответ второй закон термодинамики. Этот закон также определяет направление естественных процессов (формулировки Клазиуса, Больцмана) и характеризует качественную сторону процессов преобразования теплоты в работу. Показателем качества тепла является эксергия.
В отличие от первого закона термодинамики, являющегося абсолютным законом природы, справедливым как для макромира, так и для микромира, второй закон термодинамики получен на основании опыта для макросистем в условиях Земли и не может произвольно распространяться как на бесконечную Вселенную, так и на микромир.
2. Обратите внимание: для обратимого цикла Карно температура горячего источника (Тги) и температура подвода теплоты к рабочему телу (Т1) совпадают – Тги = Т1; температура холодного источника (Тхи) и температура отвода теплоты от рабочего тела (Т2) совпадают – Тхи = Т2. Следовательно, процессы теплообмена между рабочим телом и источниками тепла – внешне обратимые.
Адиабатные процессы сжатия и расширения рабочего тела – внутренне обратимые (без трения).
В реальных циклах все эти процессы необратимы.
3.10. Вопросы и задачи
1. В чем суть известной в философии концепции «тепловой смерти Вселенной» с позиций второго закона термодинамики?
2. Назовите известные Вам формулировки второго закона термодинамики и запишите его математическое выражение для обратимых и необратимых процессов.
3. Что такое эксергия? Можно ли утвердить, что потеря эксергии определяет уменьшение работоспособности термодинамической системы?
4. Дайте понятия термического и эксергетического КПД. Могут ли эти КПД быть равными единице и при каких условиях?
5. Чтобы испарить 1 кг кипящей воды при давлении 760 мм рт. ст., необходимо подвести 2257 кДж/кг теплоты. Рассчитайте изменение энтропии в этом процессе. Какова эксергия подводимой теплоты, если температура окружающей среды равна 20 оС?
6. В паровом котле теплота в количестве 1000 МВт передается от дымовых газов с температурой 2000 оС к воде и водяному пару со средней температурой 350 оС. Рассчитайте потерю эксергии, если температура окружающей среды равна 0 оС.
7. Для цикла Карно известны: температура подвода 500 оС, температура отвода тепла 20 оС, работа цикла l= 820 кДж/кг. Рассчитайте подводимую теплоту (q1) и изменение энтропии в цикле (ΔS).
3.11. Ответы
4. Термический КПД – характеристика обратимых циклов. Он не может быть равным 1, тт.к. невозможно всю подводимую теплоту превратить в работу.
Эксергетический КПД характеризует степень необратимости реальных процессов и циклов, и он может быть равен 1 для обратимых процессов и циклов.
5. Δs= 6,05 кДж/(кгК), ехq = 484,1 кДж/кг. 6. Δехпот = 318,1кДж/кг. 7. q1 = 1320 кДж/кг, Δs= 1,708кДж/(кгК).
Дата добавления: 2021-07-22; просмотров: 534;











