Стереохимия аминокислот
Все аминокислоты обладают оптической активностью, т.е. способностью вращать плоскость поляризованного луча. Оптической активностью обладают все соединения, способные существовать в двух формах, представляющих по своей структуре несовместимые зеркальные отражения друг друга. Все стереоизомеры аминокислот структурно соответствуют 2 изомерам глицеральдегида. Стереоизомеры, соответствующие L-глицеральдегиду, обозначаются буквой L, а стереоизомеры D-глицеральдегида - буквой D. Таким образом, символы D и L соответствуют абсолютной конфигурации, а не направлению вращения. Все встречающиеся в белках аминокислоты принадлежат к L-ряду. D-аминокислоты могут встречаться в клетках.
Связи, стабилизирующие белковую молекулу
Аминокислоты способны образовывать связи с различными реакционно-способными группами. Это свойство важно для структуры белков.
Пептидные связи
Пептидная связь образуется в результате выделения молекулы воды при взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой. Реакция с выделением воды называется реакцией конденсации, а возникающая ковалентная азот-углеродная связь – пептидной. Соединение, образующееся в результате конденсации двух аминокислот, называется дипептидом. На одном конце его молекулы находится свободная аминогруппа, на другом конце – свободная карбоксильная группа. Если таким образом соединяется много аминокислот, то такое соединение называется полипептид.
R1 H
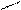
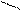
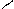
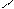
 H | O H | O
H | O H | O
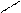


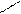 N –––– C ––––– C N ––– C –––– C
N –––– C ––––– C N ––– C –––– C
 H | OH H | OH
H | OH H | OH
 H R2
H R2
 |
 Конденсация
Конденсация
 H2O
H2O
R1 O H

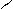
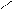
 H | || | O
H | || | O
 N –––– C –––––– C –––––– N –––– C –––– C Дипептид
N –––– C –––––– C –––––– N –––– C –––– C Дипептид
H | | | OH
H H R2
R1 O R3
| H || |

 CH N C CH
CH N C CH
N C CH N C
H || | H ||
O R2 O
Дата добавления: 2017-04-05; просмотров: 1704;











