Строение ДЭС на границе раствор-металл
Двойной электрический слой создается электрическими зарядами, находящимися на металле ионами противоположного заряда (противоионами), ориентированными у поверхности электрода.
Формулирование ионной обкладки ДЭС происходит за счет электростатических сил и сил теплового движения, за счет последних сил ДЭС приобретает размытое диффузное строение. В создании ДЭС существенная роль принадлежит специфической абсорбции ионов.
Под строением ДЭС понимают распределение зарядов в его ионной обкладке. (Гельмгольц, Штерн, Фрумкин). ДЭС состоит из двух частей:
1) Плотная или гельмгольцевская часть, образованная ионами, плотно подошедшими к поверхности металла (10-8см);
2) Диффузная часть, созданная ионами, находящимися от металла на расстоянии большем радиуса сольватированного иона (10-7-10-3см).
Рассмотрим пример: Проводник I рода (Cu) поместили в раствор CuSO4 (проводник II рода).
 Металл: в узлах кристаллической решетки находятся ионы меди, расположенные упорядоченно. В растворе электролита и у поверхности ионы Cu2+ покрыты сольватной оболочкой из молекул воды.
Металл: в узлах кристаллической решетки находятся ионы меди, расположенные упорядоченно. В растворе электролита и у поверхности ионы Cu2+ покрыты сольватной оболочкой из молекул воды.
При равновесии 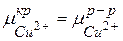
Рассмотрим два случая:
1) 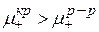 , т.е. химический потенциал катиона в кристаллической решетке больше химического потенциала катиона в растворе.
, т.е. химический потенциал катиона в кристаллической решетке больше химического потенциала катиона в растворе.
В этом случае ионы металла из твердого тела (проводника I р.) будут переходить в раствор до тех пор, пока: 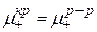 .
.
Поверхность металла заряжается отрицательно.

ψ – потенциал на границе металл - раствор
ψ1 – падение потенциала в плотном слое
ψ2 – падение потенциала в диффузной части.
ДЭС представляет собой как бы обкладку конденсатора.
2) 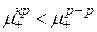 Ионы из раствора переходят на поверхность металла, заряжая ее положительно.
Ионы из раствора переходят на поверхность металла, заряжая ее положительно.

ДЭС возникает всегда на границе: проводник I рода – проводник II рода.
В целом ДЭС электронейтрален, его толщина зависит от концентрации раствора, заряда металла и температуры.
В концентрированных растворах диффузная часть практически отсутствует.
Дата добавления: 2017-03-12; просмотров: 2042;











