Поверхностное натяжение.
Суммарная энергия частиц жидкости складывается из энергии их хаотического (теплового) движения и потенциальной энергии, обусловленной силами межмолекулярного взаимодействия. Для перемещения молекулы из глубины жидкости в поверхностный слой надо затратить работу. Эта работа совершается за счет кинетической энергии молекул и идет на увеличение их потенциальной энергии. Поэтому молекулы поверхностного слоя жидкости обладают большей потенциальной энергией, чем молекулы внутри жидкости. Эта дополнительная энергия, которой обладают молекулы в поверхностном слое жидкости, называемая поверхностной энергией, пропорциональна площади слоя DS:
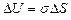 (9.6.1)
(9.6.1)
где 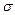 – коэффициент поверхностного натяжения.
– коэффициент поверхностного натяжения.
Так как равновесное состояние характеризуется минимумом потенциальной энергии, то жидкость при отсутствии внешних сил будет принимать такую форму, чтобы при заданном объеме она имела минимальную поверхность, т.е. форму шара. Наблюдая мельчайшие капельки, взвешенные в воздухе, можем видеть, что они действительно имеют форму шариков, но несколько искаженную из-за действия сил земного тяготения.
Итак, условием устойчивого равновесия жидкости является минимум поверхностной энергии. Это означает, что жидкость при заданном объеме должна иметь наименьшую площадь поверхности, т. е. жидкость стремится сократить площадь свободной поверхности. В этом случае поверхностный слой жидкости можно уподобить растянутой упругой пленке, в которой действуют силы натяжения.

Рассмотрим поверхность жидкости (рис.9.10), ограниченную замкнутым контуром. Под действием сил поверхностного натяжения (направлены по касательной к поверхности жидкости и перпендикулярно участку контура, на который они действуют) поверхность жидкости сократилась и рассматриваемый контур переместился в положение, отмеченное штриховой линией. Силы, действующие со стороны выделенного участка на граничащие с ним участки, совершают работу
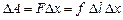 ,
,
где f – сила поверхностного натяжения, действующая на единицу длины контура поверхности жидкости. Но 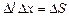 , тогда
, тогда
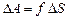 . (9.6.2)
. (9.6.2)
Эта работа совершается за счет уменьшения поверхностной энергии, то есть 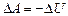 .
.
Сравнивая (9.6.1) и (90.6.2), видим что 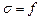 , то есть коэффициент поверхностного натяжения может быть определен как величина, равная силе, действующей по касательной к поверхности жидкости, приходящейся на единицу длины линии раздела.([
, то есть коэффициент поверхностного натяжения может быть определен как величина, равная силе, действующей по касательной к поверхности жидкости, приходящейся на единицу длины линии раздела.([ 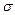 ]=Н/м. )
]=Н/м. )
Из(9.6.2) можно видеть также, что коэффициент поверхностного натяжения измеряется работой, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу. [ 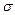 ]=Дж/м2.
]=Дж/м2.
Из (9.6.1) следует, что изменение площади поверхности dS влечет за собой изменение потенциальной энергии
dUs=s dS,
которое сопровождается совершением работы 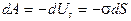 .
.
Если изменение поверхности осуществляется изотермически, то, как известно, необходимая для этого работа равна изменению свободной энергии: 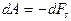 .
.
Если изменение поверхности жидкости происходит адиабатно, то ее температура изменится.
Значит, избыточная потенциальная энергия поверхности жидкости является свободной энергией поверхности и, следовательно, 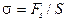 , то есть коэффициент поверхностного натяжения жидкости можно определить как свободную энергию единицы площади этой поверхности.
, то есть коэффициент поверхностного натяжения жидкости можно определить как свободную энергию единицы площади этой поверхности.
Большинство жидкостей при температуре 300 К имеет поверхностное натяжение порядка 10-2-10-1 Н/м. Поверхностное натяжение с повышением температуры уменьшается, так как увеличиваются средние расстояния между молекулами жидкости.
Поверхностное натяжение существенным образом зависит от примесей,имеющихся в жидкостях.Вещества, ослабляющие поверхностное натяжение жидкости, называются поверхностно-активными. Наиболее известным поверхностно-активным веществом отношению к воде является мыло. Оно сильно уменьшает ее поверхностное натяжение (примерно с 7,3.10-2 до 4,5.10-2Н/м). Поверхностно-активными веществами, понижающими поверхностное натяжение воды, являются также спирты, эфиры, нефть и др.
Существуют вещества (сахар, соль), которые увеличивают поверхностное натяжение жидкости благодаря тому, что их молекулы взаимодействуют с молекулами жидкости сильнее, чем молекулы жидкости между собой. Например, если посолить мыльный раствор, то в поверхностный слой жидкости выталкивается молекул больше, чем в пресной воде. В мыловаренной технике мыло «высаливается» этимспособом из раствора.
Дата добавления: 2016-12-09; просмотров: 2099;











